Srdeční selhání se zachovalou ejekční frakcí levé komory (heart failure with preserved ejection fraction, HFpEF) je podle posledních doporučení Evropské kardiologické společnosti definováno přítomností symptomů a příznaků srdečního selhání, hodnotou ejekční frakce levé komory >= 50 % a dále zvýšenou hladinou natriuretických peptidů a/nebo alespoň jedním z dalších kritérií, kterými jsou přítomnost strukturálního onemocnění srdce (hypertrofie stěny levé komory nebo zvětšení objemu levé síně) nebo porucha diastolické funkce levé komory.
Již z definice je jasné, že stanovení hladiny natriuretických peptidů má klíčový význam pro diagnostiku tohoto typu selhání. Rozdíly v definici jednotlivých typů srdečního selhání ukazuje tabulka č. 1.

Epidemiologie srdečního selhání se zachovalou funkcí levé komory
V porovnání s pacienty se sníženou funkcí levé komory (HFrEF) jsou pacienti se srdečním selháním se zachovalou funkcí levé komory starší, častěji ženy, velmi často trpí arteriální hypertenzí a fibrilací síní. Přesná čísla výskytu nejsou známa, ale data z některých registrů hospitalizací pro srdeční selhání poskytují údaje o poměru mezi oběma typy srdečního selhání. Podíl pacientů se zachovalou ejekční frakcí se pohybuje kolem 50 % všech hospitalizací pro srdeční selhání (podle Framingham Heart Study kolem 41 %, podle Cardiovascular Health Study a podle dat z Mayo kliniky 55 %). Prevalence se pohybuje kolem 1 %.
Patofyziologie HFpEF
Základním patogenetickým mechanismem u tohoto typu srdečního selhání je porucha hemodynamiky v důsledku poruchy relaxace a/nebo zvýšení tuhosti stěny levé komory, které vyžadují zvýšení jejího plnicího tlaku. Zvýšení plnicího tlaku levé komory se přenáší na síň, plicní řečiště a pravou komoru, přičemž dochází k manifestaci srdečního selhání. Stav je provázen aktivací neurohumorálních systémů (systému renin-angiotenzin-aldosteron a sympatického nervového systému). Důsledkem těchto změn je progrese remodelace myokardu provázená často jeho zvýšenou fibrózou.
Tyto patofyziologické změny vedou k rozvoji poruchy diastolické funkce levé komory srdeční (diastolická dysfunkce levé komory, DD). Diastolická dysfunkce levé komory tedy může vzniknout v důsledku poruchy relaxace (vlivem ischemické choroby srdeční, věku či v důsledku přítomnosti kardiomyopatie), dále poruchy poddajnosti její stěny (při hypertrofii a/nebo zvýšené fibróze myokardu), dále v důsledku konstrikce myokardu nebo v důsledku dlouhého trvání některých tachyarytmií. Tabulka č. 2 ukazuje klinické stavy, které jsou provázeny diastolickou dysfunkcí levé komory. V praxi jde nejčastěji o pacienty s arteriální hypertenzí, chronickou ischemickou chorobou srdeční a kardiomyopatiemi, kteří jsou starší a často mají diabetes mellitus.
Diagnostika srdečního selhání se zachovalou ejekční frakcí levé komory – klíčová role natriuretických peptidů

U nemocných se symptomy srdečního selhání s normální funkcí levé komory má naprosto klíčový význam průkaz zvýšené hladiny natriuretických peptidů. V nejnovějších doporučeních pro diagnostiku a terapii srdečního selhání byly stanoveny horní hranice normy: pro mozkový natriuretický peptid (BNP) do 35 pg/ml a pro N-terminální fragment mozkového natriuretického peptidu (NT-proBNP) do 125 pg/ml. Tyto hodnoty byly zvoleny na základě rozsáhlé analýzy řady studií s cílem získat co nejvyšší negativní prediktivní hodnotu.
Hodnoty natriuretických peptidů při akutní dekompenzaci dosahují u tohoto typu selhání vysokých hodnot (např. při edému plic), avšak při porovnání se srdečním selháním se sníženou funkcí levé komory je mírnější průběh selhání se zachovalou funkcí levé komory provázen nižšími hodnotami. Proto má velký význam znalost všech stavů, které mohou vést k jejich zvýšení: kromě selhání levé komory je to hypertrofie stěny levé komory, infiltrativní procesy myokardu, tako-tsubo kardiomyopatie, myokarditida, chlopenní vady, arytmie, akutní koronární syndromy, užití některých drog, chemoterapie (nejenom antracykliny), terapie inhibitory neprilysinu (pouze BNP), pokročilá onemocnění plic (ARDS, onemocnění provázená selháním pravého srdce), plicní hypertenze, sleep apnea syndrom, pokročilý věk, dysfunkce ledvin, anémie, některé kritické stavy (popáleniny, mozkové příhody, sepse), stavy se zvýšeným minutovým výdejem (cirhóza jater, hypertyreóza).
Kromě výše uvedených stavů je třeba věnovat pozornost i stavům, kdy zvýšení hladiny natriuretických peptidů neodpovídá tíži klinického stavu. Mezi tyto stavy patří tzv. bleskové (flash) edémy plic, ke kterým může dojít právě u nemocných se srdečním selháním se zachovalou funkcí levé komory srdeční (např. v důsledku neléčené arteriální hypertenze) či u nemocných s mitrální stenózou. V porovnání s edémy plic, které vznikají v důsledku postupného zhoršování funkce levé komory, je vznik edému plic tak rychlý, že v prvních hodinách nemusí být vzestup hladiny natriuretických peptidů stejně rychlý a vrcholu je dosaženo se zpožděním.
V souvislosti s nutností včasné identifikace pacientů se sublinickými formami srdečního selhání se zachovalou ejekční frakcí se obrací pozornost ke stanovení natriuretických peptidů, které dokážou velmi jemně odrazit počínající stadia onemocnění. Této unikátní vlastnosti bylo využito v řadě studií. Patří mezi ně například studie Luerse C. et al., kteří v souboru 542 pacientů v primární péči bez známého srdečního selhání provedli stanovení hladiny NT-proBNP a doplnili je podrobným klinickým vyšetřením včetně echokardiografie. Prokázali, že hladiny NT-proBNP neodhalily spolehlivě pouze pacienty s nízkou ejekční frakcí, ale navíc úspěšně identifikovaly pacienty se zatím asymptomatickými formami poruchy diastolické funkce levé komory.
Další metody průkazu HFpEF
K úplnému stanovení diagnózy HFpEF je nutné prokázat přítomnost strukturálního postižení myokardu a/nebo poruchy diastolické funkce levé komory. Tyto parametry se získávají při echokardiografickém vyšetření. Strukturální změny myokardu spojené s poruchou diastolické funkce představují dva nálezy: hypertrofie stěny levé komory a/nebo zvětšený objem levé síně srdeční. Oba tyto nálezy jsou úzce spojeny s příčinami tohoto typu selhání. Hypertrofie myokardu vzniká často v důsledku zvýšení tlaku uvnitř komory srdeční (příčinou je arteriální hypertenze, srdeční vada či kardiomyopatie) a je provázena změnou diastolické poddajnosti stěny levé komory. Echokardiograficky lze při transtorakálním vyšetření určit s jistou mírou přesnosti stupeň hypertrofie levé komory vyjádřený indexem masy levé komory vztaženým na povrch těla (left ventricle mass index, LVMi), za hypertrofii jsou považovány hodnoty >= 115 g/m2 u mužů a >= 95 g/m2 u žen. Z řady předchozích studií je známa velmi silná asociace hypertrofie stěny komory a hladiny natriuretických peptidů (obr. č. 1). Zařazení morfologického ukazatele a současný průkaz zvýšení hladiny natriuretických peptidů posilují diagnostickou sílu testů.
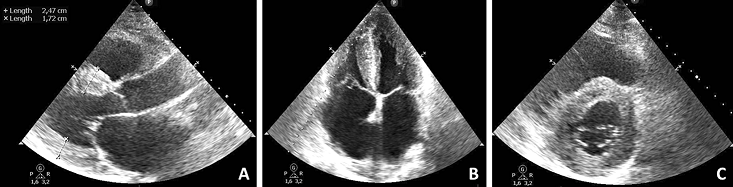
Obrázek ukazuje zesílenou stěnu myokardu u nemocného se zachovalou systolickou funkcí levé komory a poruchou diastolické funkce. Zesílení stěny levé komory srdeční dosahuje vysokého stupně (normální tloušťka stěny myokardu levé komory se pohybuje do 11–12 mm, hodnoty nad 15 mm budí podezření na hypertrofickou kardiomyopatii). U nemocného byla diagnostikována amyloidóza myokardu. Obrázek vlevo (A) ukazuje parasternální projekci s mírami septa a zadní stěny levé komory, střední obrázek (B) ukazuje apikální projekci ukazující významnou dilataci obou síní, obrázek vpravo (C) ukazuje projekci levé komory v příčném řezu.
Druhým strukturálním parametrem je velikost levé síně, která je zde hodnocena objemem (left atrial volume, LAV) a jeho indexem na plochu těla (LAVi). Ke zvětšení levé síně dochází v důsledku zvýšení intrakardiálního tlaku uvnitř levé komory (levá síň je tenkostěnná a podstatně snáze dilatuje). I tento stav je provázen zvýšením hladiny natriuretických peptidů (v důsledku zvýšení napětí myocytů). Stanovení objemu levé síně se provádí při běžném vyšetření výpočtem ploch levé síně z projekcí na sebe kolmých. Za patologickou hodnotu se považuje index objemu levé síně (LAVi) nad 34 ml/m2.
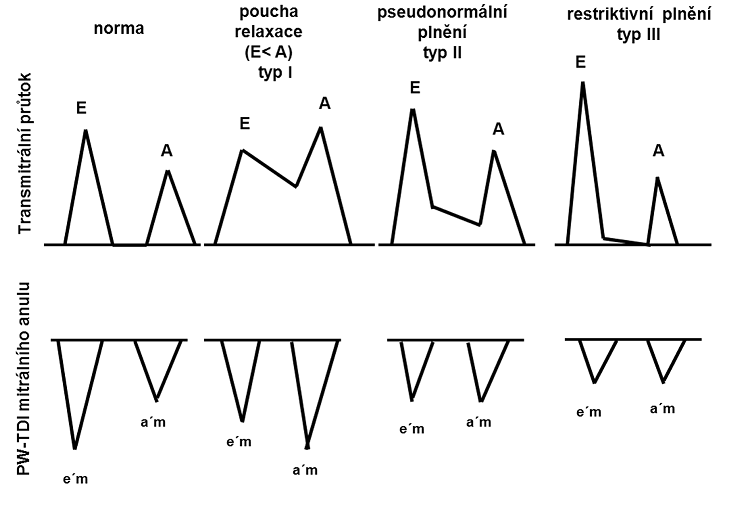
Transmitrální průtok hodnocen pulzním dopplerovským vyšetřením: E = vlna pasivního plnění levé komory; A = vlna aktivního plnění levé komory (systola síně); PW-TDI = pulzně dopplerovská analýza mitrálního anulu; e´m = tzv e-prime, vlna vzniklá pasivním plněním levé komory; a´m = odpovídá aktivnímu plnění.
Echokardiografie umožňuje detekovat poruchu diastolické funkce levé komory srdeční. Využívá k tomu dopplerovských metod: hodnocení průtoku mitrální chlopní v době diastoly komory pulzním Dopplerem a metodu tkáňově dopplerovského hodnocení pohybů prstence mitrální chlopně (obr. č. 2 a 3). Je známo, že porucha diastolické funkce levé komory je spojena s vyšším tlakem uvnitř levé komory na konci její diastoly (end-diastolický tlak levé komory), toto vede k ovlivnění jejího plnění – přesunu krve ze síní přes mitrální chlopeň do komory. Na základě hodnocení těchto parametrů jsme schopni stanovit někdy i stupně diastolické poruchy (v případě sinusového rytmu). Echokardiografický obraz dokresluje přítomnost plicní hypertenze (určuje se z hodnoty vrcholového gradientu na trikuspidální regurgitace). V souvislosti s využíváním zobrazovacích metod je nutné připomenout, že řada studií prokázala spojitost mezi echokardiografickými parametry a hladinou natriuretických peptidů (např. práce Troughtona a Richardse, kteří analyzovali hladiny BNP i NT-proBNP u pacientů se známkami diastolické dysfunkce levé komory a prokázali jako jedni z prvních jejich významnou asociaci).
Terapie srdečního selhání se zachovalou funkcí levé komory srdeční
Doposud nemáme důkazy o jasném snížení mortalitních ukazatelů nemocných s tímto typem srdečního selhávání. V případě známek retence tekutiny jsou namístě diuretika, výsledky některých studií naznačily příznivý efekt betablokátorů, inhibitorů angitenzin-konvertujícího enzymu/sartanů. Nicméně lze důrazně doporučit podrobné vyšetření těchto nemocných s cílem odhalení příčiny, která vedla k tomuto typu selhání, a tuto příčinu intenzivně léčit (arteriální hypertenze, chronická ICHS a podobně).
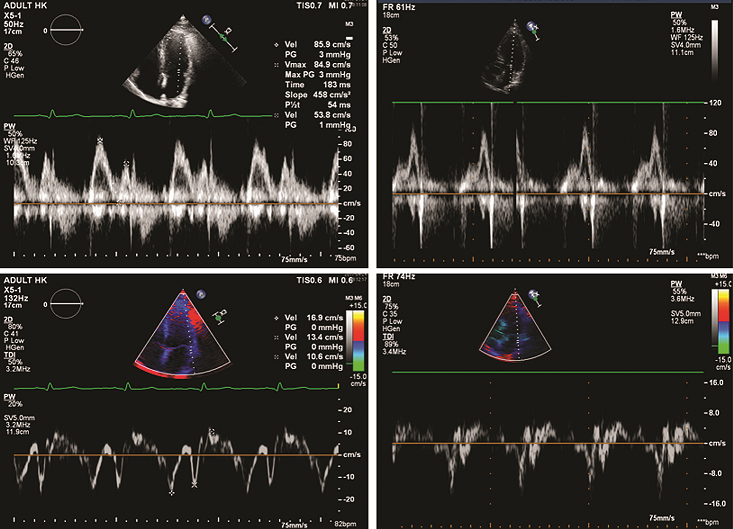
Dvojice obrázků v levém sloupci ukazuje normální průběh plnění levé komory s vyznačením vln E a A; dvojice obrázků v pravém sloupci ukazuje poruchu diastolické funkce levé komory. Nahoře vždy pulzně dopplerovský obraz plnění levé komory (vzorkovací objem je umístěn mezi vrcholy cípů mitrální chlopně); dole tkáňově dopplerovské charakteristiky mitrálního anulu (zde laterální část, v praxi vždy hodnotíme i mediální část anulu).
Závěr
Srdeční selhání se zachovalou ejekční frakcí by mohlo být podceňovanou klinickou jednotkou. Z výše uvedeného přehledu vyplývá velké množství pacientů, kterým hrozí riziko tohoto typu selhání. Je namístě si uvědomit nezastupitelnou roli stanovení natriuretických peptidů a echokardiografického vyšetření pro diagnostiku tohoto onemocnění. Ukazuje se, že hladiny natriuretických peptidů mají významné místo také ve stratifikaci rizika těchto nemocných. Ačkoliv je málo dat o specifické terapii tohoto typu srdečního selhání, je nezbytné identifikovat příčinu, která tento typ selhání vyvolala, a tu intenzivně léčit.