Jednou z nejvýznamnějších novinek v nových doporučeních pro diagnostiku a terapii akutního a chronického srdečního selhání je možnost ovlivnit hladiny natriuretických peptidů a využít tak jejich pozitivního vlivu na kardiovaskulární systém. Tuto novou skupinu léků představují inhibitory neprilysinu a blokátory AT1 receptorů pro angiotenzin II, tzv. ARNI, jejichž zatím jediným představitelem je chimérická molekula sacubitrilu a valsartanu.1 V historii terapie pacientů se srdečním selháním je to vůbec poprvé, kdy se dostává tato možnost do evropských doporučení a má vysokou úroveň evidence.
Role natriuretických peptidů v patofyziologii srdečního selhání
Srdeční selhání je charakterizováno jako stav, kdy srdce není schopno při normálním žilním návratu čerpat krev v souladu s potřebami metabolismu tkání, nebo je toho schopno jen při zvýšení plnicích tlaků komor. V patofyziologii srdečního selhání je v současnosti akceptován hemodynamický pohled v kontextu neurohumorální aktivace a progresivní přestavby na makroskopické i ultrastrukturální úrovni. V průběhu srdečního selhání dochází k aktivaci řady systémů, které se vzájemně velmi významně ovlivňují. Patří mezi ně sympatický nervový systém, systém renin-angiotenzin-aldosteron (RAAS), systém natriuretických peptidů, svůj význam mají také další působky (cytokiny, endotelin, vasopresin a další).
Tyto systémy se vyvinuly během fylogeneze a jejich vzájemné působení je výsledkem určité rovnováhy mezi dvěma základními tendencemi: na jedné straně je to snaha o zabezpečení dostatečného perfuzního tlaku orgánů a tkání těla navozením vazokonstrikce, retence sodíku a vody (systém renin-angiotenzin-aldosteron, sympatický nervový systém, vasopresin, endotelin), protiváhou tohoto systému je aktivace systému natriuretických peptidů, který podporuje vazodilataci, stimuluje diurézu, natriurézu a snižuje remodelaci myokardu2,3,4. Zatímco dlouhodobá aktivace systémů první skupiny může mít negativní efekt u pacientů se srdečním selháním, aktivace systému natriuretických peptidů působí ve většině těchto účinků právě opačně a má velmi příznivý efekt na průběh srdečního selhání (tab. č. 1). Proto se objevila snaha ovlivnit hladiny natriuretických peptidů terapeuticky.

Možnosti ovlivnění hladiny natriuretických peptidů u pacientů se srdečním selháním

Snaha využít pozitivních efektů natriuretických peptidů v terapii srdečního selhání není nová. A zahrnuje dva základní přístupy: podání natriuretických peptidů (například analoga a jim podobné látky odolné vůči degradaci) nebo zvýšení hladiny endogenních natriuretických peptidů. Tato historie je zajímavá a stojí za krátkou připomínku. Mezi syntetické natriuretické peptidy, které byly testovány ve velkých klinických studiích, patřil carperitid (HANP, α-human A-type natriuretic peptide), který byl v roce 1995 registrován v Japonsku a jeho efekt byl sledován u souboru 1 200 pacientů s akutním srdečním selháním ve studii COMPASS. Podání carperitidu vedlo ke zlepšení hemodynamiky, současně byl také příznivě ovlivněn systém renin-angiotenzin-aldosteron5. Dalším lékem byl urodilatin (Ularitide, syntetická izoforma ANP), který byl testován ve studiích SIRIUS I, II (pacienti s akutní dekompenzací srdečního selhání) a ve studii True-AHF6. Synteticky připravený mozkový natriuretický peptid – nesiritid (Natrecor) byl testován ve studii VMAC (Vasodilatation in the Management of Acute CHF). Na základě výsledků studie schválila FDA tuto účinnou látku pro terapii pacientů s akutní dekompenzací srdečního selhání7. Podání těchto léků přineslo data o příznivém ovlivnění hemodynamiky v akutních stadiích, nebyly však zcela rozptýleny obavy ze zhoršení renálních funkcí a výskytu symptomatické hypotenze. Proto byly provedeny další 2 studie, které byly zaměřeny na bezpečnost použití.
Zatímco studie ADHERE nepotvrdila obavy, studie ASCEND-HF přinesla neutrální výsledek. Vývoj v této oblasti směřuje k subkutánnímu podání BNP, zatím ojedinělá data potvrzují pozitivní efekt (zlepšení symptomů a redukce masy levé komory srdeční). Druhou možností, jak zvýšit hladinu endogenních natriuretických peptidů, je inhibice neutrální endopeptidázy (neprilysin)8. Neprilysin patří mezi vazopeptidázy. Štěpí/inaktivuje nejenom natriuretické peptidy (ANP, BNP, CNP), ale také další látky (enkefaliny, oxytocin, gastrin, substance P, bradykinin), avšak mezi jinými také angiotenzin I a II. Neprilysin se nalézá ve tkáních mozku, ledvin, endotelií, svaloviny cév, myokardu, v neutrofilech a na dalších místech. První snahy ovlivnit tento systém se objevily v 80. letech, kdy byl testován thiorphan, následně se objevily i další inhibitory neprilysinu (např. candoxatrilát)9. Podání těchto látek mělo velmi příznivý vliv na hladinu natriuretických peptidů, ale současně se také zvyšovala hladina angiotenzinu II a endotelinu 1, které patří mezi vazokonstriktory. Proto vznikl koncept současné blokády neprilysinu a systému renin-angiotenzin-aldosteron. Prvním testovaným duálním inhibitorem (současná inhibice neprilysinu a angiotenzin konvertujícího enzymu) byl omapatrilát10. Ten byl testován ve studii IMPRESS (573 pacientů se sníženou ejekční frakcí levé komory) a dále ve studiích OVERTURE (5 770 pacientů se srdečním selháním, kde byl omapatrilát srovnáván s enalaprilem) a u hypertoniků ve studii OCTAVE. Použití omapatrilátu přineslo velmi příznivá data o zlepšení hemodynamiky léčených pacientů, problémem však zůstával vyšší výskyt angio-edému. Tyto skutečnosti bránily zavedení této velmi nadějné terapie do běžné klinické praxe.
Sacubitril/valsartan
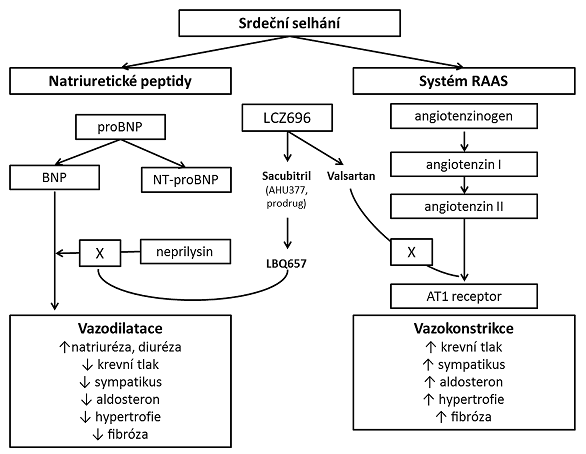
Molekula sacubitril/valsartan má chimérickou strukturu, resp. představuje supramolekulární komplex složený z 6 molekul sacubitrilu a 6 molekul valsartanu. Mechanismus účinku spočívá v současné inhibici neutrální neuroendopeptidázy (neprilysinu) sacubitrilem a blokádě receptorů typu 1 pro angiotenzin II valsartanem11,12. Sacubitril (LCZ696) je proléčivo, které se mění na účinnou látku LBQ657. Výsledkem působení sacubitrilu je zvýšení hladiny mozkového natriuretického peptidu, které přináší aditivní pozitivní efekty pro terapii nemocných se srdečním selháním. Schéma působení sacubitrilu u nemocných se srdečním selháním ukazuje obr. č. 1.
Velice příznivá data o působení této molekuly přinesla studie PARADIGM-HF (Prospective comparison of ARNI with ACEI to Determine Impact on Global Mortailty and morbidity in Heart Failure trial), ve které bylo randomizováno 4 187 pacientů pro terapii zkoušeným lékem (LCZ696) a 4 212 pro terapii enalaprilem13,14. Studii PARADIGM-HF se věnuje další článek tohoto čísla. Výsledky studie byly jednoznačně pozitivní. Terapie sacubitrilem/valsartanem vedla ke statisticky významnému snížení všech hlavních sledovaných ukazatelů (úmrtí z kardiovaskulární příčiny, hospitalizace pro srdeční selhání, celková mortalita léčených pacientů). Tato molekula byla testována i v řadě dalších studií, které přinesly pozitivní výsledky. Velmi příznivý bezpečnostní profil vedl k zařazení této účinné látky do algoritmu doporučení medikamentózní terapie pacientů s chronickým srdečním selháním (obr. č. 2).
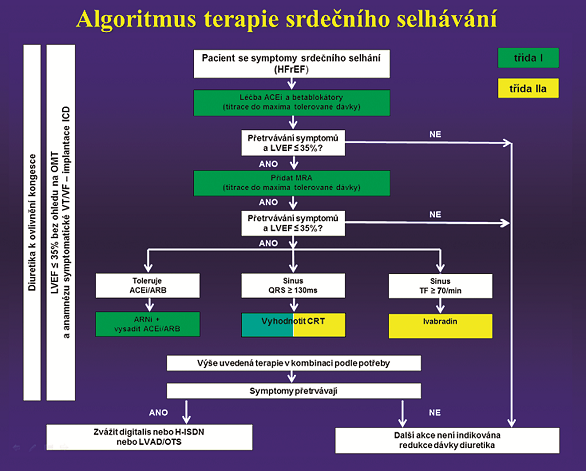
Upraveno podle doporučení ESC pro diagnostiku a léčbu akutního a chronického srdečního selhání 1
Vliv sacubitrilu/valsartanu na hladiny natriuretických peptidů
U pacientů se srdečním selháním následuje po tlakovém a objemovém přetížení srdečních oddílů vzestup hladiny natriuretických peptidů. Proporcionálně dochází ke zvýšení všech sledovaných hladin natriuretických peptidů (BNP, NT-proBNP, ale i dalších). V důsledku úspěšné léčby a nastupující srdeční kompenzace pozorujeme pokles jejich hodnot15. U pacientů léčených sacubitrilem/valsartanem se projeví mechanismus účinku sacubitrilu, který inhibuje neprilysin, a tím dochází k inhibici degradace natriuretických peptidů. V případě mozkového natriuretického peptidu byl zaznamenán fenomén stabilní až lehce zvýšené hladiny BNP. Ve studii PARADIGM-HF byl medián vstupní hodnoty BNP 200 ng/l, při terapii došlo ke vzestupu na 225 ng/l. Je velmi důležité poznamenat, že hladina BNP ve většině stanovení nepřesáhla hodnotu 500 ng/l, která je rozhodujícím limitem pro diagnostiku srdečního selhání. Vlivem terapie dochází současně k poklesu hladiny NT-proBNP (vysvětlením je pravděpodobné snížení podnětů pro produkci proBNP, který je prekurzorem těchto peptidů, v důsledku úspěšné léčby).
Některá sdělení z letošního roku analyzovala tento efekt a jeho potenciální vliv na diagnostiku srdečního selhání a monitoraci efektivity terapie s využitím stanovení natriuretických peptidů. Přinesla zajímavé poznatky, mezi které jistě patří předpoklad, že sacubitril neovlivňuje pouze hladiny mozkového (BNP), ale také síňového (ANP) natriuretického peptidu, jehož zvýšená hladina má pozitivní vliv také na průběh srdečního selhání. Přičemž je již z dřívějška známo, že se neprilysin velmi významně podílí na biodegradaci také ANP a CNP, a z toho lze usuzovat, že se hlavní pozitivní změny působení sacubitrilu týkají nejenom BNP, ale přinejmenším stejně intenzivně (a možná více v důsledku větší afinity neprilysinu k ANP) i síňového natriuretického peptidu. S ohledem na zcela nový úhel pohledu na tuto oblast byly učiněny zatím předběžné závěry16:
- klinická interpretace výsledků stanovení NT-proBNP u pacientů se srdečním selháním není ovlivněna inhibicí neprilysinu,
- současná dostupná data ukazují, že u nemocných léčených sacubitrilem/valsartanem nebude možné využít koncept nižší hladiny BNP – lepší prognóza; pro stanovení NT-proBNP zůstává tento koncept v platnosti,
- je nutné dále studovat využití stanovení hladin obou analytů (BNP i NT-proBNP) jak ve studiích, tak i v klinické praxi.
Závěrem
Koncept augmentace/podpory pozitivních efektů natriuretických peptidů na kardiovaskulární systém dostává novou podobu ve formě terapie pacientů s chronickým srdečním selháním novou skupinou léků (ARNI). Prvním představitelem této skupiny je molekula sacubitrilu/valsartanu, která příznivě ovlivňuje degradaci natriuretických peptidů blokádou neprilysinu a současně ovlivňuje systém renin-angiotenzin-aldosteron blokádou receptorů pro angiotenzin. Na základě velmi příznivých dat z klinických studií byla tato terapie zahrnuta do algoritmu terapie pacientů s chronickým srdečním selháním se sníženou ejekční frakcí levé komory. V souvislosti s mechanismy účinku tohoto nového léku nabývá na významu otázka stanovení jednotlivých typů natriuretických peptidů a správná interpretace jejich výsledků.