Na Roche sympoziu v únoru 2018 byl prezentován nový koagulometr cobas t 511, který představuje novinku v používání a přípravě reagencií, neboť využívá kazetový systém a reagencie jsou rekonstituovány přímo v analyzátoru.
Koagulometr jsme měli možnost vyzkoušet v naší laboratoři v průběhu března a dubna, kdy jsme zařadili tento analyzátor do laboratorního provozu bez připojení na LIS.
Nároky na akreditaci laboratoří a současnou automatizaci práce vedou laboratoře ke zpřísnění podmínek pro zařazení nového koagulometru do rutinního provozu, to vše jsme se snažili zohlednit ve zkušebním režimu.
Prvním cílem bylo seznámit se s novým typem analyzátoru, který využívá jiný systém přípravy reagencií, než byl dosud v laboratoři používán. Druhým cílem bylo porovnat základní koagulační testy na novém koagulometru a všech analyzátorech v laboratoři a posoudit vhodnost analyzátoru k zařazení do běžného provozu.

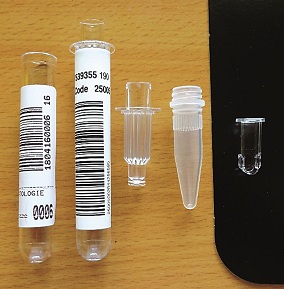
Jedná se o analyzátor, který je schopen analyzovat různé primární typy zkumavek v uzavřeném i otevřeném režimu, a to i v kombinaci v jednom stojánku (počet zkumavek v jednom stojánku je pět, maximální počet stojánků na palubě analyzátoru je 15). V případě mikrozkumavek je možné naprogramovat konkrétní stojánky, do nichž jsou tyto mikrozkumavky vkládány. Výhodou mikrozkumavek je velmi malý „mrtvý objem“ plazmy.

V analyzátoru je zabudován chladicí systém, v němž jsou uloženy kazety s reagenciemi. Z tohoto prostoru se na základě požadavku zadaného do systému přesune kazeta do horního pracovního prostoru, kde proběhne samotná rekonstituce reagencie v uzavřeném prostoru. Tento způsob přípravy reagencií představuje vyšší stupeň standardizace práce a eliminuje možné chyby v preanalytické fázi. V čárovém kódu kazety jsou pak uloženy všechny potřebné informace o reagencii (např. ISI tromboplastinu, čas normální plazmy, doba exspirace reagencie atd.). V programu „Routine – Reagent status“ pak následně můžeme všechny údaje o reagenční kazetě kontrolovat vč. počtu testů, které můžeme z daného objemu reagencie vyšetřit. Příbalové letáky k reagenciím jsou pravidelně aktualizovány on-line a všechny potřebné informace jsou uloženy v SW analyzátoru.

obr 6
Pro vlastní měření jsou k dispozici čtyři vlnové délky:
• 625 nm pro koagulační stanovení
• 408 nm pro chromogenní a koagulační stanovení
• 800 nm pro imunochemické stanovení
• 588 nm pro imunochemické stanovení a hodnocení HIL
Pro koagulační stanovení je velmi důležitá vlnová délka 625 nm, protože při ní dochází k minimu interferencí, které se mohou projevit při jiných vlnových délkách. Tuto skutečnost jsme ověřili ve dvou pokusech se silně hemolytickou a silně ikterickou plazmou.
Hemolytickou plazmu jsme připravili podle doporučeného postupu (Lippi et al.: Clin Chem Lab Med 2009; 47: 934–939) a z koncentrovaného hemolyzátu připravili 5 koncentrací za pomoci poolované plazmy jako ředicího média. Parametr H_I znamená hodnocení hemolýzy a ikterického zabarvení.
Z tabulky je patrné, že u měřených parametrů nebylo výrazné ovlivnění hemolýzou potvrzeno, i když se v případě vzorku se 100% hemolýzou jednalo o silný stupeň hemolýzy (H index – 16). Ani v grafickém znázornění výsledků stanovení antitrombinu (graf 1) ovlivnění patrné není, jedná se jen o rozdíl 3% aktivity antitrombinu, což je nižší rozdíl než povolená laboratorní chyba v případě opakovaného měření.
Měření ikterické plazmy jsme ověřovali podobným způsobem, ale příprava standardů nebyla možná přesně podle protokolu. Pomocí silně ikterické plazmy jsme připravili 3 koncentrace naředěním poolovanou plazmou (tab 2.).
Z tabulky je patrné, že u měřených parametrů výrazné ovlivnění ikterickou plazmou nebylo potvrzeno, i když v případě vzorku se značným ikterickým zabarvením (I index – 25) nebyl odečten derivovaný fibrinogen. Výsledky koagulačních parametrů u jednotlivých ředění odpovídají poměru zastoupení ikterické a poolované plazmy.
Velkou výhodou analyzátoru je vydání výsledků i v případě takto silně zabarvených vzorků, i když v těchto případech analyzátor neprovede automatickou validaci výsledku a na možnost interference upozorní.
Při dalším posuzování koagulometru jsme se věnovali vlastnímu měření základních koagulačních parametrů: protrombinový čas (PT) vyjádřený v sekundách a INR, aktivovaný parciální tromboplastinový čas (APTT), trombinový čas (TT), antitrombin (AT), fibrinogen (Fbg), D-dimery a aktivita anti-Xa. Byla měřena preciznost v sérii, mezilehlá preciznost a ev. ovlivnění analýz vkládáním vzorků s různou hladinou analytu. Výsledky byly zpracovány statisticky. Všechny uvedené parametry byly porovnány rovněž referenčním analyzátorem, kterým je BCS XP, Siemens.
Při posuzování koagulometru jsme se řídili navrženým testovacím protokolem firmy Roche a také doporučením laboratorní sekce České hematologické společnosti: http://www.hematology.cz/doporuceni/laboratorni_sekce/files/obecna/Doporuceni_LS_CHS_CLS-Zavedeni_noveho_analyzatoru_v01.pdf
Provedli jsme více než 2 000 analýz vzorků plazmy citrátové krve standardně odebrané, centrifugované, ev. zamražené aliquoty (stejné podmínky jako při běžné laboratorní praxi). Zároveň jsme prováděli měření kontrolního materiálu s definovaným rozmezím na jedné nebo více hladinách.
Metodika stanovení na referenčním analyzátoru: protrombinový čas vyjádřený v sekundách a INR, Thromborel S, APTT, Pathromtin SL, trombinový čas, Thromboclotin (5 NIH), Antitrombin, Berichrom AT, Siemens, SRN, Fibrinogen, Fibrinogen Technoclone, Rakousko, D-dimer, MediRox, Švédsko, aktivita antiXa, Biophen Heparin, Francie, analyzátor: BCS XP, Siemens, SRN.
Metodika stanovení na analyzátoru cobas t 511: protrombinový čas vyjádřený v sekundách a INR, PT Rec a PT Owren, APTT a APTT screen, trombinový čas, TT cobas t, Antitrombin, AT cobas t, Fibrinogen, Fibrinogen cobas t, D-dimer, D-DI2 cobas t, aktivita anti-Xa, anti-Xa cobas t, Roche, Švýcarsko.
Výsledky porovnání
Bylo provedeno 2 070 měření s využitím všech detekčních kanálů.
Preciznost v sérii:
Variační koeficient CV (%) se pohyboval v rozmezí 0,28–1,08 pro normální hladiny, 0,11–5,96 pro patologické hladiny. Jednotlivé statistické hodnoty pro jednotlivé parametry jsou znázorněny v tabulkách 3–6.
Graficky jsme znázornili preciznost v sérii pro každý jednotlivý kanál měření.
Mezilehlá preciznost:
Variační koeficient CV (%) se pohyboval v rozmezí 0,87–4,21 pro normální hladiny, 0,66–2,89 pro patologické hladiny. Pro stanovení mezilehlé preciznosti byl použit kontrolní materiál Roche.
Naměřená data preciznosti v sérii i mezilehlé preciznosti jsou v souladu s údaji uváděnými výrobcem i s požadavky na interní kontrolu kvality (IKK) a externí hodnocení kvality (EHK).
Závěr
Nízké hodnoty variačních koeficientů mezilehlé preciznosti i preciznosti v sérii ukazují na vhodnost zařazení nového analyzátoru do laboratorní praxe. Koagulometr cobas t 511 splňuje požadavky na kvalitní a přesné měření, které bylo porovnatelné s referenčním analyzátorem a které lze
z klinického hlediska plně akceptovat.
Obr. 1: Koagulometr cobas t 511 s příslušenstvím
Obr. 2: Typy stojánků pro kalibrátory (C), kontroly (Q) a vzorky (M, 0)
Obr. 3: Typy mikrozkumavek a měřicí kyveta
Obr. 4: Podavač stojánků s primárními zkumavkami
Obr. 5: Pracovní prostor s reagenčními kazetami
Obr. 6: Reagenční kazety v originálním balení
Tab. 1: Vliv hemolýzy na měření
Graf 1: Ovlivnění stanovení antitrombinu
Tab. 2: Vliv ikterického zabarvení na měření
Tab. 3: Hodnoty měření pro Level 1
Tab. 4: Hodnoty měření pro Level 2
Tab. 5: Hodnoty měření pro Level 3
Graf 2: Preciznost v sérii pro koagulační stanovení
Graf 3: Preciznost v sérii pro koagulační stanovení s ředěným vzorkem
Graf 4: Preciznost v sérii pro chromogenní stanovení
Graf 5: Preciznost v sérii pro imunologické stanovení
Tab. 6: Hodnoty měření kontrolního materiálu