Rozšíření nákazy SARS-CoV-2 a postupné vyhlášení epidemie a nouzového stavu představovalo zcela nový druh výzvy pro celý zdravotnický systém v ČR a jednotlivá zdravotnická zařízení. Ústřední vojenská nemocnice – Vojenská fakultní nemocnice Praha (dále jen ÚVN) ihned po vyhlášení nouzového stavu dne 12. března 2020 se již v sobotu 13. března 2020 zřízením odběrového místa aktivně zapojila do systému testování a screeningu infekce SARS-CoV-2. Nafukovací stan postavený v areálu ÚVN pro odběry nazofaryngeálních stěrů se tak stal jedním z prvních podobných testovacích míst v ČR.1
Odebrané vzorky byly zpočátku zasílány k laboratornímu vyšetření do externích laboratoří, proto byly zanedlouho po otevření prvního odběrového místa podniknuty nezbytné kroky, aby mohla být zahájena laboratorní vyšetření vzorků v ÚVN co nejdříve. Aktivitu v tomto směru vyvinulo Oddělení hematologie a krevní transfuze (dále jen OHKT), které má několikaletou zkušenost s velkoobjemovým automatizovaným vyšetřováním dárců krve a jejích složek metodou přímé detekce nukleové kyseliny, a volba padla na vysoce kapacitní systém fy Roche cobas® 6800 s právě na evropský trh uvedeným testem RT PCR SARS-CoV-2. Po nutných drobných stavebních úpravách a instalaci v rekordním čase laboratoř na vyšetřování RT PCR SARS-CoV-2 na OHKT zahájila provoz 3. dubna 2020. V té době se jednalo o nejvýkonnější laboratoř na testování RT PCR SARS-CoV-2 v ČR s možnou kapacitou až 1 000 provedených testů za 24 hodin.1
Kit cobas® SARS-CoV-2 je kvalitativní test pro použití v systému cobas® 6800 a systému cobas® 8800 pro detekci RNA nového koronaviru z roku 2019 (SARS-CoV-2) v individuálních nebo poolovaných vzorcích nazálních, nazofaryngeálních a orofaryngeálních výtěrů odebraných v médiu Copan Universal Transport Medium System (UTM-RT), médiu BD™ Universal Viral Transport System (UVT), médiu cobas® PCR Media nebo v 0,9% fyziologickém roztoku. Při zpracování se do každého vzorku přidává RNA interní kontrola, která se používá pro monitorování celé přípravy vzorku a procesu amplifikace při PCR. Test navíc využívá externí kontroly (pozitivní kontrolu s nízkým titrem a negativní kontrolu).2
Běžnou a většinovou praxí jsou odběry individuálních vzorků z nazofaryngeálního výtěru, u nově definovaných preventivních vyšetření jsme od června 2021 zavedli poolování s použitím rozpipetovávacího automatu Microlab® HAMILTON STAR IVD v systému cobas® Synergy SOFTWARE v poolu 6.
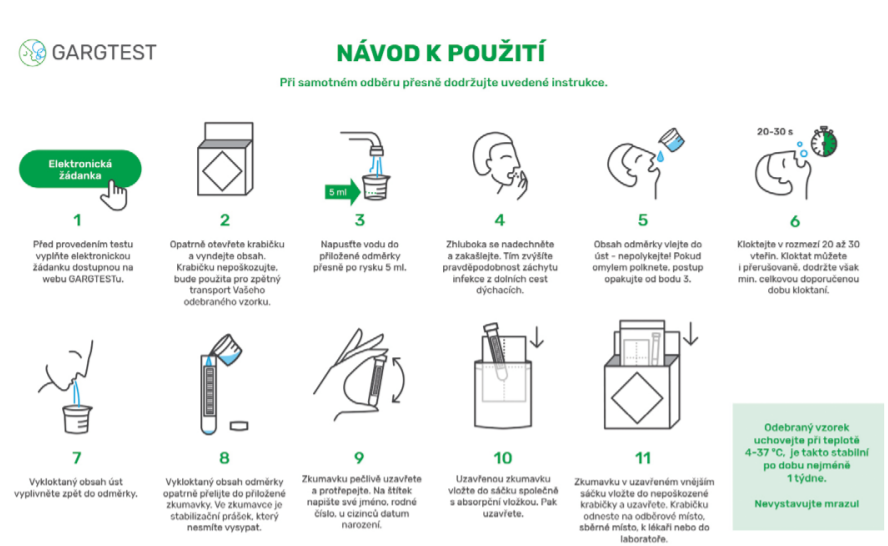
V souvislosti s diskusí o širším zavedení PCR testování ve školách jsme hledali vhodnou odběrovou soupravu na odběry slin, abychom tuto možnost mohli případně nabídnout potenciálním zákazníkům. Možnou soupravou pro otestování byla zvolena samoodběrová sada GARGTEST na principu kloktání dutiny ústní a hltanu, výrobce IntellMed, s.r.o., Olomouc. Sada je určena k odběru vzorků, které se vyhodnocují na přítomnost virů infikujících dutinu ústní a horní cesty dýchací ve zdravotnické laboratoři metodou přímého průkazu nukleové kyseliny. Virus v transportním médiu zůstává vitální a lze ho použít i pro kultivační vyšetření. Odebraný vzorek je stabilizován speciálním pufrem, není třeba jej uchovávat a převážet do laboratoří při snížené teplotě. V roztoku virus zůstává dlouhodobě stabilní v širokém rozpětí teplot (4–37 °C) po dobu nejméně 1 týdne.
Jako srovnávací test byl použit rutinně zavedený odběrový set COROTEST VTM (výrobce LabMediaServis s.r.o., Hradec Králové) pro nazofaryngeální odběr vzorku. Jedná se o polypropylenovou zkumavku s transportním médiem s 2 odběrovými tyčinkami. Médium obsahuje BSF: bovinní fetální sérum, guanidin thiokyanát, ATB potlačující růst mikroflóry, PBS pufr (pH = 7,3/25 °C).
Předmět, cíl a metoda validace
Cílem validace bylo provést ověření a potvrzení funkčnosti metody SARS-CoV-2 kitem cobas® SARS-CoV-2 (Roche, Rotkreuz, Švýcarsko) s následnou evaluací samoodběrové sady GARGTEST v rámci komparace s nazofaryngeálním odběrem do transportního média. Nedílnou součástí validace bylo provedení analytické návaznosti na testování externích kontrol kvality INSTAND EQAS Düsseldorf a externích kontrol AccuPLex SARS-CoV-2 (SeraCare).
Výpočty byly prováděny statistickým softwarem Statistica® společnosti StatSoft/DELL (verze 12 – Oklahoma, USA), určeným k biostatistickým a lékařským výpočtům klinických studií.
Rozsah validace
Specifita
Specifita, tj. těsnost souladu mezi jedním výsledkem měření a dohodnutou referenční hodnotou daného parametru. Očekávaný výsledek je 10 negativních vzorků pro daný kvalitativní parametr a minimálně 5 reaktivních vzorků (reaktivní výsledek u vzorků obsahující RNA daného viru).
Detekční limit
Detekční limit, tj. nejnižší spolehlivě detekovatelné množství nukleové kyseliny (NK) ve vzorku, která nemusí být stanovena kvantitativně. Jasné a spolehlivé stanovení NK od matrix vzorku (LoD, limit of detection) analytického postupu je dáno nejmenším množstvím analytu ve vzorku, které může být detekováno, ale které nemusí být stanovitelné jako exaktní hodnota. Očekávaný výsledek a kritérium přijatelnosti je detekce ve 100 % všech spuštěných běhů.
Robustnost
Robustnost, tj. míra schopnosti metody stanovit správné a přesné výsledky při malých změnách pracovních podmínek, ke kterým dochází při rutinní analýze, ale s dodržením pracovního postupu. Očekávaný výsledek a kritérium přijatelnosti je pozitivita všech spike vzorků.
Vyhodnocení validace
V rámci validace bylo odebráno celkem 310 synchronních odběrů (samoodběr vs. nazofaryngeální stěr), z toho 279 bylo zařazeno do studie z důvodu velkého množství neshod (viz dále).
Všechny vzorky byly testovány IDT, následně nazofaryngeální stěr také primárním poolem 6 (viz tab. 1).
Vyhodnocení preanalytické fáze
Při příjmu materiálu odebraného do soupravy GARGTEST bylo zjištěno množství neshod (celkem 31):
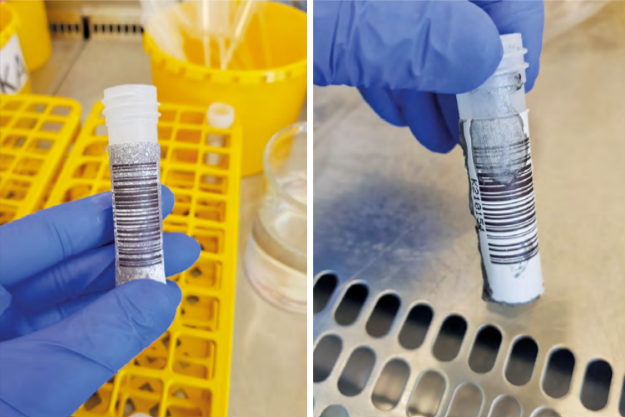
1) poškození ID barcodu (poškození vodou – postříkání po vyplivnutí nebo nalévání vody do připraveného kalíšku) – při možném budoucím používání je nutné volit laserový lesklý štítek.
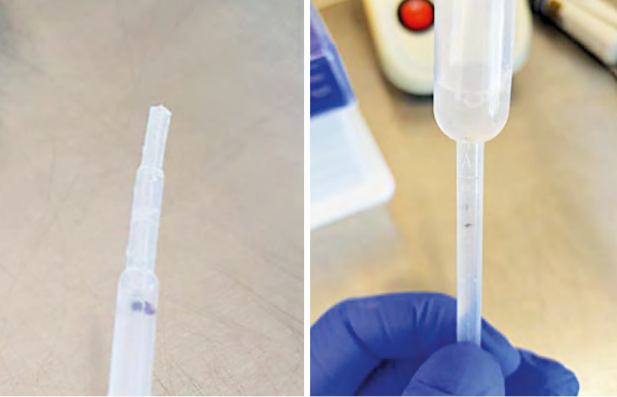
2) četné precipitáty a zbytky jídla uvnitř vlastního vzorku. Ani po ředění a lyzaci nebylo možné některé vzorky změřit – při vlastním měření byla v SW cobas® 6800 informace o přítomnosti sraženiny (clotu) nebo poruchy aspirace při pipetování vzorku.
Vyhodnocení kvalitativní metody SARS-CoV-2
Specifita
Použité vzorky byly testované jako negativní a pozitivní (viz tab. 2–7).
Závěr vyhodnocení specifity
Test cobas® SARS-CoV-2 má 100% specifitu v samoodběrové sadě GARGTEST a skutečně stanovuje negativní výsledek v externích kontrolách AccuPlex.
Výsledek byl pozitivní pouze u 3 vzorků, 276 vzorků bylo negativních. Byla provedena komparace mezi nazofaryngeální odběrovou soupravou COROTEST VTM, kdy všechny vzorky byly změřeny jak v primárním poolu 6, tak i jako IDT. Veškeré pooly a IDT byly negativní. Odchylka v negativitě oproti GARGTESTům může být způsobena např. chybně provedeným nazofaryngeálním stěrem apod.
Specifita je pro COROTEST o 1,075% nižší než u GARGTESTu. Výrobce testu cobas® SARS-CoV-2 fa Roche v příbalovém letáku uvádí specifitu testu v poolu 6 100% (95% CI: 83,9–100 %), konfidenční interval tak odpovídá našemu zjištění specifity 98,9%.
Vzhledem k malému počtu pozitivních vzorků a všech negativních vzorků v COROTESTu nelze provést statistickou analýzu specifity při porovnání těchto dvou odběrových souprav a vyhodnocení specifity není možné uzavřít.
Detekční limit a analytická senzitivita
Použité vzorky a metodika
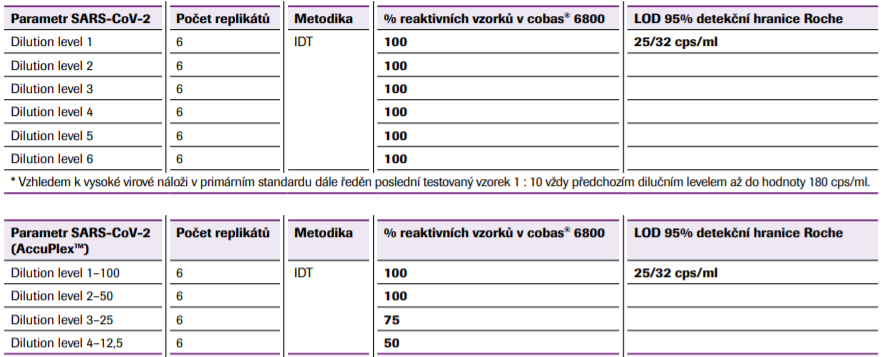
Byla použita 1 nezávislá série ředění pozitivních vzorků (STD SZÚ), které byly testovány ve dvou odlišných dnech; celkem změřeno 12 výsledků pro ředicí řadu následujícím způsobem: 6 replikátů pro každé ředění – 2 dny – 1 ředicí řada. Dále byl použit Accuplex™ SARS-CoV-2 SeraCare, který byl také použit pro vývoj kitu Roche, kdy byla do vzorku vody přidána kontrola v poměru 1: 10 (viz tab. 8–9).
Závěr vyhodnocení detekčního limitu a analytické senzitivity
U parametru SARS-CoV-2 bylo provedeno ředění vzorků dle postupu v příbalovém letáku. Z těchto naředěných vzorků byly vytvořeny ředicí řady, kdy se každé ředění testovalo v 6 replikátech.
Všechny ředicí řady v jednotlivých měřeních byly vyhodnoceny procentuálně. Po vyhodnocení výsledků jednotlivých výsledků ředicích řad je možné konstatovat, že lze spolehlivě detekovat přítomnost nukleové kyseliny viru kitem cobas® SARS-CoV-2.
Pro stanovení nejnižších detekovatelných dávek (LOD) byly použity referenční panely z externí firmy SeraCare se 100% detekcí do 50 cps/ml, standard SZÚ. Vyhodnocení bylo provedeno dle mezinárodních standardů: jako nejnižší detekovatelná hladina/senzitivita použita hladina viru, kde je detekováno 100 % reaktivit ve všech bězích s použitím 6 replikátů. V našem případě tedy jde o hladinu 50 cps/ml (AccuPlex™).
Lze předpokládat, že další ředění by ukázalo pozitivitu i v dalším násobném ředění, což ukazují hladiny specifity, viz výše. Kvůli nedostatku materiálu ale nebylo možné tento předpoklad ověřit.
Robustnost
Bylo použito 5 náhodně vybraných negativních vzorků k vytvoření „spike sample“ s přibližným 3násobkem 95% LOD, tj. 150 cps/ml. Všechny vzorky v běhu byly reaktivní.
Závěr vyhodnocení robustnosti
Test cobas® SARS-CoV-2 je vysoce robustní, ve všech námi testovaných vzorcích byla zjištěna reaktivita v obou cílech (ORF1ab, E-gen).







Závěr
Při vyhodnocení preanalytické fáze lze konstatovat, že odběry vzorků na vyšetření PCR SARS-CoV-2 pomocí odběrové soupravy GARGTEST nepředstavují optimální způsob provedení odběru biologického materiálu pro PCR vyšetření, obzvláště v automatizovaném systému (poškozené štítky s ID barcody, precipitáty a zbytky potravy), což je z velké části dáno laickým samoodběrem, který prakticky vylučuje jakoukoli standardizaci vzorku. Část odebraných vzorků nelze použít pro vlastní analytickou fázi vyšetření, což následně znehodnocuje celý případný screeningový proces.
Ve validační studii byla prokázána vyšší specifita PCR testu cobas® SARS-CoV-2 (Roche) ve vzorcích odebraných soupravou GARGTEST (o 1,075% více než u vzorků odebraných běžným nazofaryngeálním stěrem soupravou COROTEST). Bohužel toto konstatování je obecné, neboť nelze vyslovit spolehlivý závěr s pouze třemi pozitivními vzorky.
Vzhledem k tomuto nízkému počtu pozitivních vzorků v GARGTESTu a všem negativním vzorkům v COROTESTu nelze provést statistickou analýzu specifity při porovnání těchto dvou odběrových souprav.
Vzorky odebrané soupravou GARGTEST i COROTEST, které byly způsobilé pro analytickou fázi vyšetření, splňují podmínky pro dosažení detekčního limitu, analytické senzitivity a robustnosti a pro detekci přítomnosti nukleové kyseliny viru SARS-CoV-2 kitem cobas® SARS-CoV-2 jsou spolehlivé, nicméně by bylo vhodné provést validační studii s větším množstvím pozitivních vzorků.
