Motto pro následování SQC: „Fideliter et semper“
Statistická kontrola kvality (SQC) představuje statistický proces používaný k monitorování a hodnocení kvality analytického procesu, v němž se vytvářejí výsledky pacientů a jehož cílem je účinný záchyt podmínek stavů mimo kontrolu, zaměřený na omezení rizik pro pacienty na přijatelnou úroveň potřebnou pro správné lékařské rozhodování. Ve zdravotnických laboratořích má za sebou téměř 70letou cestu vývoje. Počátky dnešní laboratorní kontroly kvality totiž spadají do 50. let 20. století, ale už ve 30. letech minulého století započala historie statistické regulace a kontroly kvality procesů (SPC), která se v následujících letech postupně zaváděla a stávala běžnou součástí řízení kvality.
Stručná historie QC v laboratořích
SQC vznikla jako bezprostřední důsledek automatizované výroby a poprvé se objevila a stala součástí statistiky ve Spojeném království a ve Spojených státech, kde drasticky snížila náklady na kontrolu kvality (QC), protože zavedla koncept vzorkování. Za průkopníka dnešních plánů absolutního řízení kvality (TQCP) je považován Walter Andrew Shewhart, který 16. května 1924 prezentoval jednoduchý kontrolní graf. Primárním účelem tohoto grafu bylo zabránit výrobě vadných produktů ve společnosti Bell Telephone za předpokladu, že variabilita v důsledku náhodných, nesystémových příčin je nevyhnutelná. Shewhart navrhl speciální statistické techniky a specifické (kontrolní) diagramy jako nástroj QC a poté v laboratořích Bell Telephone vyvíjel různé koncepty statistické kontroly kvality. Shewhartův graf představuje prototyp dnešních regulačních diagramů (RD) a ty pak základ všech konceptů kontroly kvality výrobních procesů.
Regulační průběhové diagramy

Regulační průběhové diagramy aktuálně používané ve zdravotnických laboratořích jsou však úzce spojené se jmény dvou amerických chemiků, kteří v roce 1950 modifikovali Shewhartův graf a vytvořili tím diagram vhodný pro chemické analýzy běžné v lékařských laboratořích. Jmenovali se Stanley Levey a Elmer Jennings a po nich nazvané L-J grafy se liší od původního Shewhartova mj. způsobem odhadu směrodatné odchylky (SD). Shewhartův graf totiž využívá tzv. krátkodobý odhad SD (odvozený od tzv. racionální podskupiny), zatímco Levey-Jenningsovy grafy pracují s tzv. dlouhodobými odhady (výběrovými) SD. Mimochodem, před zavedením těchto
grafů do praxe se dobrá přesnost měření v mnoha laboratořích zajištovala jen měřením v duplikátu.
Regulační diagram zůstal dodnes pevným základem a nástrojem SPC a používá se ke znázornění změn procesu, resp. jeho klíčových metrik v průběhu času. Má vždy označenu střední hodnotu (CL – Central Line) a horní a dolní regulační mez (UCL – Upper Control Line; LCL – Lower Control Line), a často také tzv. akční meze, které jsou určeny buď z historických dat, nebo mají cílové hodnoty určené závazným předpisem. Z časového průběhu diagramu je možné činit závěr, zda je chování procesu či dané metriky regulované. I ve zdravotnických laboratořích se RD dodnes používají ke zjištění, jestli proces funguje jako stabilní systém s náhodnými vlivy působícími v malém rozsahu (zda je proces ve stavu „statisticky pod kontrolou“), či zda případně nedochází ke zlepšení nebo zhoršení tohoto stavu, a také ke sledování trendů, iterací a cyklů chování systému, tj. za účelem monitorování, zda systém vyhovuje stanoveným požadavkům.
Cíle SQC
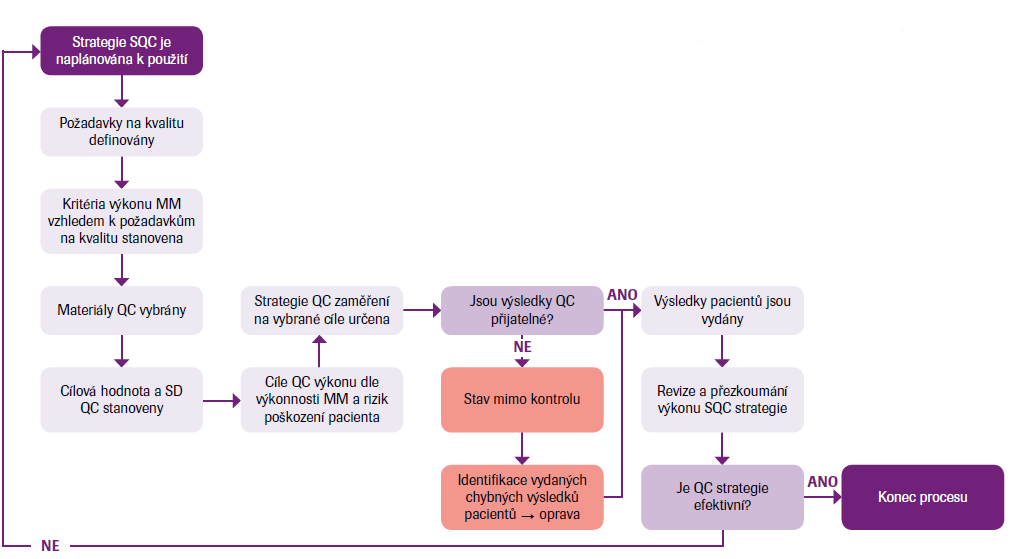
V SQC hraje ústřední roli její účinné plánování a stanovení cílů a jde především o detekci všech chybných výsledků, které svou hodnotou přesáhly nějakou přijatelnou mez (např. přijatelnou analytickou chybu TEa). K výkonu SQC, který by měl být předem stanoven, je zapotřebí:
- zvolit vhodný počet kontrolních vzorků a druh QC pravidel
- znát, resp. stanovit odhad pravděpodobnosti (P), že konkrétní výsledek za stavu měřicí metody „mimo kontrolu“ mine stanovený cíl (např. přijatelnou hodnotu celkové chyby, > TEa)
Klasické metriky výkonu SQC dle doporučení CLSI C241
- P falešných zamítnutí (chyba I. typu, chyba „skepse“; daná rozměrem testu α)
- P detekce chyb (chyba II. typu, chyba „důvěry“; daná silou testu 1-β)
- Nové současné doplňkové metriky:
a. σ-metrika (Six Sigma) převzatá z řízení rizik (ISO 14791, EP23): (x) = (TEa(x) – |Bias(x)| )/ SD(x)
b. Předpokládaný počet výsledků pacientů (PPVP) postižených stavem mimo kontrolu před tím, než je stav mimo kontrolu zjištěn, v metrikách MaxE(Nuc/Nuf):
i. MaxE(Nuc): PPVP, které byly jako chybné zachycené (> TEa)
ii. MaxE(Nuf): PPVP, které byly jako chybné vydané a mohou vytvářet nebezpečné situace
Současné způsoby zjišťování PPVP odpovídají šesté generaci SQC (viz níže) a příslušné softwarové aplikace obsahují simulační programy založené na matematickém
modelování a výpočtech P.
Stručný pohled na současnou terminologii2
Terminologie používaná v rámci SCQ vychází z Mezinárodního metrologického slovníku (VIM), a sice z jeho aktuálního 3. vydání (TNI 01 0115), v němž jsou definovány
mj. tři důležité pojmy:
- Přesnost jako těsnost shody mezi naměřenou hodnotou veličiny a pravou hodnotou veličiny měřené veličiny ~ (přesnost je vlastnost, která platí pro jednu naměřenou hodnotu)
- Preciznost jako těsnost shody mezi indikacemi nebo naměřenými hodnotami veličiny získanými opakovanými měřeními na stejném objektu nebo podobných objektech za specifických podmínek (SD, σ, CV) ~ (preciznost je vlastnost opakovaných měření) Podmnožiny preciznosti jsou míry odhadu náhodných chyb za různě definovaných podmínek: opakovatelnost (O), mezilehlá preciznost (MP) a reprodukovatelnost (R)
- Pravdivost jako těsnost shody mezi aritmetickým průměrem nekonečného počtu opakovaných naměřených hodnot veličiny a referenční hodnotou veličiny (x∾ –TV) ~ (pravdivost je vlastnost opakovaných měření)
Bias (B) představuje míru odhadu systémové chyby (a odtud i pravdivosti) a je to rozdíl mezi střední hodnotou výsledků opakovaných měření a skutečnou hodnotou (kterou obvykle neznáme). Odhad strannosti B, která vždy významně zhoršuje srovnatelnost výsledků měřené veličiny daného typu a tím deformuje vztahy mezi různými typy měřených veličin, je bez vhodného materiálu velmi obtížný! Protože cílem SQC je především zajistit srovnatelnost výsledků, je také zapotřebí trvale odstraňovat B, což s ohledem na aktuální stav standardizace/harmonizace měření různých měřených veličin odpovídajících jednotlivým analytům znamená, že se tyto analyty dělí na:
- dobře definované (chemické entity, jejichž hodnoty jsou vydávány v SI jednotkách)
- nedobře definované (např. různě složité proteinové molekuly, konvenční jednotky)
- esoterické (vydávané v UI či arbitrárních jednotkách)
Specifikace analytických cílů
V roce 1967 započala diskuse o cílech kvality (tzv. specifikacích kvality, resp. tolerančních mezích). Podnětem k této diskusi bylo použití standardu na zlepšování standardů kvality CLIA (Clinical Laboratory Improvement Act). Tato norma je použitelná pro všechny typy zdravotnických laboratoří a stanovuje specifická pravidla kvality. Biologické rozdíly, analytické cíle a limity lékařských rozhodnutí byly navrženy jako cíle kvality nejen v USA, ale i v Evropě. Na konferenci v Aspenu v roce 1977 bylo přijato, že analytická variabilita měřicí metody by měla být udržována pod polovinou intraindividuální variability, aby její velikost přidaná k celkové variabilitě činila maximálně cca 10–12 %. E. M. S. Gowans 1988 přidal ke kritériu zohledňujícímu preciznost i kritérium přijatelnosti B. Je-li B limitován ¼ odmocniny součtu mocnin inter- a intraindividuální variability, pak jen malé procento výsledků padne falešně mimo meze referenčního intervalu dané populace. Skotskému klinickému biochemikovi Callumu Fraserovi a španělské lékárnici a klinické biochemičce v jedné osobě Carmen Ricósové se podařila teoretická i praktická aplikace biologických variabilit coby analytických cílů v klinické biochemii.
Cíle SQC aneb „Ať to máme pod kontrolou…“
Motto: Bez jasně daných cílů nelze hodnotit ani výkon SQC a ani nejlepší model nemusí nezbytně představovat model nejužitečnější! Univerzální cíl pro SQC neexistuje! Lze pouze určit P, že chyba konkrétního výsledku přesahující přijatelnou mez (např. > TEa) by měla být natolik nízká, aby zajistila klinicky požadovanou výkonnost metody měření! Proto byly stanoveny tři klíčové modely stanovení cílů SQC, resp. přijatelných mezí (TEa)1:
- Model 1 zohledňuje vliv analytické výkonnosti dané metody měření (dále jen MM) na možný klinický dopad
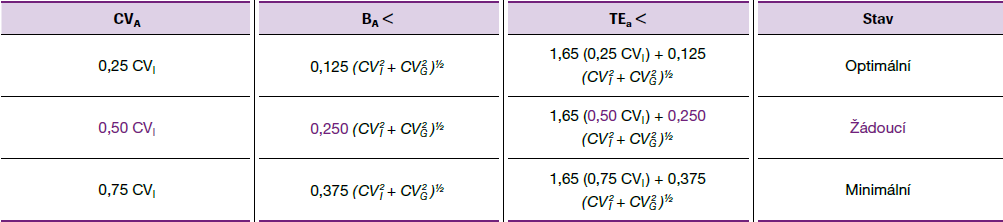
- Model 2 zohledňuje vztah přirozené variability měřené veličiny k analytické chybě (viz též tab. č. 1)
- Model 3 zohledňuje nejlepší výkon dané metody měření za stavu současných technologií (QC/PT/EQC)
Hlavním cílem SQC trvale zůstává co nejmenší chyba každého jednotlivého výsledku (= co největší přesnost každého jednotlivého výsledku) a tím i co nejmenší riziko poškození pacienta! Kvalitu výsledku pacienta tedy ovlivňuje přesnost jedinečného výsledku, což je rozdíl mezi hodnotou správnou a laboratoří vydanou. Zohlední-li se při vývoji strategie QC management rizik, měly by se zvažovat tři druhy selhání vedoucích k vadným výsledkům vyšetření pacienta (dle ISO 14791, EP23):
- PRAVDĚPODOBNOST výskytu chyb (tj. jaká je pravděpodobnost, že se chyby objeví)
- ZÁVAŽNOST chyb při jejím výskytu (tj. jak závažné může být potenciální poškození pacienta při výskytu chyb)
- ZÁCHYTNOST chyb (tj. jak spolehlivě je konkrétní QC strategie schopná odhalit chybu při jejich výskytu)
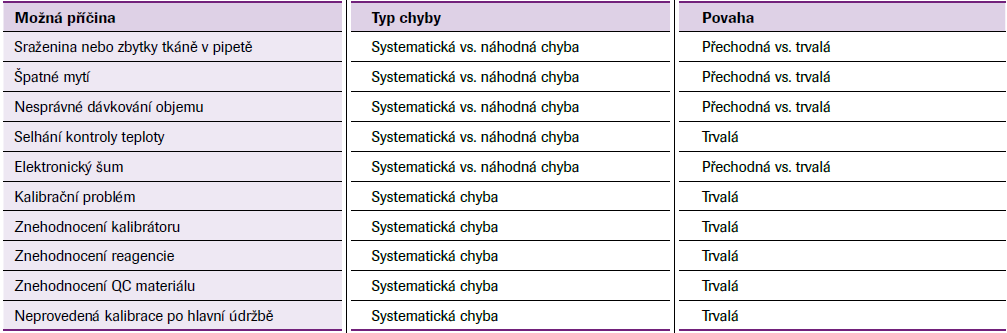
Příklady podmínek stavů mimo kontrolu v laboratoři dle CLSI C241
Pojem celkové analytické chyby a nejistoty měření
Motto: „Lékařství je věda nejistoty a umění pravděpodobnosti“ (W. Osler), to znamená, že nejistota měření (MU) typicky odráží nedostatek přesných znalostí o hodnotě měřené veličiny. Vysvětlení pojmů viz obrázky č. 2 a 3. Celková chyba (TE, TAE) je kombinací B a preciznosti a vlastností jedinečného výsledku měření ve vztahu ke skutečné hodnotě. Měření je prohlášeno za přesnější, nabízí-li menší chybu měření.
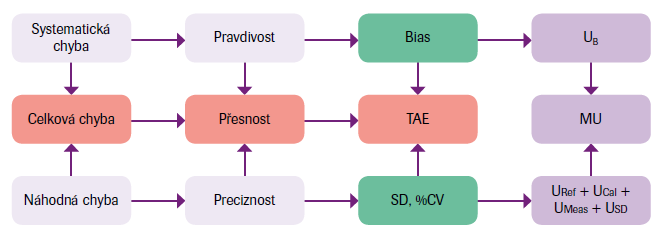
Legenda k obr. 2: Mírou přesnosti v přítomnosti bias B je celková analytická chyba (TAE), v nepřítomnosti B je to nejistota měření (MU), v níž je nejistota odhadu B (UB) zahrnuta společně s ostatními složkami nejistoty. MU lze určit součtem všech složek nejistoty odhadem shora dolů nebo zdola nahoru. Cihlově červená políčka ve schématu odpovídají vlastnostem jedinečných měření, zelená jsou vlastnosti opakovaných měření.
Klíčové položky strategie SQC v praktickém kontextu1
- Volba vhodných QC materiálů pro SQC
- Cílové hodnoty (x) QC stanovené tak, aby QC reagovaly velmi citlivě na posuny a trendy
- Postupy stanovení SD vhodné pro efektivní nastavení regulačních diagramů
- Výběr vhodných vylučovacích pravidel
pro IQC; ad 1., 2., 3. a 4. viz níže POZOR! Strategie SQC není totéž co postupy verifikace metod měření!
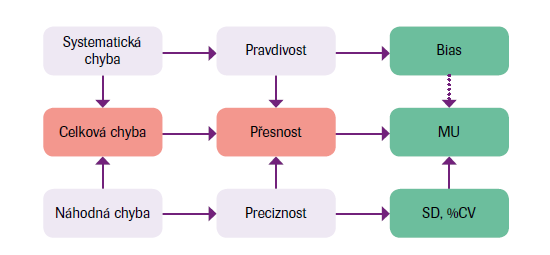
Legenda k obr. 3: Tečkovaná spojnice ve schématu od B k MU indikuje, že může-li být vychýlení (B) odhadováno, mělo by být eliminováno! MU je prezentována jako míra přesnosti za podmínek, kdy B bylo odstraněno nebo korigováno, či může být zanedbáno! Cihlově červená políčka ve schématu odpovídají vlastnostem jedinečných měření, zelená jsou vlastnosti opakovaných měření.
Ad 1. Kontrolní materiály se dle C241 dělí na:
- Vyrobené výrobcem metody měření – jsou-li optimalizované pro specifický systém a napodobují-li kalibrátor, nemusí být schopné odhalit některé specifické typy chyb
- Vyrobené 3. stranou pro výrobce metody měření – mají-li vzorec podobný kalibrátoru hlavního výrobce, nemusejí efektivně odhalit některé změny výkonu systému
- Vyrobené 3. stranou bez návaznosti na výrobce metody měření nebo výrobce kalibrátoru užívaného v dané metodě měření – lze typicky použít pro různé systémy měření, jsou tudíž považovány za nejvhodnější nejen pro interní kontrolu kvality
- Poolované vzorky pacientů nebo jiné laboratorní materiály – přijatelná volba pro některé typy analytů, ovšem poolování a suplementace mohou porušit
matrici materiálu
Materiály určené ke QC by se měly lišit od materiálů kalibračních, aby se zajistilo, že výsledky QC poskytují nezávislý odhad výkonnosti metody měření v její komplexnosti, včetně postupu kalibrace. Je-li nezbytné použít kalibrátory užité jako kontrolní materiály, je třeba, aby šarže kalibrátoru byla jiná než šarže kalibrátoru použitého jako QC. U většiny postupů měření jsou jako minimum doporučeny alespoň dvě koncentrace QC materiálů. K adekvátnímu monitorování výkonnosti postupu měření a umožnění aplikace QC pravidel, která zlepšují detekci a interpretaci potenciálních chyb měření (např. proporcionální nebo konstantní, náhodná versus systematická), je často nezbytné použít víc různých koncentračních hladin QC vzorků.
Ad 2. Cílové pravdivé hodnoty (TV) QC jako statistický parametr polohy
Iniciální pravdivá hodnota (TV) se určuje pomocí minimálně 10 měření v separátních dnech a odtud pak odhad x přezkoumané TV zahrnuje více kalibrací
a změny šarží reagencií (CLSI EP 26)
Ad 3. Úloha SD v RD a v efektivní strategii SQC = volba vhodných SD (statistický parametr variabilit) a je nutno rozlišovat:
- SD vhodné k verifikaci metody měření (údaje z příbalových letáků PL) odpovídají SD krátkodobé výkonnosti metody (dle CLSI EP 15 A3)
- SD vhodné k efektivní strategii SQC a k hodnocení dlouhodobé výkonnosti metody měření (σ-metrikou) reprezentující stabilní dlouhodobou výkonnost metody a jsou zde rozlišeny dva druhy nastavení SD:
a. počáteční
b. dodatečné (revize)
Standardní postup iniciálního odhadu preciznosti formou stanovení SD (CV) představuje minimálně 20 dní měření, stejné šarže reagencií a účast stejného operátora a zároveň existuje závislost vhodnosti odhadu SD na frekvenci kalibrací MM (viz níže)!
SD založené na měřeních po dobu kratší než jeden měsíc jsou obvykle méně klinicky relevantní a lze u nich předpokládat, že podhodnocují SD reprezentující dlouhodobou stabilní výkonnost metody měření, klíčovou pro nastavení SQC a validnost odhadu sigma metriky. Doba potřebná k dosažení spolehlivé reprezentace
všech zdrojů variability do SD však vždy závisí na konkrétní metodě měření. Např. je-li metoda kalibrovaná v každé sérii, pak studie SD prováděná po dobu 20 dní (takzvaná validační MP dle CLSI EP 05) může spolehlivě reprezentovat sledované zdroje kalibrační variability, neboť jsou při takové frekvenci kalibrací zkoumány dostatečně často. Nicméně nezřídka vedou 20denní studie SD určené pro efektivní strategii SQC k jejímu podhodnocení, a proto by měly představovat minimální, spodní mez přípustných SD.
Na druhé straně u metod měření, které se kalibrují 1x za týden, může trvat i více než čtyři měsíce, než je dosaženo srovnatelně spolehlivých odhadů kalibrační variability. Podobně je tomu s ostatními příspěvky jiných cyklických příležitostných zdrojů variability, které mohou významně přispívat k dlouhodobé stabilní výkonnosti metody měření, kde je také obvykle zapotřebí několikaměsíční studie SD pro zajištění jejich adekvátní reprezentace.
Odhady vnitřní laboratorní preciznosti poskytované v příbalových letácích výrobců nebo nezávislé literatuře se obecně vztahují v nejlepším případě ke spodním mezím SD potřebných pro efektivní strategii QC nebo pro vyhodnocení výkonnosti metody měření sigma metrikou, což je část informací potřebných pro SQC. Námitky se týkají faktu, jak přiblížit relevantní SD v krátké době zavádění nové metody měření a jak reagovat na výstrahy pravidel QC, když odhady SD nedosahují adekvátní
spolehlivosti.
Dobrá rada na okraj: Laboratoř by pro své cíle stanovené v SQC měla vždy získat dostatek homogenního, stabilního kontrolního materiálu (tj. nejlépe stejné šarže s exspirací minimálně jeden rok a více) a zároveň „lahvičková“ variabilita vhodně zvoleného kontrolního materiálu by měla být mnohem menší než variabilita zjištěná v postupu měření, který je monitorován. QC materiály by v každém případě měly mít pro daný analyt prokázanou stabilitu po dobu své deklarované trvanlivosti a během deklarovaného intervalu po otevření lahvičky!
8 doporučení C. A. Parvina
- Na konci série vyšetření pacientů zařadit vždy analýzu vzorků QC
- Znát počet pacientů mezi každým vyhodnocením QC pro možnost odhadu metrik jako MaxE(Nuc/Nuf)
- Čas mezi vyhodnocením QC by měl být mnohem kratší než čas potřebný ke korekci chybných výsledků, které již byly vydány
- Provést odhad závažnosti stavu mimo kontrolu před tím, než je odstraněn
- Odhadnout spolehlivost metody měření (např. σ-metrikou, resp. pomocí postupů z řízení rizik)
- Rozdělit analyty na ty, které mají vysokou (> 6) nebo naopak nízkou (< 3) σ-metriku, odtud pak odvodit správně dimenzovanou SQC volbou cílů, grafů, W-m-pravidel
- Přidat QC tam, kde je vysoká P vydání vadných výsledků
- Přidat QC tam, kde vydání jednoho vadného výsledku může zavinit závažné poškození pacienta
Volba W-m-pravidel dle hodnot σ-metriky
V následujících třech bodech je stručně vyjádřen způsob volby vhodné kombinace W-m-pravidel dle odhadu σ-metriky dané metody měření. Je-li σ-metrika méně nebo rovno po řadě 3, 4, 5, použije se následující doporučená kombinace W-m-p:
- 3 σ → 13s/2 ze 32s/R4s /31s/6x nebo 13s/22s/R4s /41s/8x
- 4 σ → 13s/22s/R4s /41s nebo 12,5s
- 5 σ → 13s nebo 12,5s nebo 13s/22s/R4s
σ-metrika jako nástroj srovnání analytických systémů
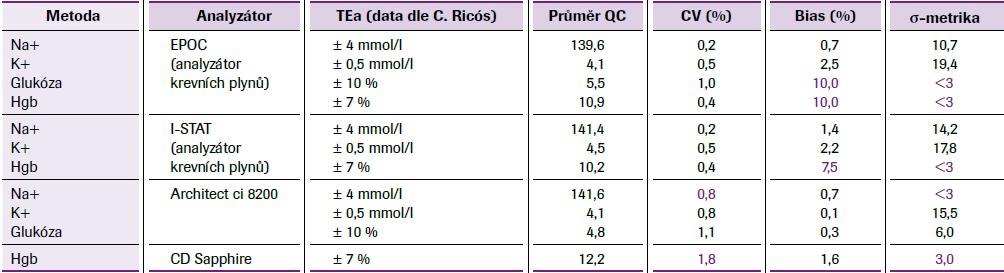
Technologický pokrok a vývoj SQC4
Šest generací statistické kontroly kvality představuje v kostce sedmdesátiletý vývoj tohoto oboru, který ovlivnil technologický pokrok směřující ke zvyšování efektivity a výkonnosti kontroly kvality, v němž sehrálo roli mnoho významných osobností, nicméně právě objev kontrolních multipravidel J. O. Westgardem potvrdil jeho nespornou roli otce laboratorní QC při výuce následovníků. Stal se nejslavnějším výzkumníkem v oblasti QC automatizovaných analyzátorů. Pracoval hlavně na počítačových simulacích, rozhodovacím limitu CUSUM grafu, výkonnostních funkcích, rozhodovacích multipravidlech pro kvalitu v Levey-Jenningsových grafech, které dodnes nesou jeho jméno, na specifikaci grafů operačních procesů, na validaci metod a teorii Six Sigma. Pracoval v týmech s mnoha dalšími vědci na dokumentaci řady metod určených ke kontrole kvality, používajících jak kontrolní vzorky, tak výsledky pacientů. Napsal šest knih a je autorem simulačních programů pro statistickou kontrolu kvality. Jeho webová stránka www.westgard.com je bohatým zdrojem informací o statistické kontrole kvality.
První generace SQC vznikla ještě před vývojem automatizovaných analyzátorů a začala zaváděním Shewhartových a Levey-Jenningsových grafů (30., resp. 50. léta 20. století) do klinické biochemie. První aplikace těchto grafů v klinické chemii používaly kreslicí papír, zpočátku bez různých hodnotových hladin. Za standardní, resp. tradiční QC se považovalo použití minimálně 2 hladin kontrol 1x za den v rámci jedné série testovaných pacientů (N = 2, R = 1) pro všechny metody a jako QC rozmezí se používala rozmezí daná výrobci kontrolních materiálů a nepoužívala se žádná rozhodovací pravidla vymezující přijatelná rozmezí.
Druhá generace SQC přišla s prvními automatizovanými analyzátory, které snížily výskyt náhodných chyb, takže se do hledáčku dostaly chyby systematické a potřeba je detekovat. Ta vedla k zavedení nových kontrolních grafů, jako je CUSUM graf (E. Page, 1954), a k prvnímu pokusu o využití výsledků pacientů ke QC, jako jsou průměry normálů (AON, 1965, Robert Hoffmann a Michael Waid). Za pravou SQC je považována ta, v níž se počet, typ a frekvence testování QC materiálů určuje z testované výkonnosti laboratoře. Cílem takové SQC je detekce chyb v čase pomocí postupů QC sloužících k monitorování přesnosti a preciznosti komplexu analytického procesu, které ovlivňují změny zkušebního systému, podmínky prostředí a výkon operátorů. Vývoj pravé SQC umožnila elektronizace QC.
Třetí generace SQC přichází se zaváděním informatiky. Kombinace informatiky a laboratorní techniky vedla k vývoji automatizovaných modelů analyzátorů, kde kontrolu kvality převzaly počítačové programy. V tomto období se nejprve používala známá ovládací Westgardova multipravidla (W-m-p.) a algoritmus klouzavých průměrů (Brian Bull, 1974). V laboratořích se od použití dvou kontrolních vzorků v jedné sérii a jednoho rozhodovacího pravidla (N = 2, R = 1 + 1 W-p., obvykle 12s) a od rozmezí kontrolních materiálů od výrobců pro všechny metody došlo postupně přes N = 2, R = 2 s kombinací W-p. k cíli, tzv. pravé SQC, kde počty kontrolních vzorků na sérii a typ rozhodovacích pravidel určuje individuální výkon metody s ohledem na vlastní stanovenou (ověřenou) cílovou hodnotu průměrů a SD (N = x, R = y, W-m-pravidla). Bezpočet metod řízení kvality pak vytvořil potřebu vhodných technik výběru. První počítačové simulační programy snížily potřebu komplikovaného
matematického ověřování spolehlivosti různých metod kontroly kvality.

Čtvrtou generaci SQC představuje rychlý nástup laboratorních informačních systémů (LIS). Sjednocení všech laboratorních operací do jediného LIS, často spojeného s informačním systémem větší zdravotnické instituce (např. nemocniční – NIS), způsobilo radikální změny ve statistické kontrole kvality. Metody založené na výsledcích pacienta (průměr normálů, delta kontroly) mohou být v laboratoři realizovány bez obtíží. LIS také dosáhly významného snížení postanalytických chyb a plánování kvality a cílů QC.
Pátou generaci SQC tvoří automatizace laboratorních procesů. Preanalytické systémy (nebo obecněji laboratorní automatizační systémy – LAS) představují nejnovější trend v laboratorní technologii s velkým potenciálem pro budoucí zlepšení. Takové systémy především snižují preanalytické chyby, ale také řeší aspekty postanalytických úkolů, jako je archivace vzorků. Nakonec nové přístupy umožňují výběr nejvhodnější metody kontroly jakosti ve všech případech. 1. vydání doporučení CLSI C24 je datováno rokem 1991 (J. O. Westgard).
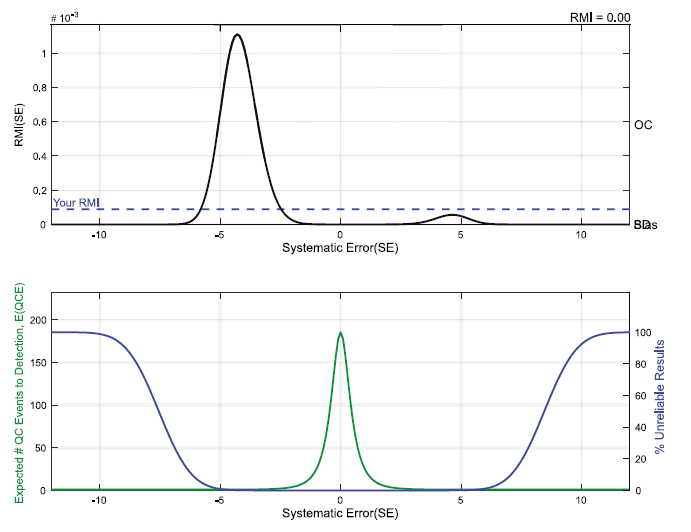
Za šestou generaci SQC jsou považovány plán absolutní kontroly kvality (TQCP), resp. individuální plán kontroly kvality (IQCP, CAP, 2016), jejichž nezbytnou součástí je definování požadavků a cílů na kvalitu, v nichž QC, počet N a R, typ W-m- -pravidel závisí na nových metrikách, jako je Six Sigma, a/nebo na odhadu rizik dané metody (CLSI EP23 (ISO 14791) Laboratorní QC založená na řízení rizik). TQCP je prezentován ve 4. vydání CLSI C24 (C. A. Parvin). Nezbytnou součást technické výbavy představuje sofistikovaný QC software (např. UnityRealTime a Mission Control MC, viz obrázky č. 4 a 5). Oba grafy programu MC verze 2 mají jedno společné: jak index řízení rizika (RMI, černá křivka v horním grafu), tak počet nespolehlivých výsledků a kontrolních vzorků potřebných k jejich odhalení (modrá a zelená křivka
ve spodním grafu) jsou funkcí systémové chyby (obrázek č. 4).
ISO 15189: od teorie SQC k praxi
Nový standard vytvořený výhradně pro zdravotnické laboratoře EN ISO 1518 vyzývá klinické laboratoře, aby používaly nejmodernější metody a dodržovaly pokyny
mezinárodních vědeckých organizací. Pro diagnostické účely musí laboratoře používat IVD činidla a zařízení. Pracovníci laboratoře musí být obeznámeni s veškerými
podrobnostmi svých metod (tj. s principy, interferencemi a zejména výkonnostními/provozními charakteristikami metod) a mít je na paměti v každodenní praxi. Použití správných metod interní kontroly jakosti a účast laboratoře v cyklech externích kontrol kvality dle normy ISO 15189 změnily jeden ze základních úkolů manažerů kvality laboratoře. Norma ISO 15189 také do klinických laboratoří přinesla některé nové koncepce statistické kontroly kvality. Odhady limitů detekce, referenčních/rozhodovacích mezí a nejistoty se staly součástí podmínek úspěšné akreditace klinické laboratoře. Stanovení zdrojů neurčitosti a odhadu jejich hodnoty
pro každou metodu je základním nástrojem porovnávání metod vytvořených různými laboratořemi navzájem.
Zkratky:
SQC: statistická kontrola kvality.
TQCP: plán absolutního řízení kvality.
TEa: přijatelná celková chyba.
MU: nejistota měření.
QC/PT/EQC: kontrola kvality/testování výkonnosti/externí kontrola kvality.
W-m-p.: Westgardova multipravidla.
RMI: index řízení rizika.