Predikce preeklampsie
Kombinovaný screening v I. trimestru těhotenství (v 11.–13. týdnu) by ve své optimální podobě měl být zaměřený na predikci a vyhledávání nejčastějších závažných porodnických komplikací, mezi které patří především velké porodnické syndromy (preeklampsie, růstová restrikce plodu, předčasný porod, nitroděložní úmrtí plodu) a vrozené vady plodu.1,2
Incidence uvedených porodnických komplikací je následující: preeklampsie (cca 1–5 %), růstová restrikce plodu (cca 5–10 %), předčasný porod (cca 8 %), úmrtí plodu v děloze (cca 0,5 %) a vrozené vady plodu (cca 2–3 %).3,4,5 Preferován by měl být komplexní screening nejen nejčastějších vrozených vad plodu (morfologických a chromosomálních), ale i těhotenství s rizikem rozvoje preeklampsie a růstové restrikce plodu, protože u žen se zvýšeným rizikem je možná účinná prevence rozvoje závažných forem onemocnění včasným zahájením léčby kyselinou acetylsalicylovou.6
Etiologie a patogeneze preeklampsie
Preeklampsie (Preeclampsia, PE) je závažné multiorgánové onemocnění komplikující těhotenství, které je charakterizováno placentární a kardiovaskulární dysfunkcí. Je celosvětově hlavní příčinou mateřské a perinatální mortality a morbidity. Odhaduje se, že následkem PE zemře každoročně více než 50 000 žen.7 Při placentární a kardiovaskulární dysfunkci je snížený přísun krve do placenty, což způsobuje hypoxii s možnou patologickou aktivací endotelu. U plodu může dojít k rozvoji růstové restrikce (Fetal Growth Restriction, FGR), event. k nitroděložnímu úmrtí a u těhotné ženy hrozí rozvoj multiorgánového postižení. V nejzávažnějších případech vyžaduje stav těhotné ženy a/nebo plodu iatrogenní předčasný porod, protože jediným kauzálním řešením patologického stavu je odstranění placenty. PE/FGR však neohrožuje ženu/ plod pouze v těhotenství, ale významně zvyšuje riziko závažných kardiovaskulárních onemocnění v dalším životě.8,9,10 Existuje mnoho důkazů, že PE není jedno onemocnění, ale zahrnuje dvě fenotypově odlišné jednotky. Označení jednotlivých typů představuje problém. Nejčastěji bývá uvedeno rozdělení na časnou PE (Early-PE) do 34. gestačního týdne a pozdní PE (Late-PE) od 34. týdne. Některé publikace však rozlišují časnou a pozdní PE do 32., resp. od 32. gestačního týdne. Mimo to se v celé řadě studií uvádí i termíny PE před termínem (< 37. týden) a PE v termínu (≥ 37. týden). Rovněž není vždy jednoznačné, zda je typ PE určen dle dne stanovení diagnózy nebo dle dne porodu.11,12
Přestože terminologie není jednotná, všechny publikace se shodují na tom, že patofyziologie těchto dvou stavů je odlišná, i když se mohou překrývat. Časná PE se rozvíjí jako důsledek především abnormální placentace a placentární dysfunkce, zatímco pozdní PE vzniká převážně následkem kardiovaskulární dysfunkce těhotné ženy. Tato klasifikace má i prognostickou hodnotu, protože časná PE s sebou nese výrazně vyšší riziko komplikací jak pro těhotnou ženu, tak i pro plod. Tím, že patofyziologie pozdní PE převážně nesouvisí s placentou, je spojena s nižší mírou postižení plodu a příznivějšími perinatálními výsledky.13,14,15,16
Predikce preeklampsie
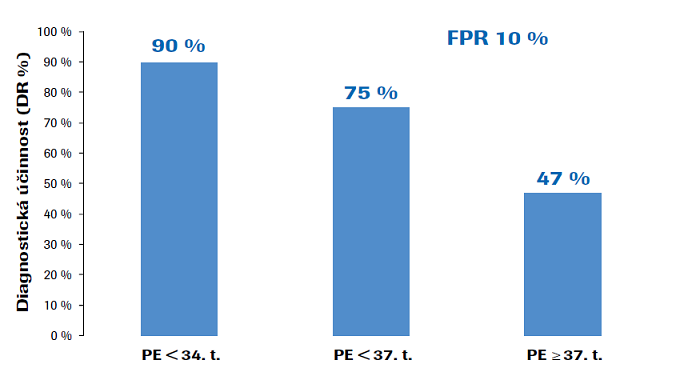
dle algoritmu The Fetal Medicine Foundation (FMF).
Časná PE (< 34. gestační týden), PE před termínem (< 37. gestační týden) a PE v termínu (≥ 37. gestační týden); FPR – false positivity rate (falešná pozitivita). Upraveno dle O'Gorman N et al. Competing risks model in screening for preeclampsia bynmaternal factors and biomarkers at 11-13 weeks gestation. Am J Obstet Gynecol. 2016 Jan; 214(1): 103.e1-103.e12.
Jednotná metodika predikce PE při provádění kombinovaného screeningu v I. trimestru těhotenství není v České republice (ČR) definována žádnou z institucí, které zodpovídají za organizaci péče o těhotnou ženu. V ČR neexistuje národní screeningový program PE (Ministerstvo zdravotnictví ČR, MZ ČR) ani doporučení odborné společnosti (Česká gynekologická a porodnická společnost České lékařské společnosti Jana Evangelisty Purkyně, ČGPS ČLS JEP).
V jiných zemích, pokud doporučení existuje, je riziko PE hodnoceno na základě maternálních charakteristik a anamnestických rizikových faktorů.17,18 Dle výsledků studie SPREE je však diagnostická účinnost takto provedeného screeningu velmi nízká. Při 10% falešné pozitivitě byla diagnostická účinnost PE před termínem 40 % a pro PE v termínu pouze 26 %.19
Jediná, v mnoha studiích validovaná metodika pro provádění screeningu PE s dostatečnou diagnostickou účinností je dána The Fetal Medicine Foundation (FMF). K výpočtu rizika je využíván Bayesův teorém, který je založen na kombinování řady parametrů. Hodnoty jsou převáděny na násobky mediánu a vzájemnou kombinací všech parametrů je kalkulováno individuální riziko pro těhotnou ženu a daný gestační věk. Podmínkou pro provedení je mít k dispozici validovaný software (SW), který je schopen kombinovat všechny požadované parametry a tímto způsobem riziko spočítat.20
Základní parametry podle metodiky FMF
Jak bylo uvedeno, účinnost takto provedeného screeningu byla validovaná v mnoha studiích. První validační studie O'Gormana a kol. z roku 2016 ukázala, že při 10% falešné pozitivitě byla diagnostická účinnost časné PE 90 %, PE před termínem 75 % a PE v termínu 47 %.21 (Obr. 1) Tan a kol. analyzovali výsledky 61 174 screeningů jednočetných těhotenství provedených v 11. až 13. gestačním týdnu a stanovili diagnostickou účinnost pro kombinace jednotlivých parametrů. Z výsledků jednoznačně vyplynulo, že pro predikci vzniku PE před termínem je nejúčinnější kombinace maternálních parametrů (maternální charakteristiky a anamnestické rizikové faktory) a biofyzikálních (pulzatilní index v děložních tepnách) a biochemických parametrů (sérová hodnota placentárního růstového faktoru). Hodnoty PAPP-A účinnost screeningu nijak nezvýšily, ale přesto se do výpočtu rizika započítávají.22 (Tab. 1)
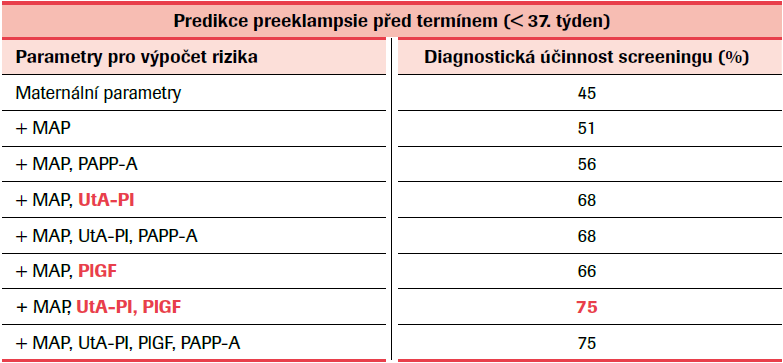
MAP – Middle Arterial Pressure (střední arteriální tlak); PAPP-A – Pregnancy Associated Plasma Protein-A (s těhotenstvím asociovaný plazmatický protein-A); UtA-PI – Uterine Artery Pulsatility Index (pulzatilní index v děložní tepně); PlGF – Placental Growth Factor (placentární růstový faktor). Upraveno dle: O´Gorman N.et al. Competing risks model in screening for preeclampsia by maternal factors and biomarkers at 11-13 weeks gestation. Am J Obstet Gynecol. 2016 Jan;214(1):103.e1-130.e12.
Mezi maternální parametry patří: věk, výška, váha, rasa, chronická hypertenze, systémový lupus erythematodes a antifosfolipidový syndrom, in vitro fertilizace, PE v rodinné anamnéze, diabetes mellitus, počet předchozích porodů bez PE a s PE. (Tab. 2) Biofyzikální parametry jsou: hodnota středního arteriálního tlaku u těhotné ženy (Mean Arterial Pressure, MAP) a hodnota pulzatilního indexu v děložních tepnách při dopplerovském ultrazvukovém vyšetření (Uterine artery Pulsatility Index, UtA-PI).
Mezi biochemické parametry, které se započítávají do výsledného rizika, řadíme sérovou hodnotu placentárního růstového faktoru (Placental Growth Factor, PlGF) a s těhotenstvím asociovaného plazmatického proteinu A (Pregnancy Asscociated Plasma Protein-A, PAPP-A). Vzhledem k nedostatečné standardizaci jednotlivých parametrů existují významné rozdíly mezi naměřenými hodnotami v závislosti na zvoleném systému. Používaný SW by měl být schopen přepočítat absolutní hodnoty na násobky mediánu v závislosti na použitém měřicím systému. Nejčastěji jsou používány systémy Roche, ThermoFisher a Perkin Elmer. V ČR je publikováno společné doporučení odborných společností (Česká společnost klinické biochemie – ČSKB ČLS JEP, Společnost lékařské genetiky a genomiky – SLG ČLS JEP) definující základní analytické požadavky na biochemické parametry screeningu.23
Optimální hodnota cut-off
Při výběru optimální cut-off hodnoty individuálního rizika pro rozvoj PE, která identifikuje „těhotenství se zvýšeným rizikem rozvoje PE“, je nutné zamyslet se nad vstupními rizikovými faktory, které tuto hodnotu ovlivňují. U screeningu PE se ocitáme ve zcela stejné situaci jako u rizika Downova syndromu. I tady nelze použít individuální hodnotu cut-off, ale hodnota musí být stanovena s ohledem na nejrizikovější faktor a tím je v případě Downova syndromu věk těhotné ženy. Riziko vzniku
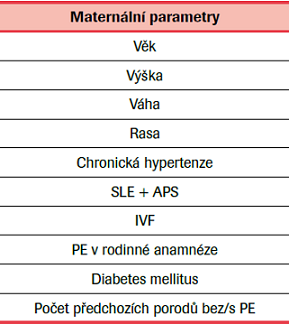
Systémový lupus erythematodes (SLE), antifosfolipidový syndrom (APS), in vitro fertilizace (IVF).
PE ovlivňuje celá řada parametrů a není možné používat hodnoty cut-off v závislosti na jednotlivých parametrech. Optimální hodnota cut-off pro multietnickou populaci byla stanovena na 1 : 100.22 Nicméně v závislosti na rase může být falešná pozitivita významně vyšší než 10 %. U screeningu Downova syndromu se snažíme falešnou pozitivitu co nejvíce snižovat, protože následně indikované invazivní výkony jsou spojeny s rizikem spontánního potratu zdravého plodu. V případě těhotenství se zvýšeným rizikem rozvoje PE je těhotné ženě nabídnuta léčba kyselinou acetylsalicylovou, která nemá žádné závažné nežádoucí účinky na těhotnou ženu nebo plod,
a zvýšená falešná pozitivita screeningu je tudíž akceptovatelná.24 Prevence preeklampsie Prevence velkých porodnických syndromů způsobených poruchou placentace je složitá. Je známo, že odpočinek v posteli a různé dietní manipulace riziko vzniku nesnižují. Účinné je podávání vápníku u populace žen s jeho nízkým příjmem, čímž se riziko PE může snížit až na polovinu. Odpočinek na lůžku, omezení příjmu soli a suplementace různými vitaminy však účinné nejsou. V mnoha studiích bylo prokázáno, že podávání nízkých dávek kyseliny acetylsalicylové v těhotenství významným způsobem snižuje výskyt PE.24,25
Mechanismus účinku kyseliny acetylsalicylové (Aspirin, Anopyrin)
Kyselina acetylsalicylová ireverzibilně (nevratně) inaktivuje enzym cyklooxygenázu (COX), který je v organismu odpovědný za syntézu prostaglandinů a tromboxanů z kyseliny arachidonové. Díkymá výrazné protizánětlivé a antitrombotické účinky. Pro prevenci placentární insuficience je nejdůležitějším mechanismem selektivní inhibice syntézy tromboxanu bez ovlivnění syntézy prostacyklinu. Tím se snižuje riziko zvýšené vazokonstrikce cév, agregace krevních destiček a tvorby trombů v placentě. Kromě toho zlepšuje nedostatečnou trofoblastickou invazi produkcí specifických cytokinů, snížením apoptózy a změnou buněčné agregace a fúze. V hypoxických podmínkách vykazuje i proangiogenní účinky tím, že inhibuje expresi sFlt-1 v lidských trofoblastech.26 Podávání antitrombotických léků založených na jiném principu (např. léky z řady nízkomolekulárních heparinů) nemá na prevenci placentárních onemocnění žádný vliv.
Studie ASPRE
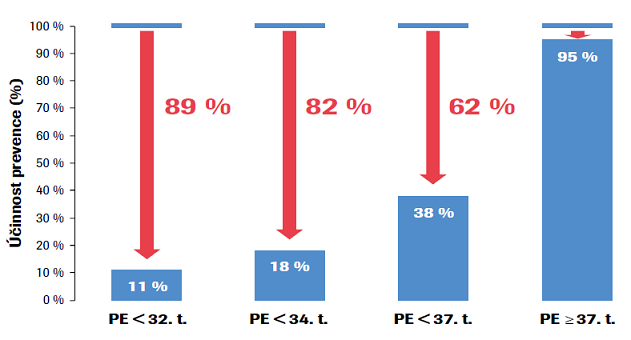
Závažné formy časné PE (< 32. gestační týden), časná PE (< 34. gestační týden), PE před termínem (< 37. gestační týden) a PE v termínu (≥ 37. gestační týden).
Upraveno dle Rolnik DL et al. Aspirin versus placebo in pregnancies at high risk for preterm preeclampsia. N Engl J Med 2017 AUg 17;377(7):613-622.
Účinek Aspirinu byl validován v mezinárodní multicentrické studii ASPRE (Combined Multimarker Screening and Randomized Patient Treatment with Aspirin for Evidence-Based Preeclampsia Prevention). Těhotným ženám v této studii byl proveden kombinovaný screening v 11.–13. týdnu těhotenství a dle metodiky FMF byla identifikována skupina žen se zvýšeným rizikem rozvoje PE. Těmto ženám byl podáván Aspirin v dávce 150 mg perorálně jedenkrát denně večer. Léčba byla zahájena v cca 12. týdnu, vždy však před 16. týdnem. Jak již bylo uvedeno, Aspirin pomáhá při zlepšování procesu placentace. Pokud je vývoj placenty dokončen v 16. týdnu, měla by léčba začít v době, kdy proces placentace probíhá, nikoli po jeho ukončení. Z tohoto důvodu je stanovení rizika rozvoje PE po 16. týdnu (např. v rámci screeningu vrozených vad plodu ve II. trimestru) zavádějící, protože účinnost preventivního podávání Aspirinu po 16. týdnu je nízká. Léčba byla ukončena před 36. týdnem z důvodů obav, že by Aspirin mohl způsobit krvácení do mozku nebo jiné hemoragické poruchy u plodu a novorozence. 27,28 Aspirin podávaný od 12. do 36. týdne snížil výskyt PE před termínem o 62 %, časné PE před 34. týdnem o 82 % a PE před 32. týdnem téměř o 90 %. Dle očekávání nemělo podávání Aspirinu významný vliv na výskyt pozdní PE. Naopak největší účinek má Aspirin na rozvoj časné PE a téměř eliminuje její nejzávažnější formy (HELLP syndrom a formy rozvíjející se před 32. týdnem).27 (Obr. 2)
Závěr
Preeklampsie představuje závažnou porodnickou komplikaci, jejíž jedinou účinnou léčbou je ukončení těhotenství, v mnoha případech iatrogenním předčasným porodem. Výsledky studie ASPRE jednoznačně prokázaly účinek podávání nízkých dávekkyseliny acetylsalicylové na prevenci rozvoje časné PE a jejích nejzávažnějších forem. Predikce PE v rámci kombinovaného screeningu v I. trimestru těhotenství (v 11.–13. týdnu) umožní identifikovat rizikové skupiny těhotných žen, které by
mohly profitovat z profylaktického prodávání kyseliny acetylsalicylové. Největší diagnostickou účinnost vykazuje screening provedený dle metodiky FMF, založený
na kombinaci mateřských, biofyzikálních a biochemických parametrů.

Nadace fetální medicíny (The Fetal Medicine Foundation) je registrovaná charita, jejímž cílem je zlepšit zdraví těhotných žen a jejich dětí prostřednictvím výzkumu a školení v oboru fetální medicíny. Nadace s podporou mezinárodní skupiny odborníků zavedla vzdělávací program pro zdravotnické pracovníky i rodiče a řadu osvědčení o způsobilosti v různých aspektech fetální medicíny. Více na https://fetalmedicine.org/

FIGO (International Federation of Gynecology and Obstetrics) je profesionální organizace, která sdružuje porodnická a gynekologická sdružení z celého světa. FIGO je oficiálním partnerem Světové zdravotnické organizace (World Health Organization, WHO) a Organizace spojených národů (United Nations, UN). Více na https://www.figo.org/