Asfyxií rozumíme přerušení dodávky kyslíku do organismu. Perinatální asfyxie je způsobená hypoxií plodu, ke které došlo v děloze před porodem nebo během porodu. Následkem toho vzniká hypoxémie, hyperkapnie a metabolická acidóza. Tyto změny vedou k hypoxicko-ischemické encefalopatii a dle rozsahu může dojít k rozvoji dětské mozkové obrny a dalších trvalých poruch funkce mozku. Časné stanovení prognózy u novorozenců s hypoxicko-ischemickou encefalopatií je obtížné. K základním úkonům mimo jiné patří zhodnocení neurologického stavu novorozence, aEEG a laboratorních parametrů včetně proteinu S100B. A právě protein S100B se jeví jako rychlý, senzitivní a specifický neurobiomarker v hodnocení tíže perinatální asfyxie a v predikci psychomotorického vývoje.
Perinatální asfyxie
Perinatální asfyxie je způsobená hypoxií plodu, ke které došlo v děloze před porodem nebo během porodu. Tento jev je provázen oběhovým a respiračním selháním s poškozením činnosti mozku a ostatních orgánů. Tyto změny vedou k hypoxicko-ischemickému poškození orgánů (mozek, ledviny, srdce, játra…) s následným rozvojem encefalopatie.
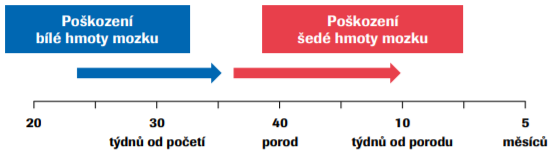
Hypoxicko-ischemická encefalopatie (HIE) je projevem poškození CNS po hypoxické příhodě. Nejčastějšími příznaky jsou křeče, porucha vědomí, poruchy svalového napětí a reflexů. U většiny novorozenců se středně těžkou a těžkou HIE je přítomna dysfunkce alespoň jednoho orgánového systému. Dlouhodobým následkem HIE může být rozvoj dětské mozkové obrny a dalších trvalých poruch funkce mozku.1,2,3
Pokud nastane hypoxie během porodu, dochází nejprve ke kompenzačním mechanismům s cílem udržet normální saturaci kyslíkem. Jestliže nedojde k odstranění příčiny hypoxie, dochází u novorozence k primární zástavě dechu, která je následována tzv. lapavými dechy (gaspy). Pokud ani nadále nedojde k úpravě stavu, dochází k rozvoji sekundární zástavy dechu, kdy se již spontánní dechová aktivita bez adekvátní pomoci neobnoví. Když se lapavé dechy objeví ještě před porodem, dochází k vdechnutí plodové vody. Při protrahované hypoxii nastává ochabnutí řitního svěrače s uvolněním smolky do plodové vody, čímž se prohlubuje bludný kruh, jelikož může dojít během gaspů také k vdechnutí mekonia (syndrom aspirace mekonia). Cílem minimalizovat následky hypoxie je co nejdříve vybavit dítě (operační porod – vakuumextrakce, forceps, akutní císařský řez). Asfyktický novorozenec po vybavení obvykle nedýchá, je bledocyanotický a potřebuje akutní resuscitaci k obnovení základních životních funkcí. Rychlost srdeční akce je dobrým bezprostředním ukazatelem tíže asfyxie a její úprava je odezvou správně vedené resuscitace.2

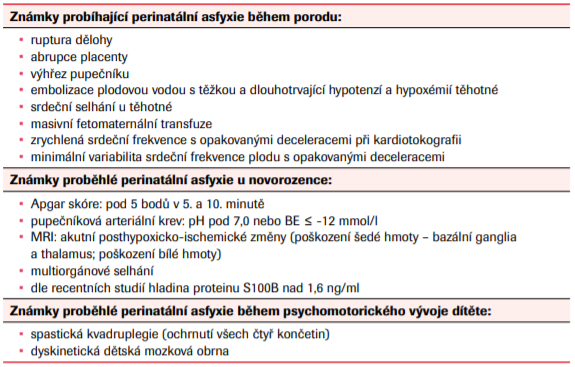
K hodnocení stavu po narození se celosvětově využívá skóre dle Apgarové. Hodnoty v první minutě se 4–7 body odpovídají lehké až střední asfyxii, 0–3 body odpovídají těžké asfyxii. Ke zhodnocení závažnosti asfyxie slouží také vyšetření acidobazické rovnováhy z pupečníkové krve. Čím závažnější asfyxie je, tím výraznější je acidóza v pupečníkové krvi. Nicméně nejdůležitějším ukazatelem je poporodní adaptace novorozence a případný neurologický deficit po porodu. V současnosti jedinou terapeutickou metodou využívanou k minimalizaci postasfyktických změn je celotělová řízená terapeutická hypotermie. Úspěšně resuscitovaný novorozenec se střední až těžkou asfyxií často vyžaduje intenzivní péči pro stabilizaci a podporu základních životních funkcí.1,2,4
Příčiny asfyxie mohou být na straně matky či dítěte. K mateřským příčinám patří abrupce placenty, pravý uzel na pupečníku, krátký pupečník způsobující nepostupující porod, kefalopelvický nepoměr, eklampsie, placenta praevia, ruptura dělohy a jiné. K příčinám ze strany dítěte patří vrozené vývojové vady, intrauterinní růstová restrikce, syndrom aspirace mekonia, krevní ztráty a další.2,5 Incidence perinatální asfyxie je závislá na její definici, kvalitě porodnické péče a včasné diagnostice. Ve světě se incidence perinatální asfyxie pohybuje okolo 5–8 na 1 000 živě narozených dětí a četnost hypoxicko-ischemické encefalopatie (HIE) se udává kolem 1 z 1 000 živě narozených dětí. V rozvojových zemích je vyšší riziko perinatální asfyxie a je jednou z hlavních příčin mortality a morbidity u dětí do 1 roku věku.2,3
Klinický obraz dítěte s perinatální asfyxií
Neurologické příznaky v časném období:
• Porucha sání
• Hypotonie
• Křeče, porucha vědomí
• Nereagující zornice
Orgánové dysfunkce v časném období:
• Plíce: TTN – tranzitorní tachypnoe novorozence, RDS (syndrom dechové tísně), pneumonie, MAS (syndrom aspirace mekonia), PPHN (perzistující plicní hypertenze)
• Srdce a cévy: insuficience myokardu, nekróza papilárních svalů, hypotenze
• Ledviny: renální selhání, oligo/anurie, polyurie, hematurie
• Játra: poškození hepatocytů, hyperbilirubinémie
• Hematologie: DIC – diseminovaná intravaskulární koagulace, trombocytopenie
• Střevo: NEC – nekrotizující enterokolitida

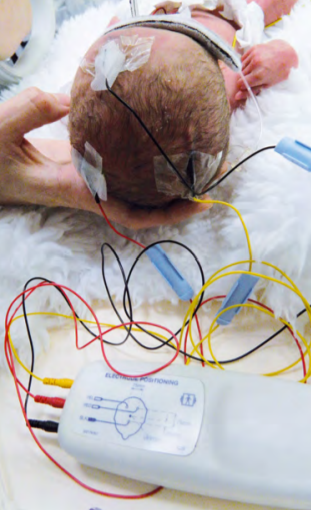
Zdroj: Novorozenecké oddělení Fakultní nemocnice v Olomouci
Prevence
Jedinou možnou prevencí je zamezení vzniku rozvoje akutní hypoxie v průběhu porodu, což je vzhledem k obtížné diagnostice a široké diferenciální diagnostice velmi obtížné. Jednou z mála možných prevencí jsou zejména pravidelné gynekologické kontroly v těhotenství a kardiotokografický záznam během porodu.2
Terapie
U indikovaných novorozenců je zahájena jediná ověřená neuroprotektivní terapie, a to celotělová řízená terapeutická hypotermie, která musí být zahájena nejpozději do 6 hodin od hypoxické příhody (indikační kritéria viz tab. 2). Jestliže novorozenec splní A i B kritéria, pak je zahájena neprodleně hypotermie a transport do perinatologického centra, kde je natočen amplitudově integrovaný elektroencefalografický (aEEG) záznam. Při abnormním aEEG záznamu je pokračováno v hypotermii, při normálním aEEG záznamu lze hypotermii ukončit vzhledem k vysoké pravděpodobnosti normálního psychomotorického vývoje. Doporučená délka hypotermie je po dobu 72 hodin, cílem je udržet teplotu v rektu mezi 33–34 °C. Zchlazení tělesného jádra významně zpomaluje metabolické pochody v mozku, čímž je dosaženo neuroprotektivity. Dle studií zlepšuje tato terapie prognózu u 1–2 z 5 novorozenců s těžkou HIE.2,3,6
Samozřejmostí je podpůrná terapie ke stabilizaci oběhu a respiračních funkcí. Novorozenci jsou během hypotermie v drtivé většině případů napojeni na umělou plicní ventilaci (i vzhledem k jejich komfortu) a důsledně analgosedováni (na našem pracovišti máme dobré zkušenosti s kombinací sufentanil + dexmedetomidin). Nezřídka se můžeme setkat s refrakterní hypotenzí s nutností kombinace katecholaminů a kortikoterapie. Důležitou součástí terapie je také úprava metabolického rozvratu (acidóza, hypoglykémie nebo hyperglykémie). Pokud se vyskytnou křeče, pak zahajujeme antikonvulzivní terapii (fenobarbital jako lék 1. volby, dále lidokain, levetiracetam či klonazepam).1,2
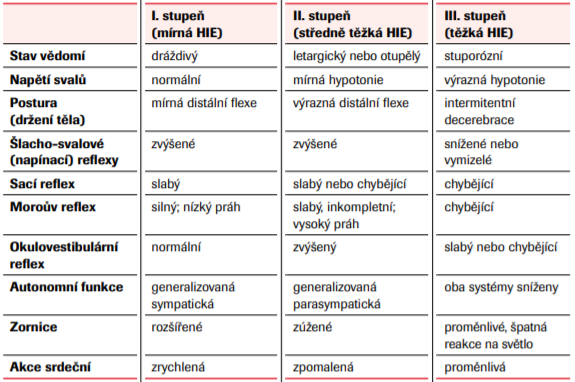
Prognóza
U dětí s mírnou a středně těžkou hypoxicko-ischemickou encefalopatií je většinou zcela normální psychomotorický vývoj.7 U těžké hypoxicko-ischemické encefalopatie je 75% riziko úmrtí v časném novorozeneckém období, případně vysoké riziko dlouhodobého těžkého neurologického deficitu. Mezi mírné následky patří např. poruchy učení nebo pozornosti. Mezi těžké následky patří zejména dětská mozková obrna (DMO), epilepsie, poruchy zraku a sluchu, mentální insuficience. Tyto děti jsou pravidelně sledovány dětským neurologem.1,8
Časné stanovení prognózy u novorozenců s HIE je i pro zkušeného lékaře obtížné až nemožné. Berličkami ve stanovení prognózy je zhodnocení mnoha parametrů zároveň – především tíže HIE, vstupní laboratorní parametry (tíže acidózy, protein S100B), rozvoj MODS, rychlost úpravy aEEG záznamu během hypotermie, RI index na arteria cerebri anterior, nález na MRI, neurologický stav novorozence.5,7,9


Laboratorní a pomocná vyšetření

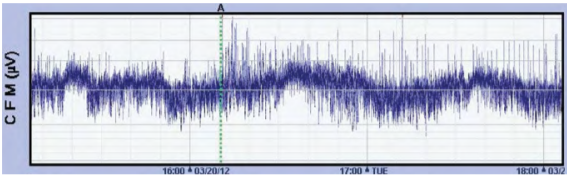
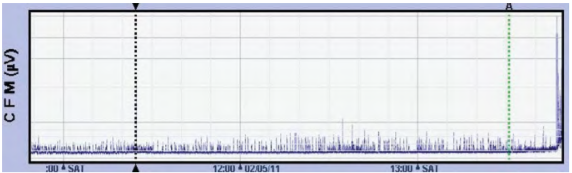
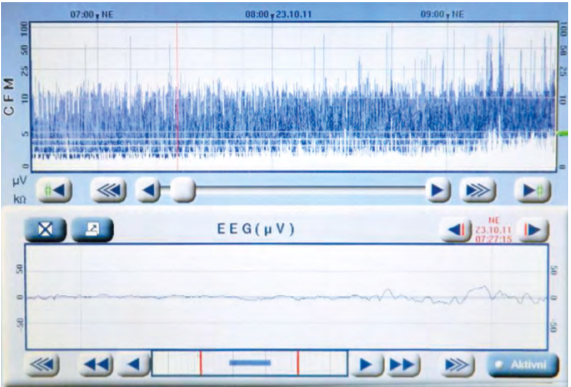
Nedílnou součástí je vyšetření acidobazické rovnováhy z pupečníkové krve (pH < -16 mmol/l), k monitoraci mozkové aktivity využíváme záznam aEEG (amplitudově integrovaný elektroencefalografický záznam). K ověření hypoxicko-ischemických změn na mozku nám slouží ultrazvukové vyšetření, případně magnetická rezonance mozku.2,6 Vyšetření kardiomarkerů (troponin, NT-proBNP, CK-MB) nám pomáhá zhodnotit postižení myokardu, nicméně tyto kardiomarkery nejsou specifické pro perinatální asfyxii. Dále je vhodné opakované sledování renálních parametrů a iontogramu vzhledem k velmi častému renálnímu postižení. Pravidelně také vyšetřujeme jaterní enzymy, díky čemuž monitorujeme posthypoxické postižení jater.2
Dle recentních literárních zdrojů se jeví jako nadějný marker mozkového postižení protein S100B.10
S100 proteiny
Jedná se o bílkoviny malé molekulové hmotnosti, jejichž významnou vlastností je vazba dvou Ca2+ a Zn2+. Díky těmto vazbám mohou vykonávat důležité intra – i extracelulární funkce.11 Název S100 si členové této rodiny vysloužili díky své rozpustnosti ve 100% nasyceném síranu amonném.12 Tyto malé proteiny jsou tkáňově, resp. buněčně specifické.13 Jednou z nejdůležitějších vlastností (funkcí) S100 proteinů je jejich schopnost chovat se po přestupu z intra- do extracelulárního prostoru jako alarminy neboli damage-associated molecular pattern molecules (DAMPS).14 Alarminy prostřednictvím specifických receptorů aktivují imunitní systém a zásadním způsobem zasahují a ovlivňují imunitní odpověď na poškození tkání. Hrají také významnou roli v reparaci tkání, například při poškození mozku působí S100A4 stejně jako S100B neuroprotektivně. 15 Extracelulárně působící S100 proteiny pracují především díky interakci s povrchovými buněčnými receptory RAGE (receptors for advanced glycosylation end products) a TLR4 (toll-like receptor 4).14,16 TLR4 převážně rozpoznávají lipopolysacharidovou komponentu buněčné stěny G negativních bakterií.17 Aktivují polymorfonukleáry, monocyty a makrofágy a tím zahajují imunitní odpověď.18,19,20 RAGE jsou exprimovány pouze buňkami, které jsou součástí zánětlivé imunitní odpovědi21 a jsou pravděpodobně hlavními aktéry tkáňového hojení a odpovědi na akutní poškození tkání.22
Protein S100B, resp. vápník vázající protein S100B, je významným členem rodiny S100 proteinů. Je exprimován převážně astrocyty, Schwannovými buňkami, určitými skupinami neuronů a buňkami odvozenými od buněk myeloidních.23 K jeho uvolnění z poškozených gliálních buněk do krevního oběhu dojde ihned při poškození CNS (trauma, hypoxie aj.). Následně je eliminován ledvinami. Poločas v krevním řečišti je 30 až 100 minut.24,25,26 S100B byl detekován v různých tělních tekutinách (plodová voda, likvor, krev, moč, sliny, mateřské mléko).10

Význam proteinu S100B v hodnocení tíže perinatální asfyxie a v predikci psychomotorického vývoje
Vyšetření proteinu S100B může identifikovat novorozence s rizikem hypoxicko-ischemické encefalopatie (HIE) po proběhlé perinatální asfyxii, odhadnout rozsah poškození mozku a pomoci s prognózou u kojenců s HIE v anamnéze.15 První autoři zabývající se S100B proteinem jakožto markerem postižení CNS u novorozenců měřili tuto bílkovinu v mozkomíšním moku. Už v roce 2001 Whitelaw et al. prokázali, že předčasně narození novorozenci s posthemoragickou dilatací mozkových komor mají v likvoru vyšší hladiny S100B proteinu než zdravé kontroly. Tyto hodnoty byly vyšší i u dětí, které zemřely, u dětí se zavedeným shuntem, i při měření v 1. roce života u dětí, které byly následkem krvácení nějakým způsobem handicapované.27 Stejně nadějné výsledky publikoval také Blennow, který ve své studii potvrdil zvýšené hladiny S100B v likvoru u donošených novorozenců po poporodní asfyxii. A co je důležité, hladina S100B korelovala s neurologickým postižením v 1. roce života dítěte.28
Vzhledem k tomu, že odběr mozkomíšního moku je vyšetření ne zcela neinvazivní, bylo třeba zjistit, zda se S100B po CNS poškození objevuje u asfyktických novorozenců také v krvi. Dle výsledků metaanalýzy z roku 2020 byly hladiny S100B v krvi novorozenců s postasfyktickou hypoxicko-ischemickou encefalopatií rovněž zvýšené. Dle závěrů metaanalýzy byla stanovena ideální cut-off hodnota proteinu S100B z periferní krve 1,6 ng/ml (specificita 91%, senzitivita 40 %).10
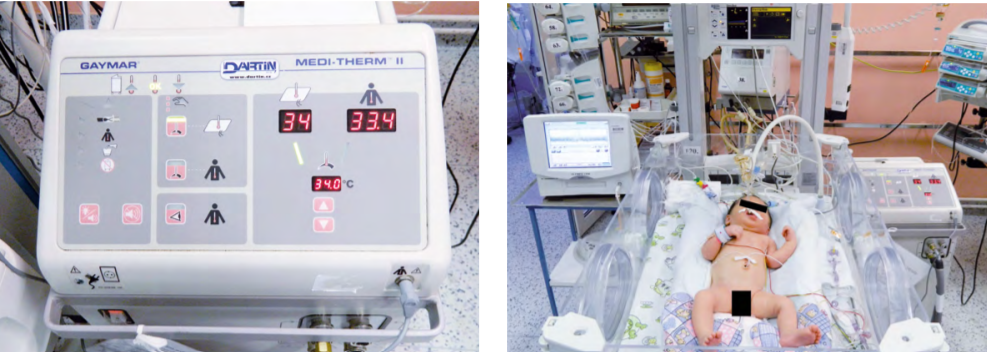
Obr. 6: Novorozenec během celotělové řízené hypotermie; vlevo aEEG monitor, vpravo přístroj pro hypotermii. Zdroj: Novorozenecké oddělení Fakultní nemocnice v Olomouci
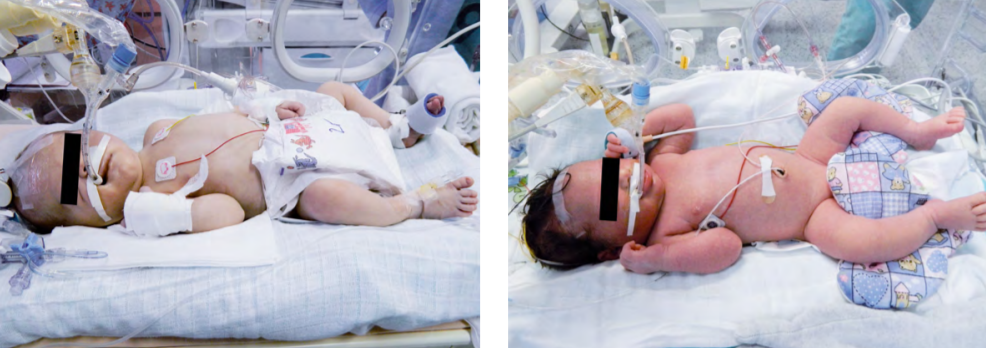
Obr. 8: Novorozenec během celotělové řízené hypotermie. Zdroj: Novorozenecké oddělení Fakultní nemocnice v Olomouci

S100B a jeho další využití
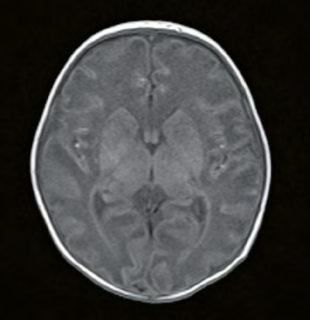
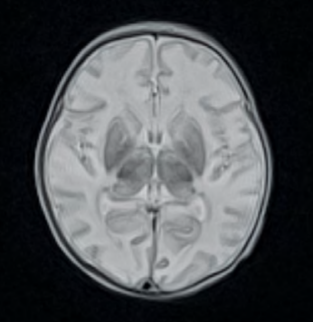
Jednou z obávaných komplikací a nejčastější formou mozkového krvácení u extrémně nezralých novorozenců je intraventrikulární hemoragie (IVH). Tento stav není jednoduché diagnostikovat, jelikož během prvních 72 hodin mohou klinické příznaky chybět a radiologické zobrazení mozku může být falešně negativní.
Bersani ve svém review z roku 2020 popisuje řadu studií, kde měřili S100B v periferní krvi či v pupečníku. Nejzásadnější zjištění, která uvádí, jsou:
(i) S100B byl zvýšený u předčasně narozených novorozenců s intraventrikulární hemoragií (IVH), a to již 48 hodin před pozitivním ultrazvukovým nálezem a rozvojem klinických příznaků. Korelovala také výše S100B a rozsah postižení.
(ii) u předčasně narozených novorozenců s intrauterinní růstovou retardací (IUGR) byl S100B také elevován.
Kromě diagnostiky postižení CNS u asfyktických novorozenců se tohoto proteinu využívá také v řadě dalších oborů.
K nejčastějším situacím patří měření hladin S100B při traumatickém poškození hlavy. Dle některých studií by mohlo měření S100B v prvních hodinách po lehkém poškození mozku nahradit vyšetření CT (computed tomography) a tím např. u dětí snížit, resp. zamezit radiační zátěži. Rozsah postižení a anatomické rozložení traumatu samozřejmě tímto vyšetřením zjistit nelze. Inhibici tohoto proteinu je možné využít například v léčbě maligního melanomu. Ukázalo se, že S100B je také důležitý nástroj monitorace léčby ER (estrogen receptor) pozitivního karcinomu prsu. Zvýšené hladiny S100B v tkáních a séru jsou ukazatelem špatné prognózy u pacientek na hormonální terapii. Navíc zvýšené hladiny sérového S100B detekované během rutinních kontrol jsou významně spojené s recidivou onemocnění.15
Závěr
Hypoxické postižení mozku novorozence může vést k takzvané hypoxicko-ischemické encefalopatii. Dle tíže poškození mozku je dítě ohroženo rozvojem dětské mozkové obrny a dalších trvalých poruch funkce mozku. Časné stanovení prognózy u novorozenců s hypoxicko-ischemickou encefalopatií je důležité, avšak obtížné. Vedle klinického zhodnocení neurologického stavu novorozence hodnotíme také úpravu záznamu aEEG během hypotermie. Z biochemických metod se jeví výhodné využití proteinu S100B vázajícího vápník. Tento neurobiomarker je zvýšený u postižení mozku. Praxe na našem pracovišti potvrzuje výsledky z recentních literární zdrojů, tj. že u hypoxicko-ischemické encefalopatie jsou hladiny proteinu S100B zpravidla zvýšené.