Preeklampsie je těhotenské multisystémové onemocnění a jedna ze závažných příčin morbidity a mortality matek a dětí.1 Postihuje asi 2–5 % těhotenství.2,3 Etiologie je stále neznámá, i když v posledních letech se rozsah vědomostí o patofyziologii tohoto stavu významně zlepšil. Dříve se za preeklampsii považovaly stavy s výskytem vysokého krevního tlaku a proteinurií ve druhé polovině těhotenství. ACOG (American College of Obstetricians and Gynecologists) byla první odbornou společností, která v roce 2013 průkopnicky definici preeklampsie změnila.4 Za preeklampsii začala považovat i stavy spojené s hypertenzí bez proteinurie, následované známkami hematologickými (trombocytopenie), hepatologickými (zvýšení AST, ALT) či neurologickými (např. oční změny) nebo plicními (plicní edém). V roce 2018 přijala tuto rozšířenou definici i FIGO (Mezinárodní federace gynekologů a porodníků).5 Kromě funkčních parametrů zmíněných ACOG lze preeklampsii definovat také tehdy, pokud u nového výskytu hypertenze v těhotenství dochází k růstové restrikci plodu (IUGR). Placentární komponenta hraje zřejmě významnou roli v etiologii preeklampsie, takže proto lze samotnou kombinaci hypertenze a IUGR již považovat za projevy preeklampsie.6
Z výše uvedeného vyplývá, že proteinurie již není pro definici preeklampsie nutná. Tato informace se objevila i v doporučeních Německé společnosti pro gynekologii a porodnictví (DGGG). Nově byly také uznány výhody nových biomarkerů. Pokud se k hypertenzi přidá změna sérových angiogenních faktorů, lze tento stav považovat za preeklampsii. Již dříve provedené prospektivní studie ukázaly, že poměr sFlt-1/PlGF může pomoci ke správnému stanovení diagnózy v případě nejasné, klinicky přítomné hypertenze. Tímto způsobem lze diagnózu časné preeklampsie stanovit s 89% senzitivitou a 95% specificitou, při hraniční hodnotě poměru 85. Pokud pracujeme s hraniční hodnotou 38, dosáhneme negativní prediktivní hodnoty 99,3 % pro vyloučení vzniku preeklampsie po dobu 7 příštích dnů a 36,7 % během příštích 4 týdnů. V klinické praxi lze v diferenciální diagnostice hypertenzních stavů v těhotenství použít graf s hraničními hodnotami 38 a 85 (viz graf č. 1).
Schéma použití poměru sFlt-1/PlGF v klinické praxi – komentář ke grafu č. 1
Hraniční hodnoty vychází z výsledků studie PROGNOSIS.13 Preeklampsie může být vyloučena s vysokou jistotou po dobu jednoho až čtyř týdnů, pokud poměr sFlt-1/PlGF nepřesáhne 38, kontrola by měla proběhnout do 4 týdnů. Pokud je u klinického podezření na preeklampsii hodnota poměru sFlt-1/PlGF 38–85, hrozí vysoké riziko rozvoje preeklampsie během následujících 4 týdnů. Asi u jedné ze 3 těhotných se v následujících 4 týdnech rozvine preeklampsie a ve stejném období je pravděpodobnost asi 66 %, že se rozvine preeklampsie a/nebo alespoň jedna z komplikací. V tomto případě se doporučuje kontrola v týdenním intervalu. Při překročení mezní hodnoty 85 hrozí vysoké riziko časného výskytu komplikací preeklampsie. Za preeklampsii lze považovat již zvýšený krevní tlak v kombinaci se zvýšeným poměrem sFlt-1/PlGF nad 85.

Pokroky v diagnostice a prevenci preeklampsie
V posledních letech se podařilo zavést screening v prvním trimestru, jakož i predikci a diagnostiku pomocí nových laboratorních markerů ve druhém a třetím trimestru těhotenství. Rozsáhlé studie prokázaly, že v prvním trimestru lze vyhledat těhotné, u kterých se ve druhé polovině těhotenství rozvine časná preeklampsie. Využívá se k tomu kombinace anamnestických údajů, hodnot středního arteriálního tlaku matky, indexu pulzatility uterinních arterií a angiogenních markerů.7,8,9 Podávání nízkých dávek aspirinu rizikovým těhotným vybraným právě tímto postupem významně snižuje výskyt časné preeklampsie. Na predikci rozvoje pozdní preeklampsie po 37. týdnu má prvotrimestrální screening jen malý vliv.10,11 Zdá se, že pomocí angiogenních markerů a identifikací dalších rizikových faktorů během druhého a třetího trimestru těhotenství se podaří zlepšit i diagnostika a management této formy preeklampsie.12,13 Kombinace anamnézy, biofyzikálních faktorů a biochemie jako součást algoritmu FMF je optimální pro prvotrimestrální screening časné preeklampsie u všech těhotných. PAPP-A v rámci screeningu preeklampsie, nikoliv aneuploidií, má smysl vyšetřovat, resp. zařadit do algoritmu, pokud se nevyšetřuje PlGF.
Těhotným s pozitivním prvotrimestrálním screeningem na preeklampsii, tedy těm s vysokým rizikem, by mělo být doporučeno podávání kyseliny acetylsalicylové v dávce 100–150 mg denně až do 36. týdne těhotenství. Užívání by mělo být zahájeno ihned po identifikaci vysokého rizika preeklampsie, ale nejpozději před 16. týdnem těhotenství. Užívat by se měl nepřetržitě, každý den večer. Preventivní podávání kyseliny acetylsalicylové všem těhotným není doporučeno.14 V současné době není jednotná strategie propojení prvotrimestrálního screeningu s vhodnými strategiemi druhého a třetího trimestru. V roce 2003 bylo poprvé prokázáno, že u těhotných s preeklampsií jsou zvýšené sérové hladiny VEGF receptoru 1 a sFlt-1.15 Důležité bylo zjištění, že placentární exprese sFlt-1 je zvýšená a v séru měřitelná ještě před nástupem symptomů preeklampsie. Naproti tomu hladiny cirkulujícího PlGF jsou snížené.
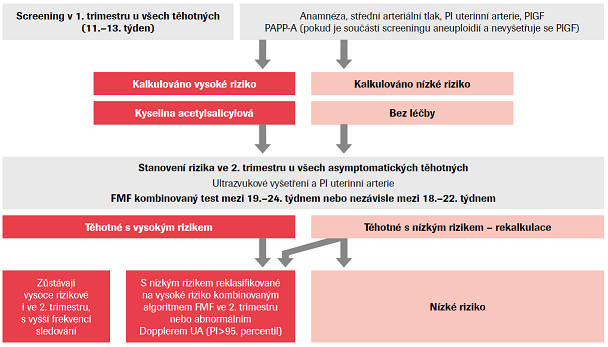
Volně podle L.C. Poon, S. Verlohren et al. From first-trimester screening to risk stratification of evolving pre-eclampsia in the second and third trimesters of pregnancy: a comprehensive approach. UOG 2019, doi: 10.1002/uog.21869
Podařilo se prokázat, že poměr sFlt-1/PlGF lze použít pro diagnostiku, predikci a prognózu preeklampsie.16,17 Následně byly vyhodnoceny automatizované testy pro použití v klinické praxi a byly stanoveny standardní rozsahy a hodnoty separace. S hraniční hodnotou poměru sFlt-1/PlGF 85 lze diagnostikovat časnou preeklampsii <34 + 0 týdnů s citlivostí 89 % a specificitou 97 %. Hraniční hodnota 85 není překročena u těhotných s jinými hypertenzními poruchami, u kterých se nevyvine preeklampsie a ani s ní spojené komplikace. U těhotenské hypertenze a u žen s chronickou hypertenzí nedochází k významnému zvýšení tohoto poměru. Dále se podařilo prokázat, že optimální mezní hodnota pro diagnózu preeklampsie po 34. týdnu těhotenství odpovídá hodnotě poměru sFlt-1/PlGF 110. Dvoufázovým měřením lze dosáhnout citlivosti až 88 % se specificitou až 99,5 %, a tak umožnit spolehlivou diagnózu preeklampsie.18,19,20

Volně podle L.C. Poon, S. Verlohren et al. From first-trimester screening to risk stratification of evolving pre-eclampsia in the second and third trimesters of pregnancy: a comprehensive approach. UOG 2019, doi: 10.1002/uog.21869
Posouzení rizik by mělo být provedeno ve druhém a třetím trimestru bez ohledu na výsledky screeningu v prvním trimestru. Dopplerovské měření v uterinních arteriích se provádí mezi 18. a 22. týdnem těhotenství. U asymptomatických žen považovaných za vysoce rizikové pro rozvoj preeklampsie buď na základě screeningu v prvním trimestru, nebo na základě dopplerovského měření uterinní arterie mezi 18. a 22. týdnem lze vyšetřit poměr sFlt-1/PlGF již mezi 24.–28. týdnem těhotenství. Alternativně je možné kombinovat měření v uterinních arteriích mezi 19. a 24. týdnem s dalšími vyšetřeními, včetně mateřského krevního tlaku, a angiogenními biomarkery. Toto hodnocení lze opakovat mezi 30. a 34. a 35. a 37. týdnem těhotenství, v závislosti na výši rizika. Opětovné posouzení rizika by mělo být provedeno u všech těhotných po 36. týdnu těhotenství, bez ohledu na předchozí klasifikaci rizika. To lze provést pomocí měření poměru sFlt-1/PlGF nebo použitím kombinovaného algoritmu ve 35.–37. týdnu těhotenství. Vysoké riziko preeklampsie stanovené prvotrimestrálním screeningem platí pro celé těhotenství. Těhotné, které byly původně v 1. trimestru klasifikovány jako nízkorizikové a u nichž byly mezi 18. a 22. týdnem naměřeny abnormální hodnoty průtoků v uterinní arterii (PI > 95. percentil) nebo které byly dodatečně klasifikovány jako vysoce rizikové pomocí screeningu algoritmem FMF pro 19.–24. týden, by měly být následně reklasifikovány jako vysoce rizikové a sledovány odpovídajícím způsobem.

U těhotných s klinickým podezřením na preeklampsii a nízkými hodnotami poměru sFlt-1/PlGF lze vyloučit nástup preeklampsie během příštích 7 dnů. NPH (negativní prediktivní hodnota) poměru sFlt-1/PlGF ≤38 pro výskyt PE v průběhu jednoho týdne je 99,3 % (při 95% intervalu spolehlivosti [CI] 97,9–99,9 %). Poměr sFlt-1/PlGF ≤38 vylučuje výskyt dalších komplikací během jednoho týdne také s vysokou spolehlivostí (NPH 98,5 %, CI 96,9–99,5 %). U hodnot nad 38 riziko preeklampsie a souvisejících komplikací stoupá. PPH (pozitivní prediktivní hodnota) poměru sFlt-1/PlGF >38 byla 36,7 % (CI 28,4–45,7 %). U jedné ze tří žen s klinickým podezřením a zvýšeným
kvocientem se tedy v následujících 4 týdnech objeví preeklampsie. PPH komplikací souvisejících s preeklampsií při poměru sFlt-1/PlGF >38 je 65,5 % (CI 56,3–74 %). U dvou ze tří žen s poměrem sFlt-1/PlGF >38 se tedy do čtyř týdnů rozvine preeklampsie a/nebo související komplikace.
Nástup PE a komplikací lze predikovat i mezi 24 + 0 a 36 + 6 týdnů těhotenství. Týká se těhotných:
- s nově vzniklou hypertenzí nebo zhoršením již existující hypertenze;
- s bolestmi hlavy a/nebo horní části břicha;
- s významnými otoky nebo náhlým přírůstkem hmotnosti;
- s patologickým dopplerovským vyšetřením plodu v souvislosti s placentární dysfunkcí (IUGR).
Při manifestní preeklampsii, eklampsii nebo HELLP syndromu nepřináší vyšetření poměru sFlt-1/PlGF další informaci, a proto v těchto jasných případech již není přínosem. Současně není stanovení sFlt-1/PlGF možné považovat za screeningové vyšetření preeklampsie ve druhém trimestru a nemělo by se používat u všech těhotných žen. Dále bylo prokázáno, že střední délka doby zbývajícího těhotenství u žen s poměrem sFlt-1/PlGF >38 je 17 dní ve srovnání s 51 dny u žen s hodnotou ≤38.21 Zvláštní pozornost by měla být věnována také opakovaným vyšetřením: u těhotných s rychlým nárůstem hodnot během 2 a 3 týdnů je signifikantně vyšší pravděpodobnost vzniku preeklampsie nebo souvisejících komplikací. Ve skupině pacientek s preeklampsií je průměrné zvýšení poměru sFlt-1/PlGF mezi dvěma měřeními do 2 týdnů 31,2, zatímco u pacientek bez preeklampsie je to pouze 1,45.22
Závěry pro praxi
Kombinace anamnézy, biofyzikálních faktorů a biochemie jako součást algoritmu FMF je optimální pro prvotrimestrální screening časné preeklampsie u všech těhotných. Preventivní podávání kyseliny acetylsalicylové těhotným s vysokým rizikem rozvoje časné preeklampsie snižuje významně rozvoj onemocnění před 32. týdnem těhotenství. Užívání kyseliny acetylsalicylové by mělo být zahájeno nejpozději před 16. týdnem těhotenství. Preventivní podávání kyseliny acetylsalicylové všem těhotným není doporučeno. V současné době se nabízí jednotná strategie propojení prvotrimestrálního screeningu s vhodnými strategiemi druhého a třetího trimestru. Stanovení poměru sFlt-1/PlGF ve druhé polovině těhotenství se stalo nepostradatelným diferenciálně diagnostickým vyšetřením v klinické praxi. Umožňuje rychle a efektivně vyloučit preeklampsii u žen s hypertenzí, u kterých je klinické podezření na preeklampsii, a predikovat těhotenské komplikace, které jsou způsobeny placentární dysfunkcí. Naměřené hodnoty poměru sFlt-1/PlGF či jeho dynamika umožňují včas reagovat na hrozící rozvoj preeklampsie a poskytují informace o možnostech prodloužení těhotenství. Výsledky vyšetření umožnují modifikovat sledování těhotných, zejména se bezpečně rozhodnout o možnosti ambulantního sledování.
Seznam zkratek
ALT – Alanin transamináza; AST – Aspartát aminotransferáza; CI – Confidence interval, interval spolehlivosti; DGGG – Deutsche Gesellschaft für Gynäkologie und Geburtshilfe; FIGO – Fédération Internationale de Gynécologie et d’Obstétrique, International Federation of Gynecology and Obstetrics; FMF – Fetal Medicine Foundation, nadace fetální medicíny se sídlem v Londýně; HELLP – Hemolysis Elevated Liver enzymes and Low Platelets; IUGR – Intra uterine growth restriction, intrauterinní růstová restrikce plodu; NPH – Negativní prediktivní hodnota; PAPP-A – Pregnancy-associated plasma protein A; PE – Preeklampsie; PlGF – Placental growth factor, placentární růstový faktor; PPH – Pozitivní prediktivní hodnota; sFlt-1 – Soluble fms-like tyrosine kinase-1; rozpustná fms podobná tyrosinová kináza 1.