Firma Roche uvedla začátkem roku 2017 novou generaci metody Elecsys® Vitamin D total II v první etapě na modulu cobas e 801. Inovovaná metoda byla otestována v ostravské laboratoři společnosti SPADIA LAB, a.s. a je možné potvrdit, že došlo k dalšímu zvýšení klinické a analytické hodnoty tohoto stanovení.
Úvod
V posledních letech se enormně zvyšuje počet klinických indikací pro kvantifikaci vitaminu D v biologickém materiálu, který souvisí s narůstajícím významem tohoto analytu – vitamin D představuje důležitou komponentu v homeostáze kalcia a fosfátů v lidském organismu. Deficit vitaminu D lze pozorovat u chronických onemocnění, a to jak u chorob kostního systému (rachitis, osteoporóza, osteomalacie), tak u mimokostních nemocí (kardiovaskulární choroby, nádorová onemocnění, autoimunitní choroby, diabetes mellitus a infekce).
Syntéza a metabolismus vitaminu D
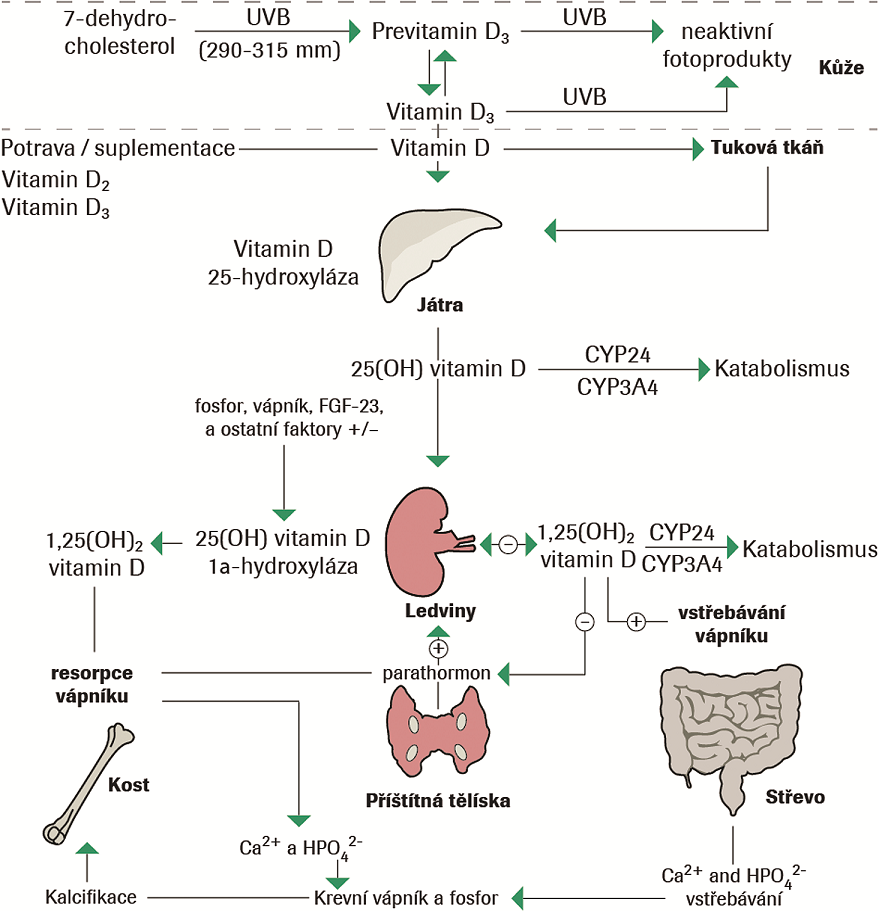
Syntéza a metabolismus vitaminu D představují složité mechanismy reakcí probíhajících v lidském organismu od neaktivních prekurzorů až k účinné formě vitaminu D (viz obr. 1). Rozlišují se dvě hlavní formy vitaminu D: vitamin D3 (cholekalciferol) živočišného původu a vitamin D2 (ergokalciferol) rostlinného původu, přičemž ergokalciferol ve stravě představuje jen omezený zdroj příjmu a majoritním zdrojem pro člověka je endogenní produkce pod vlivem ultrafialového záření 1,2. Počátečním bodem endogenní strukturální přestavby vitaminu D je tzv. provitamin D3 (7-dehydrocholesterol), resp. provitamin D2 (ergosterol), který se v epidermis účinkem ultrafialového záření konvertuje na vitamin D3 (cholekalciferol), resp. vitamin D2 (ergokalciferol). Účinnost endogenní syntézy vitaminu D je závislá na době expozice slunečnímu záření, geografické poloze, ročním období, denní době, pigmentaci kůže a použití protektivních krémů na povrchu těla. Velmi důležitým aspektem je autoregulační systém endogenní syntézy. Při déletrvající sluneční expozici nedochází k elevaci vitaminu D, ale k přeměně provitaminu na biologicky neaktivní izomery 1,2,3.
Obě vzniklé formy vitaminu D (cholekalciferol i ergokalciferol) jsou biologicky inaktivní a pro potřeby organismu vyžadují dvoukrokovou aktivaci v játrech a ledvinách. V hepatocytech nastává primární hydroxylace v poloze 25 účinkem 25-hydroxylázy, přičemž reakcí vzniklý 25-hydroxyvitamin D (kalcidiol) je považován za nejvhodnější ukazatel stavu metabolismu vitaminu D v lidském organismu, který současně zohledňuje endogenní produkci i exogenní příjem vitaminu D potravou. Druhý stupeň dvoukrokové hydroxylace a aktivace probíhá v ledvinách v poloze 1 účinkem 25-hydroxy-1-a-hydroxylázy za vzniku 1,25-dihydroxyvitaminu D (kalcitriol). Biologicky aktivní 1,25-dihy-droxyvitamin D se intracelulárně váže na receptor vitaminu D, který je zodpovědný za biologické účinky 4.
Metoda Elecsys® Vitamin D total II
V roce 2017 uvedla firma Roche k rutinnímu užívání inovovanou soupravu Elecsys® Vitamin D total II – iniciálně pro systémy e 801, nyní v dostupnosti pro systémy e 401, e 601 a e 602. Počátkem roku 2017 byl poprvé v České republice instalován nový imunochemický modul e 801 v diagnostické laboratoři SPADIA LAB, a.s., Ostrava, a to na modulárním systému cobas® 8000 v konfiguraci c 502/c 702/e 801. Součástí implementace nového modulu v rutinním režimu bylo testování inovované diagnostické soupravy Vitamin D total II. Uvažujeme-li o vitaminu D, je nutné blíže specifikovat analyt, který stanovujeme. Metoda Elecsys® Vitamin D total II kvantifikuje sumární koncentraci 25-hydroxyvitaminu D2 a 25-hydroxyvitaminu D3.
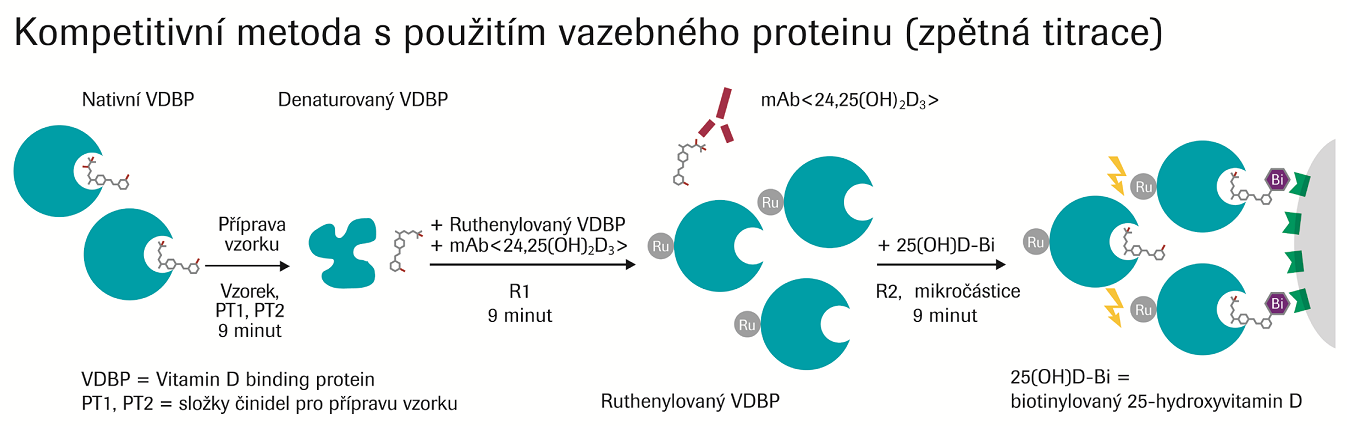
Souprava se vyznačuje přímou návazností na referenční metodu Ghent LC-MS/MS s detekcí v pozitivním módu v režimu sledování vícenásobných přechodů (MRM) a návazností na certifikovaný referenční materiál NIST 2972. Dalším důležitým aspektem je blokace neaktivního metabolitu 24,25-dihydroxyvitaminu D2/D3 (pomocí specifické monoklonální protilátky), vznikajícího při dostatečné saturaci hormonálně aktivního 1,25-dihydroxyvitaminu D2/D3 v organismu. Design testu je až na přidanou blokační protilátku totožný s předchozí generací 5. Iniciačním krokem stanovení je denaturace vitaminu D vázajícího protein (VDBP) v krvi, blokace neaktivního metabolitu 24,25-dihydroxyvitaminu D2/D3 užitím specifické monoklonální protilátky a následně přídavek VDBP značeného rutheniem k reakční směsi. Tímto krokem dochází ke specifické vazbě vitaminu D z pacientských sér se značeným VDBP. K vzniklému komplexu je přidán biotinem značený vitamin D, v reakční směsi dochází ke kompetitivnímu procesu stanovovaného vitaminu D se značeným vitaminem D. Celý komplex je následně navázán na pevnou fázi magnetické mikročástice prostřednictvím vazby biotinu a streptavidinu. Detekce průběhu analytické reakce probíhá pomocí elektrochemiluminiscence (viz obr. 2).
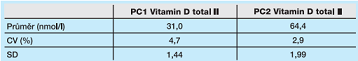
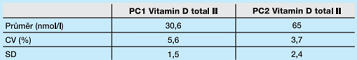
Inovovaná diagnostická souprava disponuje velmi uspokojivými analytickými charakteristikami testovanými v rutinní laboratoři, souhrn opakovatelnosti i mezilehlé preciznosti je uveden v tab. 2 a 3. Ke kalibraci metody byl využit inovovaný, firemně dodaný kalibrační materiál Vitamin D total II CalSet, kontrola kvality byla prováděna pomocí Vitamin D total II PreciControl (Roche) na dvou koncentračních úrovních – velmi pozitivně lze pohlížet na koncentrační úrovně použité v kontrolním materiálu s cílovými hodnotami v blízkosti klinicky významných rozhodovacích mezí. Firemní dokumentace výrobce doporučuje realizovat kalibraci metody ve frekvenci 1 x 28 dnů při používání stejné šarže reagencií, 1 x 7 dnů při používání identické soupravy v analyzátoru a/nebo dle potřeby podle vychýlení v procesu interní kontroly kvality 5. V námi testovaném období vykazovala diagnostická souprava vysokou stabilitu bez nutnosti provádění mimořádných kalibrací s absencí náhodných a systematických chyb v procesu interní kontroly kvality.
Srovnání metod
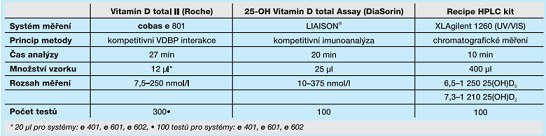
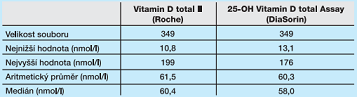
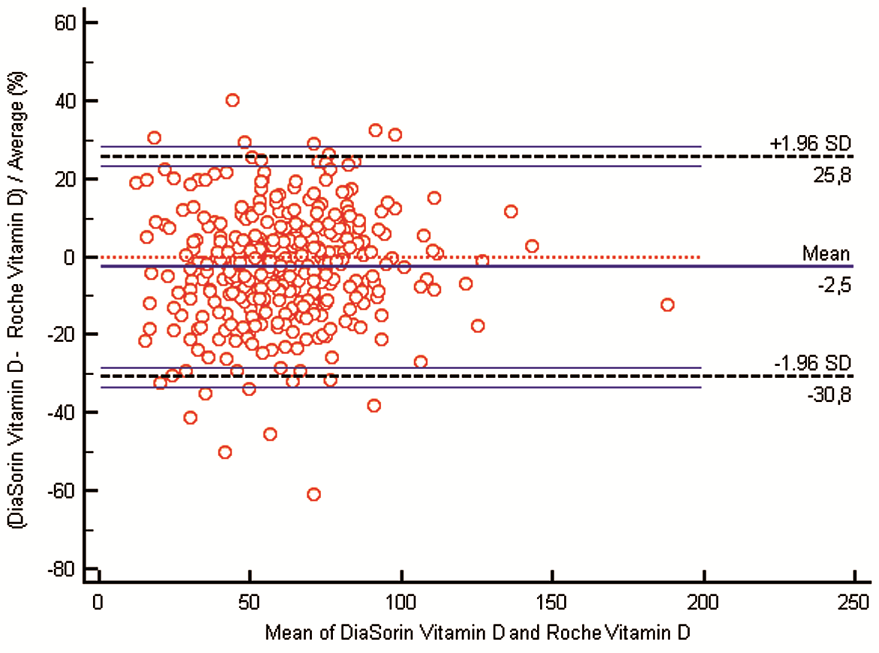
Cílem testování diagnostické soupravy bylo srovnání nové generace soupravy Vitamin D total II (Roche) s rutinně využívanou 25-OH Vitamin D total Assay (DiaSorin) na systému LIAISON® a s chromatografickým stanovením 25-hydroxyvitaminu D2/D3 použitím Recipe HPLC kitu. Základní charakteristiky měřicích technik shrnuje tab. 1. Srovnávací studie probíhala ve dvou navazujících etapách, první etapa srovnání datována na duben–červen s využitím zamrazeného biologického materiálu z Fakultní nemocnice Ostrava. Před analýzou bylo sérum temperováno na laboratorní teplotu a ve všech vzorcích byl vyšetřen 25-hydroxyvitamin D (suma 25-hydroxyvitaminu D2 a 25-hydroxyvitaminu D3) pomocí chromatografického stanovení s UV detekcí užitím 25-OH Vitaminu D2/D3 Recipe a pomocí imunoanalytických metod na systémech cobas® 8000 (Roche) a LIAISON® (DiaSorin). Do druhé etapy srovnání (květen–srpen) bylo bez bližší specifikace zařazeno celkem 349 rutinních vzorků pacientů ostravské diagnostické laboratoře SPADIA LAB, u kterých bylo lékařem indikováno stanovení 25-hydroxyvitaminu D. Aby byl minimalizován vliv preanalytické fáze ve druhé etapě, byly vzorky séra pro stanovení vitaminu D paralelně vyšetřeny na systémech cobas® 8000 a LIAISON®. Naměřená data byla statisticky zpracována pomocí softwaru MedCalc verze 16.1.2 (Belgie). Iniciálně byly hodnoceny sumární statistiky testovaného souboru I (tab. 4) a testovaného souboru II (tab. 5), ke zjištění statistické významnosti rozdílů průměrů naměřených hodnot byl použit Bland-Altmanův rozdílový graf, neparametrická regrese dle Passing-Babloka a korelační koeficient. Statistická významnost „p“ byla hodnocena dle Spearmanova testu na zvolené hladině významnosti.
Výsledky
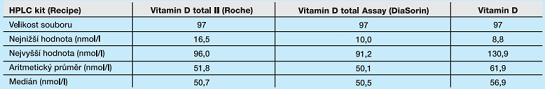
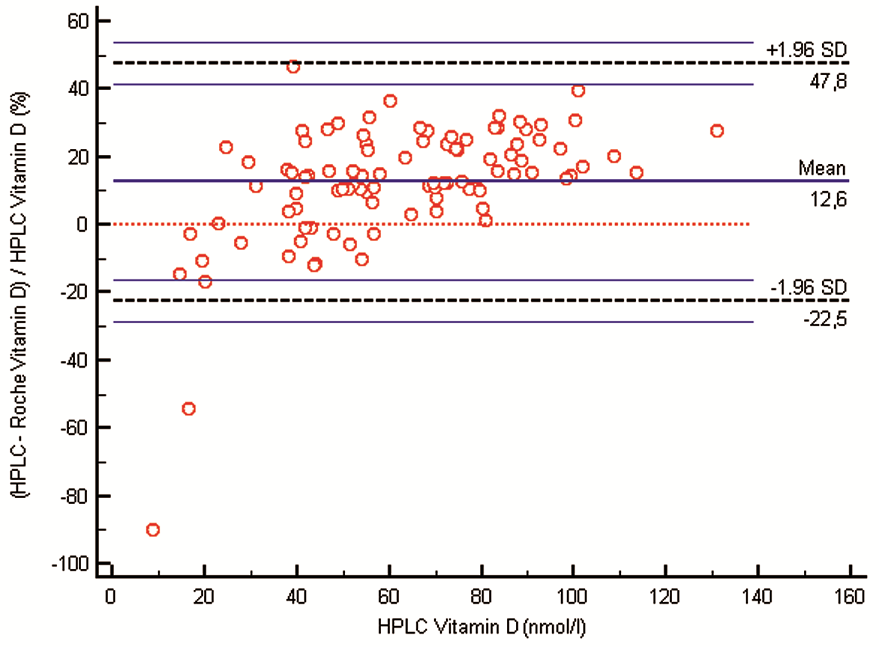
Sumární statistiky etapy I a II testovaných metod jsou shrnuty v tab. 4 a 5. Z dat první etapy je patrný rozdíl mezi imunoanalytickými metodami a chromatografickým stanovením 25-hydroxyvitaminu D v séru. Podle očekávání je variabilita výsledků stanovení vitaminu D etapy I statisticky významná mezi chromatografickým stanovením a jednotlivými imuno-analytickými metodami (graf 1, graf 2). Kvůli ověření statistické významnosti mezi imunoanalytickými metodami navzájem bylo přistoupeno k rozšíření testovaného souboru o rutinní vzorky a porovnání obou imunoanalytických metod (Roche vs. DiaSorin). Etapa II poskytla výstupy uvedené v tab. 5, grafy 3 a 4 reflektují výstupy shrnuté v diskusní části.
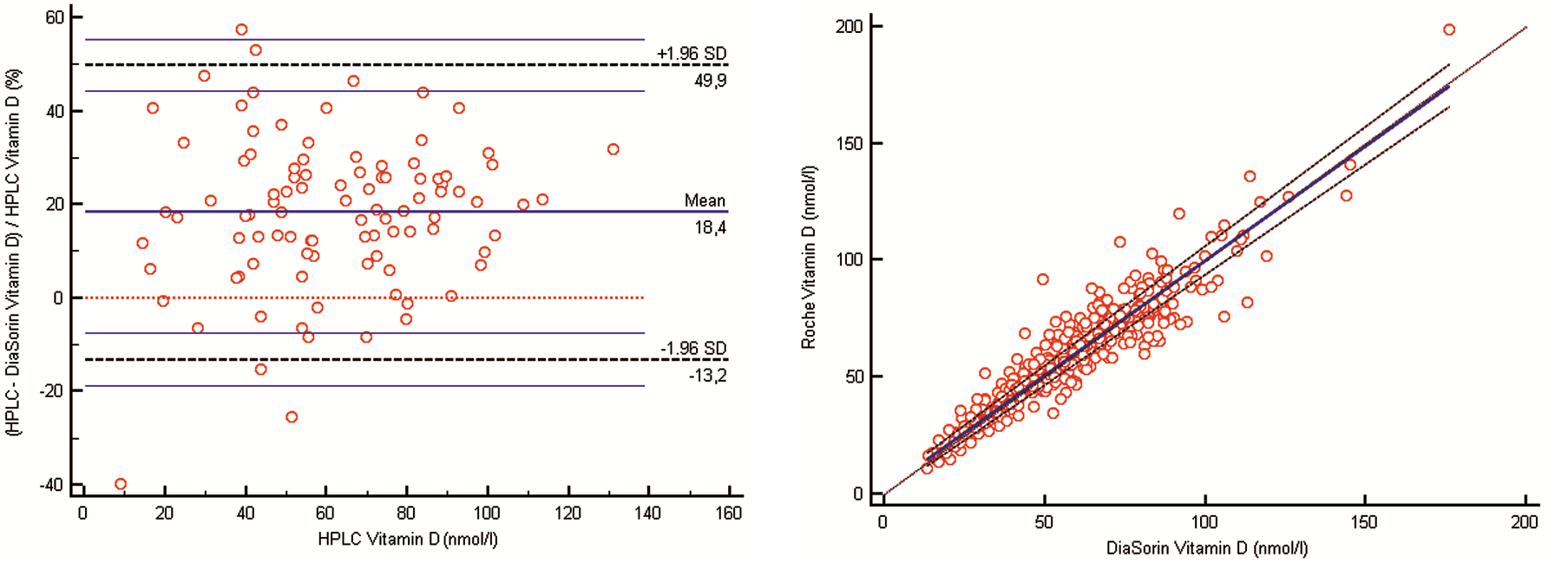
Graf 3: Passing-Bablokova regresní analýza srovnání stanovení 25-hydroxyvitaminu D, etapa II, imunoanalytické metody
Parametry Passing-Bablokovy regresní analýzy
Rovnice regresní přímky: Roche = 0,981.DiaSorin + 2,191 nmol/l
Korelační koeficient r = 0,92 (p < 0,001)
95% interval spolehlivosti směrnice (0,943–1,022)
95% Interval spolehlivosti interceptu (-0,307–4,137)
Diskuse
Je známou skutečností, že imunoanalytické metody stanovení 25-hydroxyvitaminu D jsou zatíženy nedostatečnou srovnatelností výsledků měření napříč výrobci diagnostických souprav 6,7. Limitujícím faktorem imunoanalytických metod jsou fyzikálně-chemické vlastnosti hydrofobního analytu 25-hydroxyvitaminu D a poměrně silná vazba na VDBP 7,8. Významnou měrou se na úrovni správnosti metod podílí úroveň vyvázání analytu z vazby na VDBP a rovněž dokonalost denaturace VDBP. Koncentrace VDBP je různá u různých skupin pacientů a tomuto také odpovídá příslušné ovlivnění naměřených koncentrací 25-hydroxyvitaminu D total II 9.
Rovněž zkřížené reaktivity ostatních metabolitů (např. 24,25-dihydroxyvitaminu D a 3-epi-25-hydroxyvitaminu D) mohou být příčinou významných systematických diferencí, zejména u specifických klinických kohort (pacienti s poškozením renální funkce se sníženými hladinami 24,25-dihydroxyvitaminu D) nebo dětských pacientů (zvýšená koncentrace C3-epimeru do 2 let věku).
U imunoanalytických metod velmi častá zkřížená reaktivita s 24,25(OH)2D (u diagnostické soupravy firmy DiaSorin není tato informace v příbalové dokumentaci k dispozici) byla v případě druhé generace metody Elecsys 25(OH) Vitamin D total II výrazně potlačena, nicméně příbalová dokumentace k této metodě stále deklaruje poměrně vysokou zkříženou reaktivitu vůči C-3-epimeru (113 % u 25(OH)D3 a 91 % u 25(OH)D2), která se v zásadě neliší od předchozí generace metody Elecsys. Otázkou této interference se zabýval ve své práci Van den Ouweland,11 který zjistil, že u nativních sér novorozenců (až do podílu 58 % C3-epimeru) k této zkřížené reaktivitě u metody Roche nedochází, což potvrdilo paralelní stanovení koncentrací metodou LC-MS/MS. Zjištěná zkřížená reaktivita deklarovaná v příbalovém letáku nevychází z nativních vzorků s endogenním obsahem C3-epimeru, nýbrž odráží chování u vzorků s exogenně přidaným C3-epimerem. Podobně se toto chování může projevit u vzorků využívaných v systému externího hodnocení kvality, což je potřeba brát v úvahu 11.
Naproti tomu výrazným benefitem imunoanalýzy je rychlost prováděných vyšetření a množství vzorku použitého k analýze. V komplexním pohledu je nutné konstatovat, že z námi naměřených dat nevyplývají statisticky významné rozdíly mezi metodami Vitamin D total II (Roche) a 25-OH Vitamin D total Assay (DiaSorin). Porovnání obou metod pomocí lineární Passing-Bablokovy regrese naznačuje, že obě metody poskytují srovnatelné výsledky stanovení 25-hydroxyvitaminu D (rovnice závislosti Roche = 0,981.DiaSorin + 2,191 nmol/l, přičemž 95% interval spolehlivosti směrnice obsahuje hodnotu 1 a interval spolehlivosti úseku obsahuje hodnotu 0, tedy s absencí konstantní i proporcionální chyby v celém měřeném rozsahu).
Závěr
Metoda Elecsys® Vitamin D total II (Roche) patří mezi nové, principiálně odlišné metody stanovení 25-hydroxyvitaminu D (specifická VDBP interakce), které umožňují monitorovat dostatečnou saturaci organismu vitaminem D a lze je rovněž bez obav použít u specifických klinických kohort pacientů. Přínos této inovované metody byl potvrzen testováním rutinních neselektovaných vzorků v diagnostické laboratoři. Ke zvýšení správnosti výsledku měření přispívá přímá návaznost na referenční metodu LC-MS/MS (Ghent) a certifikovaný referenční materiál NIST 2972.