Lidské papilomaviry (human papillomaviruses, HPV) patří do evolučně staré a rozsáhlé skupiny papilomavirů (PV) z čeledi Papillomaviridae. Jejich adaptace na přežívání v lidském organismu je dokonalá, jsou víceméně schopny dlouhodobě a možná i celoživotně přežívat v hostitelském organismu a efektivně se replikovat většinou bez ohrožení existence hostitele. Ale není tomu tak vždy.
Úvod a klasifikace
Kvalifikované odhady hovoří o tom, že existuje více než 400 typů PV infikujících nejen člověka, ale i jiné savce. Nicméně jejich výskyt byl potvrzen také u ptáků a plazů, nově dokonce i u ryb1, což nám umožňuje spekulovat o ještě starším původu PV, než se dosud předpokládalo. Dále se ukazuje, že PV se vyvíjely spolu se svými hostiteli, neměnily hostitelské druhy a udržely si základní organizaci genomu v téměř nezměněné podobě po více než 100 milionů let. Na základě fylogenetických výzkumů se ukazuje, že typy HPV16 a HPV18 pravděpodobně pocházejí z Afriky, odkud se rozšířily spolu s expanzí lidské populace do celého světa.
V roce 2004 publikoval tým prof. Haralda zur Hausen studii popisující zhruba 100 typů HPV 2. Avšak o deset let později (ke konci roku 2014) identifikuje práce Bzhalava et al. již 202 HPV typů, zatříděných ve 49 druzích celkem pěti rodů (α, ß, γ, µ, ν). Ale ve svých odhadech zmiňuje možnou existenci nejméně 400 typů HPV 3.
Struktura virionů a organizace genomu
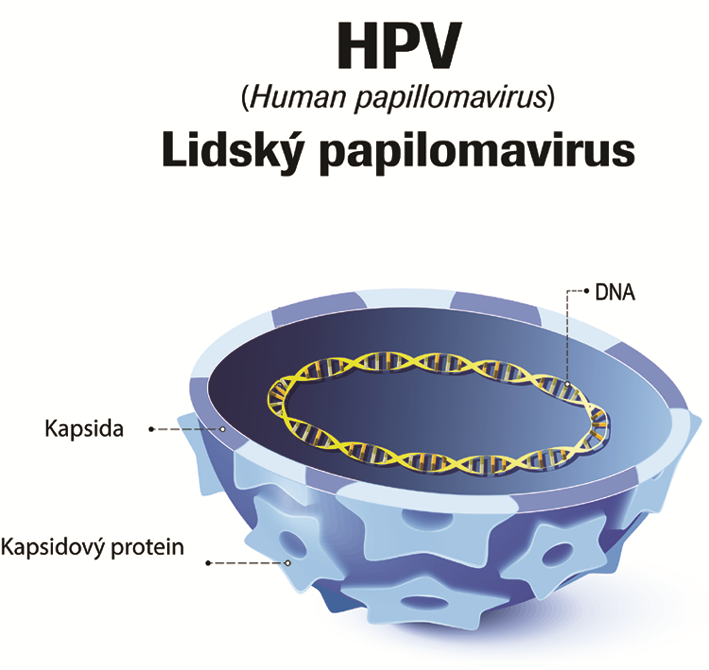
HPV jsou malé (55 nm) neobalené viry s dvouvláknovou DNA, tvořené kubickými viriony. Virová kapsida je sestavena z pentamerických kapsomer, které jsou tvořeny proteiny L1 a L2, kódovanými virovými geny.
Jejich genom je jednoduchý, s velikostí 7 500–8 000 párů bází. Porovnání mnoha genomů lidských a zvířecích papilomavirů ukazuje na zakonzervovanou základní organizaci virového genomu. Je totiž kódován (v drtivé většině případů) 8 geny: 6 z nich slouží jako geny časné fáze (early, E) a 2 se účastní pozdní fáze infekce (late, L). Geny E1, E2, E4–E7 kódují jaderné funkce viru, a to včetně E6 a E7 genů, které jsou zodpovědné za buněčnou transformaci a lze je klasifikovat jako virové onkogeny. Geny L1 a L2 kódují proteiny virové kapsidy a řídí tak skládání virionu a jeho uvolnění z hostitelské buňky 4. Genom dále obsahuje regulační elementy, jako jsou promotory exprese časných i pozdních genů, a taktéž nekódující oblast.
Patogeneze
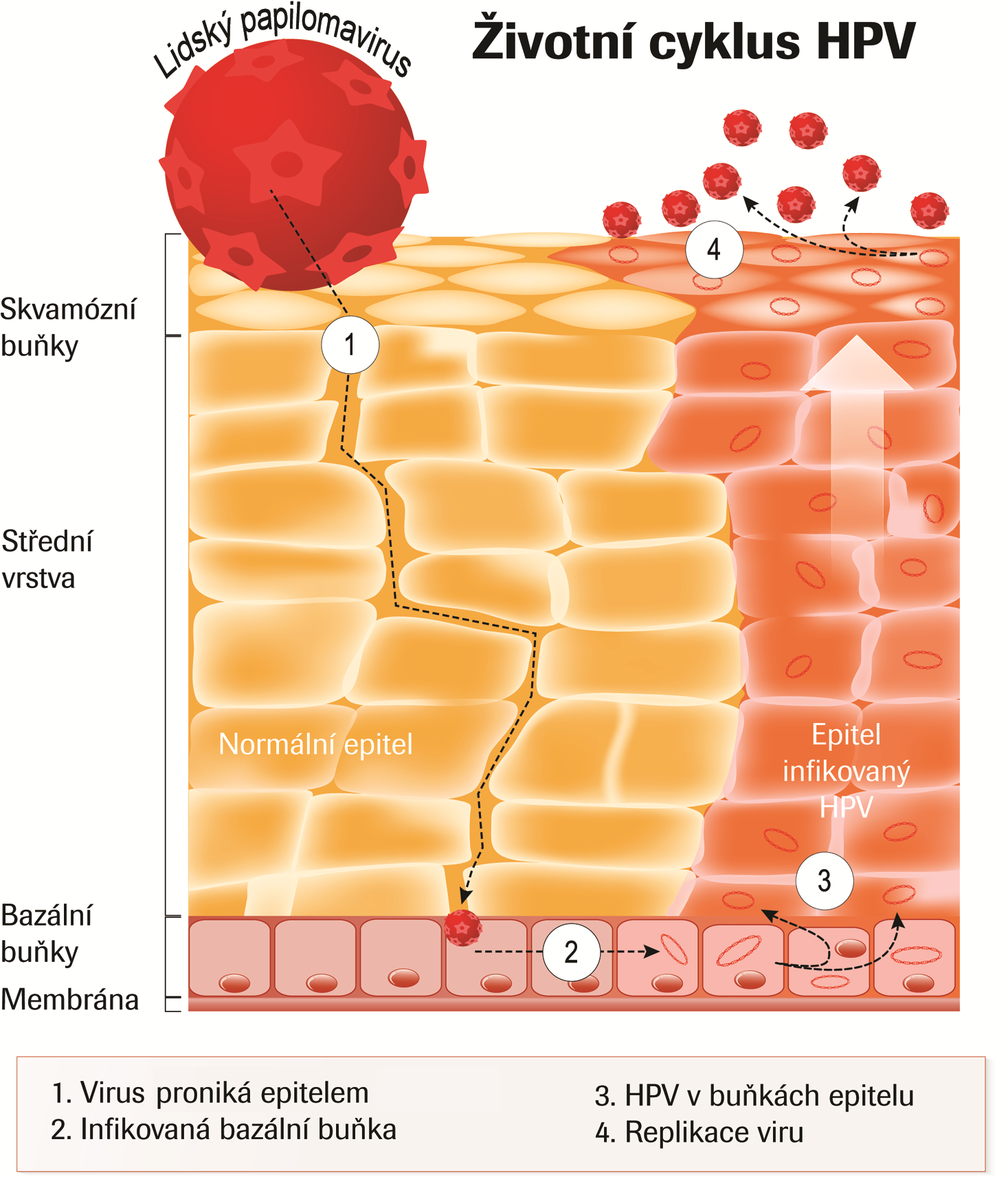
Papilomaviry jsou druhově specifické, což znamená, že napadají pouze živočišné druhy, se kterými se vyvíjely společně v průběhu evoluce. Dále lze konstatovat, že jsou striktně epiteliotropní (napadají pouze epitely) a tkáňově specifické – na základě tohoto tvrzení je lze rozdělit na druhy kožní a slizniční. Dalším možným rozdělením je členění na typy s nízkým onkogenním potenciálem (low-risk HPV, LR HPV) a typy s vysokým onkogenním potenciálem (high-risk HPV, HR HPV).
Drobnými poraněními v epitelu dochází k proniknutí virů až na úroveň bazální membrány a následně ke vstupu do hostitelských buněk. Při infekci kožního epitelu nastává diferenciace napadených buněk na keratinocyty, nicméně genom viru zůstává v buňce v epizomální formě. U infekcí slizničního epitelu dochází v místě infekce k vývoji lézí. V tomto případě může dojít k integraci virového genomu do genomu hostitelské buňky a tím k aktivaci exprese virových onkogenů E6 a E7, což může vést ve svém konečném důsledku k maligní transformaci buňky.
V závislosti na typu HPV může dojít k vývoji dysplazií či benigních genitálních bradavic. Díky aktivní imunitní odpovědi dojde u zhruba 70 % žen s incidentní HPV infekcí k potlačení infekce a spontánnímu vyléčení během jednoho roku. Infekce HR HPV mohou naopak během několika měsíců vést k rozvoji závažné dysplazie, nicméně progrese k prekancerózním lézím se objevuje pouze u případů s dlouho přetrvávající infekcí. Invazivně rostoucí nádory většinou nastupují po dlouhé prekancerózní fázi.
Epidemiologie HPV
HPV jsou považovány za původce některých nádorů, a to jak benigních, tak i maligních. Zároveň jsou pokládány za nejčastější virovou sexuálně přenosnou infekci (STI). S tím souvisí skutečnost, že celoživotní riziko infekce HPV se pohybuje okolo 80 %. Celkové odhady hovoří kupříkladu o 300 milionech žen, které jsou ročně infikovány HPV. Většina těchto genitálních infekcí je tranzientní, zůstává bez příznaků, a tudíž neodhalena. Je to nejpravděpodobněji způsobeno aktivací buněčné imunitní odpovědi v postižené tkáni. Pouze u 10 % infikovaných žen se vyvine chronická, perzistující infekce cervixu, což je hlavní podmínka pro možný vznik high-grade dysplastických změn a karcinomu.
Ačkoli je většina HPV infekcí benigních, odhaduje se, že infekce určitými typy HPV jsou ročně celosvětově zodpovědné za zhruba 610 000 nádorových onemocnění. Největší podíl na tomto počtu má cervikální karcinom, jímž dle odhadů onemocní každoročně 530 000 žen a 265 000 jich zemře 5. V zemích Evropské unie pak představuje cervikální karcinom 57 000 případů ročně a 25 000 úmrtí na tuto diagnózu.
Infekce LR HPV
Skupina LR HPV je odpovědná za vznik řady onemocnění pokožky, jednak ve formě klasických bradavic rukou a nohou, jednak tzv. genitálních bradavic, ale vzácně i orálních a laryngeálních papilomatóz, včetně rekurentní respirační papilomatózy a velmi vzácné fokální epiteliální hyperplazie.
Genitální bradavice, tzv. condylomata acuminata, jsou nejčastěji se vyskytujícím následkem infekce (LR) HPV. Jsou lokalizovány v dolním genitálním traktu, perianální oblasti a análním kanálu. Toto onemocnění je způsobeno ve více než 90 % případů LR typy HPV6 a HPV11. Jsou vysoce infekčními nezhoubnými nádory
s výskytem u obou pohlaví. Léčba je obtížná, založená na odstranění všech viditelných lézí pomocí různých metod, případně kombinovaná s aplikací specifických léčiv. Nejspolehlivější prevencí je profylaktická vakcinace proti výše uvedeným LR HPV typům.
Rekurentní respirační papilomatóza (RRP) je nejčastější benigní, často multifokální neoplazie hrtanu a průdušnice. Navzdory zařazení mezi benigní tumory je RRP sice relativně vzácným, ale nicméně život ohrožujícím onemocněním, způsobeným infekcí LR HPV6 a HPV11. Je charakterizováno růstem obvykle květákovitě utvářených lézí v dýchacím traktu, což může vést až k obstrukci dýchacích cest. Léčba je založena na chirurgickém odstranění lézí. Někteří pacienti z důvodu agresivní RRP musí během života podstoupit více než 40 operací. Existuje sice několik preparátů, které jsou podávány v rámci adjuvantní terapie, nicméně ani jeden z nich nevede k úplné eradikaci HPV infekce.
Infekce HR HPV
Naopak skupina HR HPV je v současnosti prokázaným původcem cervikálního karcinomu a dále nádorů vaginálních, vulvárních, penilních, análních a v neposlední řadě nádorů orofaryngeálních. Podrobněji je dále v textu popsán cervikální a orofaryngeální karcinom.
Cervikální karcinom
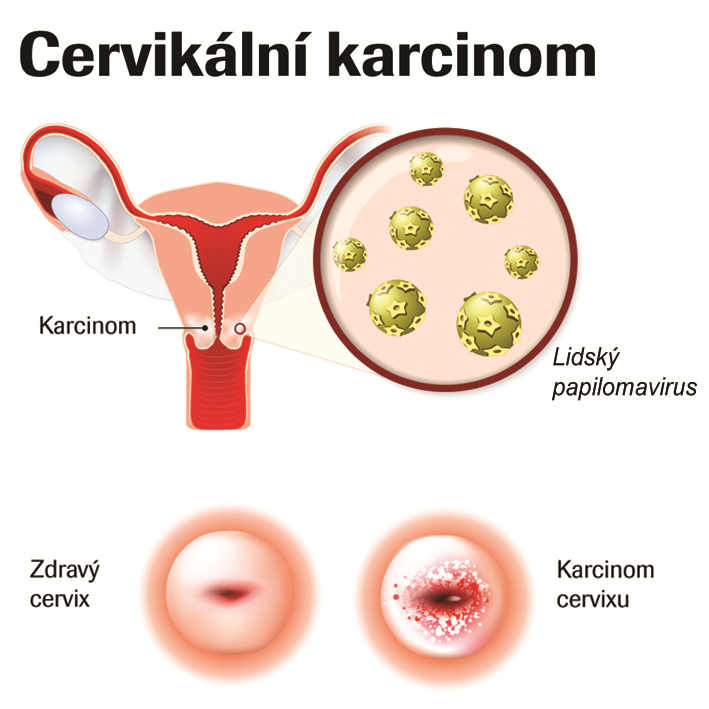
Největší podíl na celkovém počtu nádorových onemocnění způsobených HPV infekcemi má cervikální karcinom, jímž dle odhadů onemocní každoročně 530 000 žen a 265 000 jich zemře 5. V zemích Evropské unie pak představuje cervikální karcinom 57 000 případů ročně a 25 000 úmrtí na tuto diagnózu.
Cervikální karcinom (CxCa) je druhým nejčastějším nádorem u žen ve věkové skupině 15–44 let. V celkové populaci žen se řadí na čtvrté místo 5. Co se týče jeho výskytu v ČR, situace je dlouhodobě nepříznivá – téměř 900 případů výskytu a okolo 400 úmrtí ročně nás řadí (po přepočtu na počet obyvatel) v rámci evropských zemí zhruba do druhé třetiny, a to mezi Rusko a Bosnu a Hercegovinu. Ve srovnání s vyspělými zeměmi západního světa je tak u nás incidence a mortalita tohoto onemocnění stále velmi vysoká.
Téměř u 100 % CxCa byla prokázána přítomnost HR HPV typů, které jsou dle Mezinárodní agentury pro výzkum rakoviny (IARC) prokázaným původcem těchto nádorů 6. Vždyť jen typy HR HPV16 a HPV18 jsou zodpovědné za více než 70 % případů CxCa. Perzistující infekce těmito HR HPV typy může vést k integraci virových onkogenů E6 a E7 do hostitelského genomu a tím k aktivaci kontinuální exprese virových onkoproteinů E6 a E7, které inaktivují tumorsupresorové proteiny p53 a pRb. Tyto změny jsou spolu se somatickými mutacemi, které umožňují nekontrolovatelný růst, invazi, angiogenezi a další procesy, podstatou a základními podmínkami pro vývoj zhoubného nádoru, jímž cervikální karcinom bezesporu je.
Nejčastějším způsobem přenosu genitální HPV infekce je pohlavní styk. Byly popsány i jiné způsoby přenosu, jako je perinatální, orální či pomocí prstů a hygienických potřeb. Mezi rizikové faktory dále patří časný vstup do sexuálního života a vyšší počet sexuálních partnerů. Faktory jako imunosuprese, HIV infekce, kouření, sexuální promiskuita či dlouhodobé užívání orálních kontraceptiv zvyšují riziko rozvoje HPV infekce směrem k cervikálnímu karcinomu.
Léčba tohoto závažného onemocnění závisí na stadiu nemoci, jejím rozsahu a postižení přilehlých uzlin a orgánů. Zahrnuje chirurgické zákroky, radio- či chemoterapii a další léčebné postupy. Základním problémem tohoto onemocnění je skutečnost, že raná stadia cervikálního karcinomu jsou bezpříznaková. Přitom
v případě časného záchytu cervikálního karcinomu je hodnota 5letého přežívání mezi 100–80 % u stadia I, zatímco s rostoucím stadiem onemocnění se doba 5letého přežívání významně snižuje 7. Z tohoto důvodu se výrazně zvyšuje význam profylaktické vakcinace.

Orofaryngeální karcinom
V zemích rozvinuté části světa tvoří nádory hlavy a krku (HNSCC) okolo 5 % všech nádorů. Ačkoli incidence výše uvedených nádorů, asociovaných s konzumací alkoholu a tabáku, v rozvinutých zemích dosti významně poklesla, incidence orofaryngeálního karcinomu (OPC) roste. V některých zemích je nárůst incidence za posledních 30 let i šestinásobný. V roce 2008 byl výskyt nádorů ústní dutiny a OPC odhadován celosvětově na 400 000 případů a 223 000 úmrtí 8. V České republice bylo v roce 2015 zaznamenáno 94 případů výskytu OPC a 61 úmrtí na tuto diagnózu 9. HPV infekce se podílí na OPC zhruba 20 %. Dalšími etiologickými faktory jsou užívání alkoholu a tabáku, kouření marihuany a další virové infekce, jako je infekce herpes simplex virem (HSV) či virem Epstein-Barrové (EBV). 90 % těchto nádorů představují spinocelulární karcinomy. Hlavní terapií je chirurgická léčba a radioterapie, v pozdních stadiích chemoterapie. Doba 5letého přežívání je 90–75 % u I. stadia, zatímco ve IV. stadiu mezi 30–10 %.
Laboratorní detekce HR HPV infekcí
V současnosti probíhající cervikovaginální screening v ČR využívá v první řadě gynekologické cytologie, která se vyznačuje vysokou specificitou, ale nedosahuje požadované senzitivity. Tuto nevýhodu překonávají molekulárně biologické metody detekce HR HPV, využívající například technologie přímé hybridizace virové DNA s RNA sondou nebo metody založené na technologiích PCR v reálném čase. Metody PCR v reálném čase přinášejí navíc i možnost genotypizace HR HPV, tudíž vypovídají nejen o tom, zda vzorek je nebo není pozitivní na přítomnost HR HPV, ale zároveň umožňují určit vybrané konkrétní typy HR HPV16 a HPV18, jejichž výskyt v premaligních lézích je spojován s nejzávažnější prognózou a nejvyšším rizikem maligní progrese. Tudíž detekce těchto konkrétních typů HR HPV dává lékařům možnost personalizace a optimalizace léčebných postupů při léčbě výše uvedených nádorů a jim předcházejících stadií.
V naší laboratoři jsme v průběhu více než deseti let vyšetřování cervikovaginálních stěrů na přítomnost HR HPV měli možnost testovat a využívat různé detekční systémy.
Počátky patřily „zlatému standardu“ testování HR HPV – systému Hybrid Capture® 2 spolu s testem hc2 High-Risk HPV DNA Test® společnosti Digene (nyní Qiagen). Jedná se o neamplifikační metodu (bez PCR amplifikace virové DNA) založenou na zesílení signálu pomocí přímé hybridizace virové DNA s RNA sondou
a chemiluminiscenční detekcí. Metoda neprovádí izolaci virové DNA a detekuje 13 HR HPV typů. Za nevýhodu lze považovat absenci interní kontroly, která by umožňovala ověřit adekvátnost odebraného vzorku, tj. dostatek buněčného materiálu ve zpracovávaném vzorku. Kit využívá pouze sady kalibrátorů pro ověření správného průběhu zpracování série vzorků. Taktéž základní test neumožňuje ani částečnou genotypizaci, tj. určení přítomnosti konkrétního HR HPV typu, pouze uvádí přítomnost či nepřítomnost HR HPV. Test je schválen jako CE-IVD a také americkou FDA jako US-IVD.
Mezi testy, které jsme v laboratoři vyzkoušeli a používáme je dodnes, patří Inno-LiPA® HPV Genotyping Extra II firmy Innogenetics (nyní Fujirebio). Na rozdíl od předchozího tento kit neslouží ke screeningovým účelům, používá se jako diagnostický nástroj pro genotypizaci 32 LR a HR HPV typů. Principem je izolace a PCR amplifikace virové DNA s následnou reverzní hybridizací na nitrocelulózovém stripu, který nese komplementární úseky DNA ke všem testovaným HPV typům. Test zahrnuje i interní kontrolu amplifikace a nese označení CE-IVD.

Další z technologií, se kterou jsme se v laboratoři setkali, byl systém Panther™ firmy Gen-Probe (nyní Hologic) s testem Aptima™ HPV16 18/45 Genotype Assay. Test je na rozdíl od předchozích zaměřen na detekci virové mRNA virových onkogenů E6 a E7, tudíž umožňuje stanovit jejich integraci do genomu hostitelské buňky a tím i riziko její maligní transformace. Test detekuje celkem 14 HR HPV typů včetně genotypizace HR HPV16 a HPV18/45 metodou Transcription Mediated Assay (TMA) a Hybridization Protection Assay (HPA) s využitím amplifikace mRNA. Test používá interní kontrolu amplifikace a je označen CE-IVD a US-IVD.
Jednou z technologií, které v současnosti máme k dispozici, je GeneXpert® firmy Cepheid s testem Xpert® HPV. Test je založen na automatizované izolaci a amplifikaci DNA metodou PCR v reálném čase, provádí genotypizaci HR HPV16 a HPV18/45 a detekuje celkem 14 HR HPV typů. Systém používá interní kontrolu amplifikace. Modularita systému umožňuje zpracování malého i většího počtu vzorků v samostatných modulech. Vyšetření jednoho vzorku tak trvá 60 minut. Nevýhodou systému je poměrně vysoká cena za vyšetření jednoho vzorku. Test je schválen jako CE-IVD.
Testem, který využíváme již několik let a který představuje hlavní metodu pro vyšetřování vzorků cervikálních stěrů na přítomnost HR HPV typů, je cobas® 4800 HPV Test společnosti Roche. Díky automatizaci s využitím systému cobas® 4800 je práce s tímto testem jednoduchá, rychlá a komfortní. V jednom běhu lze najednou analyzovat 22 vzorků a provést 2 kontroly. Výsledek těchto vyšetření je možné obdržet během 3,5 hodiny. Systém je založen na automatické izolaci virové DNA a přípravě reakční destičky v přístroji cobas® x 480 s následnou detekcí pomocí real-time PCR v přístroji cobas® z 480. Test provádí genotypizaci HR HPV16 a HR HPV18 a detekuje celkem 14 HR HPV typů. V rámci série 22 vzorků je zahrnuta i pozitivní a negativní kontrola. Test používá interní kontrolu pro ověření dostatečného množství virové DNA či její amplifikovatelnosti a je schválen jako CE-IVD a americkou FDA jako US-IVD. Navíc je cobas® 4800 HPV test jako jediný diagnostický test schválen (od září loňského roku) FDA pro HPV screening karcinomu děložního čípku bez doprovodné cytologie.
Komerčních testů a systémů používaných v rámci screeningu je celá řada, nicméně jejich správný výběr je důležitým krokem v procesu vyšetřování HPV infekce. Testy založené na detekci virové DNA, jako je cobas® 4800 HPV Test (Roche), umožňují detekovat tuto virovou DNA v kterékoli fázi HPV infekce, a to od samotného prvotního výskytu virového agens v lidském organismu přes období, kdy dochází k vývinu dysplastických změn, až po fázi rozvoje cervikálního karcinomu. Naopak systémy pracující na principu detekce mRNA (např. Aptima HPV mRNA Assay, Hologic) jsou schopné zachytit přítomnost HPV infekce teprve ve fázi, kdy se HPV inkorporuje do genomu hostitelské buňky a dochází k transkripci virových onkogenů E6/E7. Dřívější fáze infekce jsou tímto testem nezachytitelné. Ve zkratce lze říci, že DNA-based testy detekují HPV DNA od fáze akutní infekce přes fázi replikace viru, inkorporace do hostitelského genomu, onkologické transformace buněk až po fázi invazivního karcinomu, zatímco RNA-based testy dokážou detekovat mRNA viru teprve od fáze začlenění virové DNA do genomu hostitele.
Vakcinace
V neposlední řadě je nezbytné zmínit možnosti profylaktické vakcinace proti HPV infekci. Kvůli vysokému celoživotnímu riziku setkání s HPV infekcí (přičemž se toto riziko vzhledem k výše zmiňovaným 80 % jeví jako velice reálné) je jedinou účinnou prevencí proti infekci lidskými papilomaviry aplikace vakcín vyvinutých na ochranu před infekcí vybranými typy HPV. V současnosti jsou na trhu komerčně dostupné tři profylaktické vakcíny.
Víceméně zároveň byly na trh uvedeny dvě profylaktické vakcíny. První z nich je bivalentní vakcína Cervarix™ proti HR typům HPV16 a HPV18, zodpovědným zhruba za 70 % všech CxCa. Druhou z vakcín je tetravalentní vakcína Silgard® proti HPV16 a HPV18 a současně proti LR typům HPV6 a HPV11. Chrání tudíž nejen proti HR HPV typům, ale i proti dvěma LR HPV typům, zodpovědným především za výskyt genitálních bradavic. Poslední v řadě je od roku 2014 nonavalentní vakcína Gardasil®9, chránící proti 9 typům HPV: HR HPV16, HPV18, HPV31, HPV33, HPV45, HPV52, HPV58 a LR HPV6 a HPV11. Výrobce udává vysokou účinnost proti rozvoji CxCa, vaginálního, vulvárního a análního karcinomu a jim předcházejících lézí.
V souvislosti s objevem komerčně dostupných profylaktických vakcín se celosvětově vyvíjí rozsáhlé úsilí o jejich aplikaci v rámci národních vakcinačních programů. V některých zemích, jako je například Austrálie, mají s tímto programem již téměř desetileté zkušenosti. V roce 2013 běžela vakcinace proti HPV již ve 45 zemích světa a v dalších 4 se připravovala 10.
V České republice také existuje národní vakcinační program proti HPV. Započat byl roku 2012 a je určen pro třináctileté dívky (od roku 2018 i pro chlapce), u nichž se předpokládá, že se dosud s HPV infekcí nesetkaly. Účast v tomto programu je dobrovolná a je zdarma. Náklady spojené s vakcínou a její aplikací jsou hrazeny z prostředků veřejného zdravotního pojištění.
Závěr
HPV infekce provázejí člověka celou jeho existencí. Ačkoli je většina těchto infekcí dočasná, přetrvávající onemocnění HR HPV může být impulzem k rozvoji prekancerózních lézí a v nejzávažnějších případech i příčinou vzniku nádorového onemocnění. Z tohoto důvodu je nezbytná přesná a dostupná diagnostika těchto infekcí. Pro výběr adekvátní vyšetřovací technologie je nejlepší zvolit si metodu prověřenou jak časem a velkým počtem spokojených uživatelů, tak i řádně validovanou a podloženou dostatkem klinických studií. Při hledání takové technologie může pomoci poznatek, že jde o metodu schválenou nejen jako CE-IVD, tj. in vitro diagnostiku vyhovující harmonizovaným evropským normám, ale také schválenou americkou FDA (U.S. Food & Drug Administration) jako US-IVD. Počet těchto metod není velký, ale cobas® 4800 HPV Test (Roche) spolu s automaty pro jeho použití cobas® z 480 a cobas® x 480 mezi ně rozhodně a zcela oprávněně patří.