Na panelu pozitivních vzorků jsme testovali různé soupravy a popisujeme je hlavně z hlediska citlivosti a dále z pohledu hodnotícího vývoje odpovědi v čase. Nově máme zařazeno i testování prvních dvou dostupných automatických metod. Vedle toho jsme ověřili citlivost jedné soupravy chromatografické, za ideálních podmínek v laboratoři. Po diskusi nastiňujeme diagnostické schéma sérologických testů, které doplní přímý průkaz v dalším vývoji epidemie COVID-19. Práce obsahuje i souhrn nabízených sérologických metod.
Úvod
Základní metodou diagnostiky onemocnění COVID-19 je přímý průkaz virové RNA. Pro množství případů a vzniklých otázek vyvstává potřeba principiálně jiného vyšetření. Na počátku letošní epidemie jsme zkusmo objednali řadu souprav, které byly chvatně vyvíjeny a často k nim chyběly údaje o specifitě a citlivosti. Také v literatuře se píše1 o chybějícím dozoru FDA. Řada těchto objednávek nakonec nebyla realizována, naopak do zdravotnictví bylo „vrženo“ velké množství imunochromatografických rychlých testů. V této situaci se v naší spádové oblasti objevila dvě dobře popsaná ohniska a řada sporadických případů, čímž vznikl panel pozitivních vzorků, na kterém jsme přezkoušeli i soupravy, které se na trhu objevily později. Studie je zaměřena na citlivost vzhledem k záchytu nových případů či celých ohnisek.
Principiální základy sérologických testů
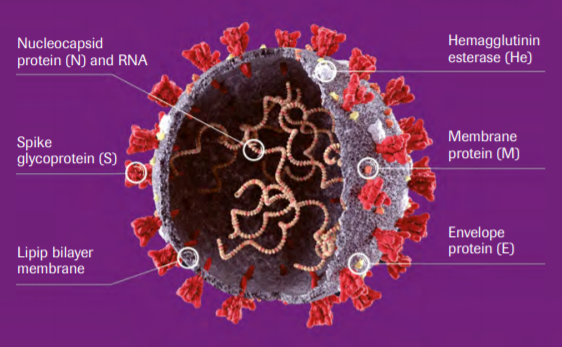
Antigenní skladba viru SARS-CoV-2 sestává z antigenu hrotového (spike – S), obálkového (envelope – E), matrixového (M) a nukleokapsidového (N) Zjišťované protilátky mohou být třídy IgG, IgA, IgM nebo celkové (total). Metodicky jde o testy enzymatické (ELISA), chromatografické (rapid) a chemiluminiscenční (CMIA, CLIA).
Použité soupravy
• Generic Assays GA COV-2 IgG, sendvičová ELISA, použitý antigen neuveden. Výrobce udává specifitu nad 95 %. Poznámka: U malého počtu „normální“ populace byly nalezeny protilátky proti nukleokapsidovému antigenu.
• Generic Assays GA COV-2 IgM, sendvičová ELISA, použitý antigen neuveden. Specifita nad 98 %, citlivost 98 %. Stejná poznámka jako u IgG.
• Generic Assays GA COV-2 IgG plus, sendvičová ELISA, profil protilátek proti antigenům S1, S2 a N. Ve studii nebylo testováno.

• EDI Novel Coronavirus COVID-19 IgM ELISA kit firmy Epitope Diagnostics, inc. ELISA capture, použitý antigen neuveden („rekombinantní“). Citlivost ani specifita nejsou uvedeny. • EDI Novel Coronavirus COVID-19 IgG ELISA kit. Sendvičová ELISA, nukleokapsidový antigen. Uvedena citlivost i specifita 100 % na kohortách 30 a 54 vzorků.
• Anti-SARS-CoV-2 ELISA IgA a IgG firmy Euroimmun. Sendvičová ELISA, rekombinantní antigen S1. Specifita IgA na panelu 200 sér 92,5 %, na panelu zdravých dárců 10–12,7 % nespecifických reaktivit IgA, specifita IgG na panelu 200 sér 98,5 %. Citlivost kombinace IgG + IgA (9 vzorků) do 10 dnů od nástupu příznaků 66,7 %, nad 10 dnů 100 %.
• SARS-COV-2 IgG Architect Abbott. CMIA, antigen neuveden. Citlivost i specifita v příbalové informaci rovněž chybí.
• Elecsys Anti-SARS-CoV-2 cobas® Roche, dvojantigenová ECLIA, rekombinantní nukleokapsidový antigen, stanovuje principiálně celkové protilátky. Udávaná specifičnost 99,81 % (5 272 vzorků), citlivost do týdne po prvním pozitivním PCR je 65,5 %, 7–13 dnů 88,1 % a nad 14 dnů 100 %.
• Souprava SARS-CoV-2 (COVID-19) IgG/IgA/IgM Novalisa (sendvičová ELISA, nukleokapsidový antigen) od Novatecu byla použita s dobrým výsledkem, ale před sestavením panelu, proto v přehledu není uvedena. Naopak soupravy SARS-CoV-2 IgG/ IgA/IgM Test Line nám byly dodány až po vyčerpání panelu.
• 2019-nCOV Ab Test (colloidal gold) IgG/IgM Innovita, Qian an, China – chromatografický test. Antigen neuveden („rekombinantní“). Provedeno v laboratoři ze separovaného séra, hodnocení vždy třemi pracovníky, jako pozitivní označena jejich shoda, jinak uzavřeno jako sporné. PCR bylo provedeno v laboratoři FN HK, údaj vztahujeme vždy k časově nejbližšímu odběru séra. Všechny testy byly provedeny podle postupů a podmínek stanovených výrobci.
Výsledky
Panel sér
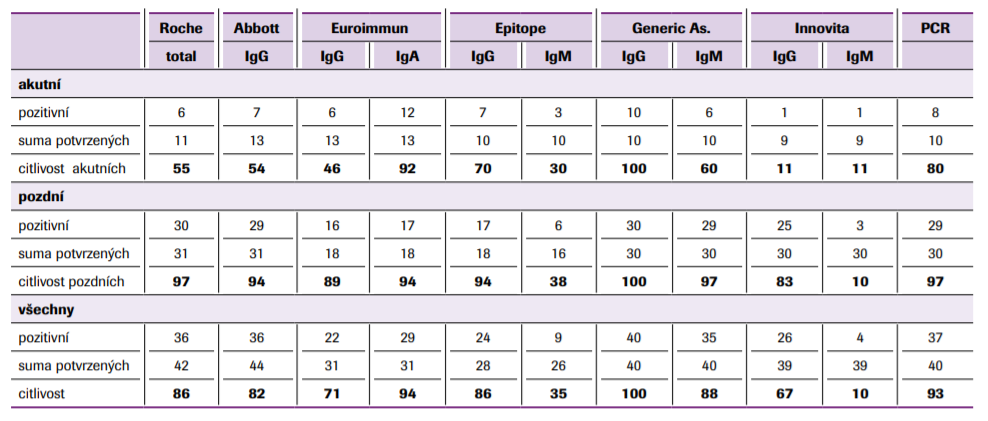
Bylo vybráno 43 vzorků. 17 vzorků bylo od mužů, 26 od žen, průměrný věk byl 75 let (23–93), což bylo dáno převažujícím zastoupením klientů domova pro seniory. 33 vzorků bylo od pacientů s dobře doloženou diagnózou (PCR + epidemiologická souvislost + klinika). Z toho 4 pacienti měli těžký průběh s nutnou hospitalizací, 2 z nich zemřeli. Bez příznaků, ale pozitivní PCR a epidemiologickou souvislost vykazovalo 5 pacientů (od nich v souboru 8 vzorků). Jeden pacient, který vyhovoval epidemiologicky a klinicky, ovšem s negativním PCR, reagoval přítomností protilátek, ale nebyl dále přímými metodami testován. Od 15 pacientů byly získány nejméně dva vzorky pro zachycení dynamiky. Počátek infekce byl stanoven na den hospitalizace u těžkých pacientů, vzestup teploty u nehospitalizovaných pacientů a předpokládané datum nakažení s odhadem inkubační doby plynoucí z epidemiologie u bezpříznakových případů. V informacích výrobců se opakuje hodnocení stavu do 7–14 dnů od počátku příznaků jako akutní skupina, která se zřetelně odlišuje od pozdějších vzorků. V našem souboru jsme viděli výrazně oddělenou skupinu do 11 dnů (12 vzorků, 0–11 dnů, průměr 7,2), kterou jsme označili jako akutní, později odebrané vzorky jsou ve skupině pozdní (31 vzorků, 15–57 dnů, průměr 33 dnů).
Diskuse
Dynamika protilátek se liší jak podle imunoglobulinových tříd, tak podle užitého antigenu. Uváděný vrchol koncentrace protilátek IgM je v druhém týdnu po objevení příznaků, IgG protilátek ve třetím. O průběhu odpovědi IgA se zprávy liší, nicméně počátek produkce v prvním týdnu by se měl shodovat s IgM. Sledování dynamiky by mělo pomoci v prognóze.1
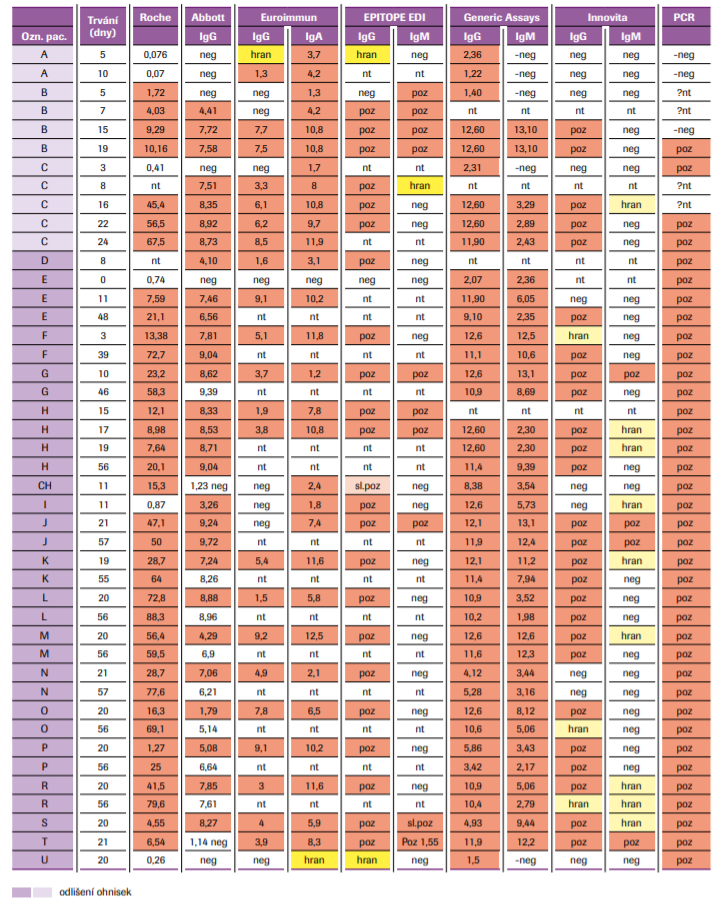
Naše nálezy se od literatury (zejména firemní) v něčem dosti liší. Citlivost souprav je celkem srovnatelná a při doporučeném opakování odběru by neměla mít mnoho uniklých případů. Složitější je to při odhadu délky trvání infekce. IgM soupravy GA přetrvávalo značně, s vysokými titry i po padesáti dnech. Naproti tomu u akutních vzorků mělo menší citlivost než Epitope. Epitope IgM v čase dobře klesalo, bylo pozitivní nejdéle 21 dnů. Souprava IgA Euroimmun zachycovala pozitivity velmi časné, prakticky zároveň s přímým průkazem, ale vzhledem k delšímu trvání odpovědi IgA (ve shodě s literaturou) nezobrazila zřetelně pokles u pozdních vzorků a nepomohlo ani sledování semikvantitativní dynamiky. Stanovení celkových protilátek metodou Elecsys Roche mělo dobrou citlivost a jeho dynamika odrážela velmi dobře postup odpovědi v čase – zde je výhodou větší rozsah měření ECLIA proti ELISE. Podobně provozně výhodný automatický test Abbott Architect byl dostupný pouze ve třídě IgG a výmluvné hodnocení by žádalo i některý z akutních markerů. Zkoumané rapid-testy ukazují mizivou citlivost v akutní fázi. U pozdních sér mělo IgG s tolerancí použitelnou citlivost IgG, za předpokladu provedení ze séra. IgM reagovalo i v optimálních podmínkách provedení špatně. Sloupec PCR odráží ve shodě s literaturou2 fakt, že ani PCR není stoprocentně citlivé – zde hraje roli hlavně provedení odběru. Přetrvávání pozitivity PCR po klinické úzdravě přesahuje zaměření této práce. Pro úplnost sdělení mimo referovaná data: interpretovat izolované reaktivity IgA negativní v PCR, které jsme pozorovali my i jihočeská studie,2 je poměrně těžké. Bude nutné sledování v delším čase, užití virus neutralizačního testu (VNT) a dalších postupů. Stejně nerozřešeným problémem je spolehlivé stanovení protektivity. Ověření specifity jednotlivých testů bude vyžadovat větší soubor negativních vzorků.
Praktické dopady
Laboratoře, které se sérologií CoV-2 zabývají, mají různý přístup. Jihočeská studie byla provedena na soupravách IgG/IgA firmy Euroimmun, obdobně virologie ZÚ Ostrava má tyto soupravy jako základ a doplňuje je soupravou IgM Epitope (osobní sdělení), ovšem zásadní silnou zbraní této laboratoře je VNT, který rutinní laboratoř nemá. VNT pravděpodobně řeší i problém protektivity.
Zkušenosti s automatickými metodami jsme v dostupných zdrojích dosud nenašli. Shrnutí našich praktických poznatků nám umožňuje sestavit kombinaci testů pro různé účely stanovení protilátek při onemocnění COVID-19 a případných kontaktech a suspekcích.
Jednotestové, dosti citlivé stanovení celkových protilátek doplňujeme při nalezené reaktivitě panelem IgG/IgA/IgM: nejcitlivější IgA pro záchyt akutních, IgM se zřetelným poklesem titru v čase (soupravy s přetrváváním IgM nebudou specifické). V rozhodování bude hrát roli i cena. Opakování testu s rekonvalescentními séry zvýší citlivost a zachytí i sérokonverzi. Závěr Zkoušené soupravy ELISA i chemiluminiscenční vykazovaly v praxi použitelnou citlivost. Jedna ze souprav IgM vykazovala nižší citlivost v akutní fázi a naopak prodlouženou reaktivitu proti srovnatelnému testu konkurenčnímu. Rapid-testy byly málo citlivé v akutní fázi a později reagovaly prakticky jen v IgG.
Konflikt
Pro dané sledování jsme vešli ve spolupráci se všemi dodavateli diagnostiky uvedenými v práci, kromě toho jsme zkoušeli soupravy Novatec a Test Line, z technických důvodů na jiných vzorcích. Firmám Vidia, Dynex a Test Line jsme poskytli pozitivní séra. Firmy Roche a Test Line daly ke zkoušení soupravy zdarma.