Test cobas® CMV na systému cobas® 4800 je navržen pro efektivní poskytování standardizovaných, klinicky ověřených výsledků. Jedná se o in vitro amplifikační test nukleové kyseliny pro kvantitativní měření DNA cytomegaloviru (CMV) v lidské EDTA plazmě. Je určen k použití jako pomůcka pro diagnózu a léčbu CMV u pacientů s transplantací orgánů a u pacientů s transplantací hematopoetických kmenových buněk. U těchto populací lze tímto testem stanovit, zda je potřeba zahájit antivirovou léčbu. U pacientů na anti-CMV terapii je možné sériová měření DNA použít ke stanovení virové odpovědi na léčbu. Výsledky testu cobas® CMV je třeba interpretovat v kontextu všech relevantních klinických a laboratorních nálezů.6
Cytomegalovirus (CMV) je běžný virus nalezený u lidí všech věkových kategorií, přičemž více než polovina všech dospělých byla nakažena do 40. roku věku.1 CMV přetrvává latentně po celý život a může být reaktivován. I když virus obecně nezpůsobuje problémy osobám se zdravým, fungujícím imunitním systémem, může mít závažné následky pro lidi s oslabeným imunitním systémem.
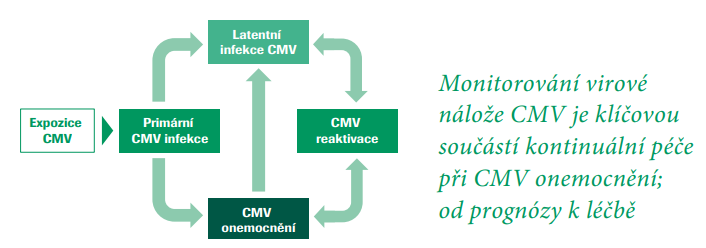
IInfekce CMV je hlavní příčinou morbidity a mortality u pacientů po transplantaci. Kalibrace a hlášení virové zátěže CMV DNA v mezinárodních jednotkách na mililitr (IU/ml) zlepšilo harmonizaci výsledků z různých laboratoří. Řízení aktivní infekce CMV je však stále omezováno nedostatečnou komutabilitou výsledků mezi referenčními materiály a klinickými vzorky a následným nedostatkem prahových hodnot virové zátěže založených na důkazech. Komutabilita je schopnost referenčního materiálu (kalibrátoru, kontrolního materiálu) vykazovat při měření a při hodnocení kvality stejné chování jako analytické vzorky. Nedostatek komutability vede k chybným výsledkům měření a k chybným závěrům o kvalitě analytické činnosti.
Současné laboratorně vyvinuté metody kvantifikace CMV DNA jsou omezeny nedostatkem standardizovaných výsledků, což může vést k vysoké variabilitě mezi jednotlivými laboratořemi a testy. Laboratorní metody diagnózy u lidského CMV zahrnují izolaci viru kultivací z periferních krevních leukocytů (PBL), histologii biopsií, sérologická vyšetření, měření hodnot antigenu pp65 v krvi a detekci CMV DNA pomocí polymerázové řetězové reakce (PCR). Sérologie má význam pouze pro zjištění, zda byl pacient dříve infikován CMV a podléhá riziku reaktivace. Metody založené na kultivaci mají nízkou prediktivní hodnotu, doba jejich provedení přesahuje 48 hodin a mají omezené použití zvláště u imunokompromitovaných pacientů. Test antigenu pp65 v krvi je pracný a kvůli snižování hladiny antigenu v krvi při skladování vyžaduje zpracování krve do šesti hodin od odběru. Test pp65 lze také obtížně provádět u pacientů s neutropenií. Přímá detekce CMV DNA, např. metodami PCR v reálném čase, potenciálně nabízí široký dynamický rozsah, přesnost a vysokou citlivost. U přibližně 20–60 % příjemců transplantací orgánů se rozvine symptomatická infekce CMV, obvykle během prvních několika měsíců po transplantaci.2 Pacienti mohou být infikováni dárcovským orgánem nebo může být virus reaktivován, pokud byl dříve přítomen. Reaktivaci CMV po transplantaci lze rychle detekovat a léčit pomocí antivirotik. Pokud jde o úspěšné zvládání infekce a možnost pacientů po transplantaci prožít dlouhodobý, zdravý život, hraje zásadní roli spolehlivost výsledků testů.

Test cobas® CMV umožňuje detekci a kvantifikaci CMV DNA, který se shoduje s 1. mezinárodním standardem WHO pro lidský CMV v EDTA plazmě infikovaných pacientů.5 Virová nálož je kvantifikována pomocí kvantifikačního standardu DNA (DNA QS) jiného původu, než je CMV, který je do každého vzorku přidán během přípravy. Standard DNA QS slouží také k monitorování celého procesu přípravy vzorku a PCR amplifikace. Test navíc využívá tři externí kontroly: pozitivní kontrolu s vysokým titrem, pozitivní kontrolu s nízkým titrem a negativní kontrolu.6
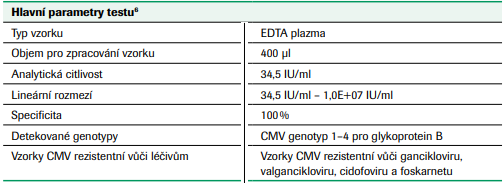
Test cobas® CMV se zakládá na plně automatizované přípravě vzorků (extrakce a purifikace nukleové kyseliny) s následnou PCR amplifikací a detekcí. Systém cobas® 4800 sestává z přístroje cobas x 480 a analyzátoru cobas z 480. Software systému cobas® 4800 provádí automatizované zpracování dat, při kterém přiřazuje kategorii „Target not detected“ (cílová sekvence nedetekována) výsledkům < LLoQ, below lower limit of quantitation (pod dolní mezí kvantifikace), nebo > ULoQ, above upper limit of quantitation (nad horní mezí kvantifikace); anebo kategorii „CMV DNA detected“ (detekována DNA viru CMV) s hodnotou v lineárním rozmezí LLoQ ≤ x ≤ ULoQ. Výsledky lze prohlížet přímo na obrazovce systému, exportovat nebo vytisknout jako zprávu.6 Výsledky jsou v IU/ml, což je v souladu s doporučeními pro optimalizaci řízení CMV. Systém zjednodušuje a standardizuje operace s minimálními zásahy uživatele a prodlouženou dobou bez nutnosti zásahu až na 3 hodiny, s WHO kalibrovanými reagenciemi připravenými k okamžitému použití. V laboratoři není nutné provádět žádné kalibrace ani rozpouštění reagencií a kontrol.3,4 Výsledky jsou k dispozici za 4 hodiny a 20 minut. Krev se odebírá do zkumavek pro přípravu plazmy BD Vacutainer® PPTTM nebo zkumavek s víčky levandulové barvy pro molekulární diagnostické testovací metody nebo do sterilních zkumavek za použití EDTA jako antikoagulantu. Objem pro zpracování vzorku systémem cobas® CMV je pouze 400 μl. Mez detekce (Limit of detection, LoD) testu cobas® CMV pro EDTA plazmu je 34,5 IU/ml, lineární rozmezí testu cobas® CMV je 34,5 až 1,0 E+07 IU/ml.
Účinnost testu cobas® CMV u různých genotypů CMV byla vyhodnocena pomocí:
- Verifikace meze detekce u genotypů 2 až 4 pro glykoprotein B
- Verifikace lineárního rozmezí u genotypů 2 až 4
Výsledky ověřily, že test cobas® CMV detekoval CMV DNA pro tři různé genotypy při koncentraci 34,5 IU/ml s úspěšností detekce ≥ 95 %.
Účinnost testu cobas® CMV u vzorků CMV rezistentních vůči léčivům byla vyhodnocena pomocí:
- Verifikace meze detekce u vzorků CMV rezistentních vůči léčivům (rezistence vůči gancikloviru, valgancikloviru, cidofoviru nebo foskarnetu)
- Verifikace lineárního rozmezí u vzorků CMV rezistentních vůči léčivům (rezistence vůči gancikloviru, valgancikloviru, cidofoviru nebo foskarnetu)
Test cobas® CMV detekoval DNA CMV pro všechny testované vzorky rezistentní na běžné léky na CMV při koncentracích 34,5 IU/ml s úspěšností detekce ≥ 95 %.
Společnost Roche je odhodlána pomáhat zabránit šíření a reaktivaci cytomegaloviru a poskytuje standardizované testy podle doporučení WHO pro detekci a monitorování progrese CMV infekcí. Test cobas® CMV přináší transplantační komunitě standardizaci při testování a výdeji výsledků pro optimální řízení CMV infekce. Vede laboratoře ke standardizovanému použití typu vzorku (plazma) a vykazování výsledků v IU/ml. Jedná se o první komerční test standardizovaný podle mezinárodního standardu WHO, s certifikátem CE i FDA. Nabízí alternativu k laboratorně vyvinutým testům (LDT) se sníženou pracností a bez rizika nesprávných výsledků.