Vírusová hepatitída B (VHB) je infekčné ochorenie pečene. Prenáša sa krvou a telesnými tekutinami. Svetová zdravotnícka organizácia (WHO) eviduje celosvetovo viac ako 250 miliónov pacientov s vírusovou hepatitídou B. Na komplikácie ročne umiera viac ako 800 000 pacientov napriek tomu, že hepatitída B je ochorenie preventabilné očkovaním 1 .
Vírus hepatitídy B
VHB spôsobuje vírus hepatitídy B patriaci do čeľade Hepadnaviridae, rodu Orthohepadnavirus. Ide o obalený, parciálne dvojvláknový DNA vírus, ktorý na replikáciu využíva reverznú transkriptázu. Rozlišujeme 3 typy vírusových častíc a to Daneovu časticu, ktorá je infekčná, a neinfekčné cirkulárne a fi lamentózne častice. Genóm vírusu je tvorený 3 200 pármi báz a je najmenší z ľudských DNA vírusov. Mínus vlákno tvorí takmer úplný kruh, na 5´ konci s pripojenou reverznou transkriptázou. Plus vlákno je neúplné a je zakončené krátkym úsekom RNA. Genóm hepadnavírusov je usporiadaný veľmi úsporne, jeho jednotlivé ORFs (Open Reading Frames) pre P, S, C a X gén sa prekrývajú, resp. sa prepisujú z oboch vlákien DNA. Rozlišujeme 10 genotypov hepatitídy B (A-J), u nás sa vyskytuje najčastejšie genotyp A 2,3 .
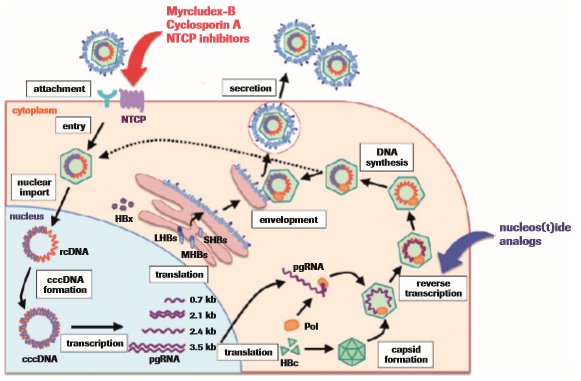
Vírus hepatitídy B má výraznú afi nitu k hepatocytom. Viaže sa prostredníctvom L glykoproteínu HBsAg na receptor NTCP (Na+ taurocholate cotransporting polypeptid). V cytoplasme stráca obaly a preniká do jadra. Tu je dokončená syntéza plus vlákna a vzniká kovalentne uzavretá cirkulárna DNA (ccc DNA). Prostredníctvom nej perzistuje vírus trvalo v bunke a v podstate bráni úplnej eradikácii. V jadre sa cccDNA prepisuje na subgenómové mRNA (sgRNA) pre transláciu proteínov S, M a L tvoriace HBsAg a pregenómovú mRNA (pgRNA). Pregenómová mRNA je templátom pre syntézu novej vírusovej DNA. Zostrihom pgRNA vznikajú molekuly mRNA pre proteíny P a C, ktoré sa stávajú súčasťou jadra nového viriónu. Obaľovanie nových častíc sa uskutočňuje na membránach vezikúl endoplazmatického retikula. Súčasťou obalu sa stávajú glykoproteíny S, M aj L syntetizované prepisom sg RNA. L glykoproteín je súčasťou len Daneovej častice. S a M glykoproteíny, ktoré sú produkované v nadbytku, sa uvoľňujú z hepatocytu do krvného obehu aj samostatne ako solubilný HBsAg a tvoria cirkulárne a filamentózne častice. Transkripcia sgRNA a pgRNA sú procesy riadené odlišnými, od seba nezávislými promotormi a sú na sebe nezávislé 2,3 .
Diagnostika VHB
Diagnóza vírusovej hepatitídy B sa stanovuje na základe vyšetrenia markerov VHB. Patrí sem stanovenie povrchového HBsAg a anti HBc. Negativita oboch parametrov vylučuje prebiehajúcu infekciu s výnimkou inkubačnej doby. V prípade pozitivity HBsAg je možné kvantitatívne stanovenie HBsAg. Kvantita HBsAg sa udáva v IU/ml. Bežne sa stanovujú aj ďalšie markery a to HBeAg, anti HBe, anti HBs a anti HBc IgM. Podľa výsledkov všetkých markerov vieme s veľkou pravdepodobnosťou stanoviť fázu VHB. V prípade pozitivity HBsAg alebo anti HBc máme k dispozícii stanovenie vírusovej nálože metódou HBV DNA RealTime PCR 4 .
Klinický priebeh
Hepatitída B prebieha ako akútna alebo chronická infekcia. O jej priebehu rozhoduje imunitný systém hostiteľského organizmu.
O akútnej infekcii hovoríme, ak prítomnosť HBsAg v sére netrvá viac ako 6 mesiacov a končí totálnou sérokonverziou, t.j. prítomnosťou protilátok proti antigénom HBs, HBe a HBc. Priebeh varíruje od asymptomatického po fulminantný.
Chronická vírusová hepatitída B je charakterizovaná prítomnosťou HBsAg v sére dlhšie ako 6 mesiacov. Môže progredovať do fibrózy, cirhózy až hepatocelulárneho karcinómu. Prebieha v niekoľkých fázach.
Prvá fáza, nazývaná imunotolerantná, je charakterizovaná vysokou vírusovou náložou v krvi, pozitivitou HBs antigénu a HBe antigénu. Keďže imunitný systém nereaguje na prítomnosť vírusu, nedochádza k poškodzovaniu hepatocytov, nezvyšuje sa ALT a na histologickej úrovni nie sú na pečeni prítomné známky inflamácie ani fibrotických zmien. V tejto fáze je pacient vysoko kontagiózny.
Po niekoľkých rokoch dochádza k prechodu do druhej fázy a to imunoreaktívnej. Postupne sa znižuje hladina HBV DNA aj hladina HBsAg, pretrváva pozitivita HBeAg. Nakoľko imunitný systém atakuje hepatocyty, dochádza ku zvýšeniu hladiny ALT. Histologicky pozorujeme inflamáciu heparu a pri hojení dochádza k vzniku fibrotických zmien. V dôsledku mutácie génu v pre-core oblasti vymizne HBe antigén a infekcia prechádza na HBeAg negatívnu CHB.
Po sérokonverzii na anti HBe, alebo po vymiznutí HBeAg nastáva fáza nosičstva HBsAg. Sérologickým vyšetrením základných markerov nie je vždy rozdiel medzi fázou inaktívneho nosičstva H BsAg a HBeAg negatívnej CHB. V prípade HBeAg negatívnej CHB sa jedná sa o aktívne ochorenie s postupnou progresiou do fibrózy, cirhózy, príp. hepatocelulárneho karcinómu.
Aj v prípade chronickej hepatitídy môže dôjsť k sérokonverzii na anti HBs, hladina protilátok býva v mnohých prípadoch nízka, pod detekčným limitom.
Terapia VHB
V terapii hepatitídy B sa používajú dva rôzne typy liekov. Prvým je pegylovaný interferón α (PEG-IFN α), druhým sú analógy nukleotidových/nukleozidových báz (NAs).
Výhodou liečby PEG-IFN α je skutočnosť, že nevzniká rezistencia a je možné dosiahnuť úplnú virologickú odpoveď. Nevýhodou je nutnosť parenterálneho podania a častý výskyt závažných nežiaducich účinkov, pre ktoré pacienti nie sú schopní pokračovať v terapii.
NAs blokujú syntézu HBV DNA v hepatocyte. V prípade terapie NAs sa nežiaduce účinky vyskytujú zriedka, ale môže sa objaviť rezistencia. Terapia NAs je dlhodobá, obvykle doživotná. O jej prípadnom prerušení rozhoduje viacero faktorov, napríklad viremická a biochemická aktivita ochorenia, štádium, ako aj pridružené ochorenia. Kontraindikáciou prerušenia terapie sú najmä ochorenia, ktoré vo svojom priebehu alebo počas terapie navodzujú stav imunodefi citu.
Rozhodnutie o začatí terapie vychádza z troch základných kritérií, a to: hladina HBV DNA v sére, hladina ALT a závažnosť poškodenia heparu. Cieľom terapie je virologická supresia, ktorá vedie k biochemickej remisii a histologickému zlepšeniu. Ako u HBeAg pozitívnych, tak aj u HBeAg negatívnych pacientov s chronickou hepatitídou B je ideálnym cieľom terapie vymiznutie HBsAg a to s následnou sérokonverziou na anti HBs, prípadne aj bez nej.
Monitoring priebehu terapie
U pacientov HBeAg pozitívnych na terapii PEG IFN α sa v 12., resp. 24. týždni terapie sleduje vírusová nálož. Pokles hladiny HBV DNA pod 20 000 IU/ml zvyšuje predpoklad sérokonverzie na anti HBe. Rovnako pokles HBsAg pod 1 500 IU/ml je silným prediktorom sérokonverzie HBeAg/anti HBe. Na druhej strane,
pravdepodobnosť dosiahnutia sérokonverzie sa znižuje v prípade, ak nedôjde k poklesu hladiny HBsAg pod 20 000 IU/ml 5 .
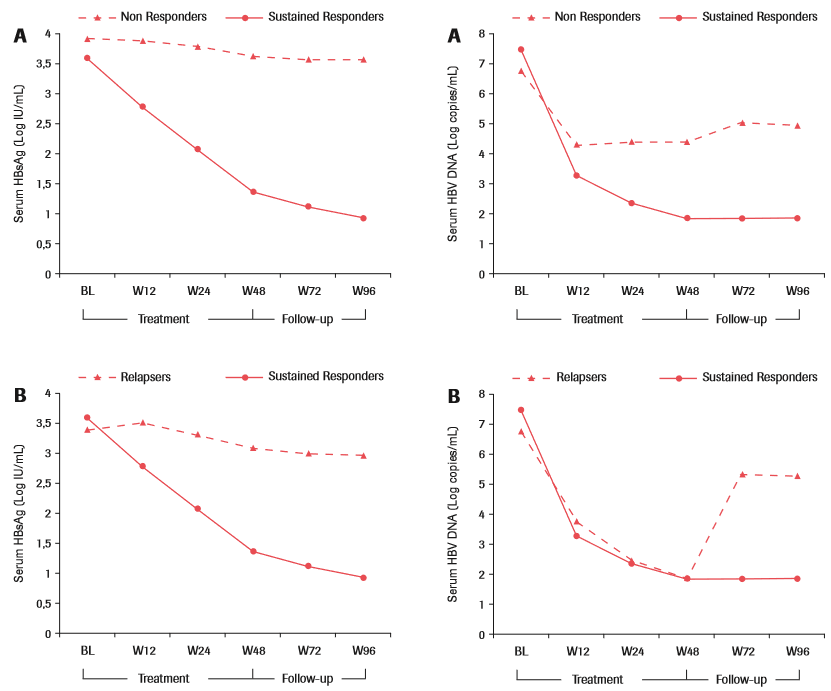
U pacientov HBeAg negatívnych na terapii PEG IFN α bolo pozorované, že rýchly pokles hladiny HBsAg v 12. týždni po začatí terapie je silným prediktorom trvalej vírusovej odpovede. K poklesu hladiny HBV DNA došlo po začatí terapie u respondérov, non respondérov aj relapsérov. Na druhej stane k signifi kantnému poklesu hladiny HBsAg v 12. týždni po začatí terapie došlo len u pacientov, ktorí dosiahli trvalú vírusovú odpoveď (Obr. 2).
U pacientov s terapiou NAs sa počas liečby sleduje vírusová nálož. V prípade HBeAg negatívnych aj reaktívnych pacientov platí, že nedetegovateľná hladina HBV DNA v 12. resp. 24. týždni terapie znižuje pravdepodobnosť vzniku rezistencie a predikuje trvalú vírusovú odpoveď 6 .
Výsledky
Naším cieľom bolo porovnanie výsledkov HBV DNA a kvantitatívneho HBsAg v sledovaní natívneho priebehu chronickej hepatitídy B a v sledovaní pacientov s terapiou v našom súbore pacientov.
Kvantitatívny HBsAg sme stanovovali na analyzátore cobas e 411 testom HBsAg II quant Roche. Vyšetrili sme vzorky pacientov, ktorí sú dispenzarizovaní u hepatológa/infektológa pre chronickú hepatitídu B a u ktorých sme zaznamenali požiadavku na stanovenie kvantity HBsAg. Do súboru bolo zaradených 95 pacientov, u ktorých sme zároveň stanovili aj vírusovú nálož HBV DNA v sére.
Súbor sme rozdelili na pacientov s terapiou a bez terapie a podľa prítomnosti HBeAg.
Do skupiny bez terapie bolo zaradených 46 pacientov. Z nich 4 boli v čase vyšetrovania indikovaní na terapiu, jeden pacient pre reaktiváciu VHB po chemoterapii a traja HBeAg reaktívni pacienti. Týchto pacientov sme dodatočne vyradili zo súboru a ďalej sme pracovali so súborom 42 pacientov bez terapie. Všetci pacienti boli zároveň HBeAg negatívni.
Vzorky sme rozdelili podľa viremickej nálože na skupinu s HBV DNA < 2 000 IU/ml, skupinu s HBV DNA 2 000 – 20 000 IU/ml a skupinu s HBV DNA > 20 000 IU/ml. U jednotlivých skupín sme sledovali hladinu HBsAg (Tab.1).

Hladinu HBsAg menej ako 1000 IU/ml malo v súbore celkom 20 pacientov, všetci patrili do skupiny s hladinou HBV DNA menej ako 20 000 IU/ml, resp. menej ako 2 000 IU/ml.
U 22 pacientov sme zaznamenali hladinu HBsAg > 1000 IU/ml. Jeden z nich mal zároveň vírusovú nálož > 20 000 IU/ml HBV DNA. Ostatní mali vírusovú nálož menej ako 20 000 IU/ml.
Zo 17 pacientov s HBV DNA PCR < 2 000 IU/ml a HBsAg kvant. viac ako 1000 IU/ml nás najviac zaujímali pacienti, ktorí mali pri nízkej vírusovej náloži veľmi vysokú hladinu HBsAg. Identifi kovali sme 5 pacientov s nálezom nízkej vírusovej nálože a zároveň hladinou HBsAg viac ako 13 000 IU/ml.
Zhodu výsledkov HBV DNA a HBsAg v skupine pacientov bez terapie sme zaznamenali u 21 pacientov zo súboru, čo je 50 %.
V čase vyšetrovania vzoriek bolo 49 pacientov zo súboru liečených, z nich 8 bolo HBeAg pozitívnych, ostatní HBeAg negatívni. Ani jeden z pacientov nebol liečený pegylovaným interferónom α, všetci mali v terapii analógy báz, a to tenofovir (41 pac.), entecavir (4 pac.) a lamivudin (4 pac.). Jeden pacient bol liečený krátkodobo entecavirom a v priebehu roku u neho došlo k sérokonverzii na anti HBs. Tohto pacienta sme vyradili z ďalšieho sledovania.
Na dlhodobej terapii NAs bolo 48 pacientov. U pacientov na terapii NAs sa pravidelne vyšetruje viremická nálož a biochemické a histomorfologické hepatálne parametre. Porovnali sme výsledky HBV DNA PCR a kvantity HBsAg v tejto skupine pacientov.
Zaujímali nás najmä pacienti s dobrou viremickou odpoveďou na terapiu, t.j. pacienti s HBV DNA PCR s negatívnym nálezom alebo s nálezom HBV DNA PCR < 13 IU/ml, čo bolo spolu 41 pacientov. Vzorky sme rozdelili podľa hladiny HBsAg na skupinu s HBsAg kvantitou < 1000 IU/ml a skupinu s kvantitou H BsAg viac ako 1000 IU/ml (graf 1).
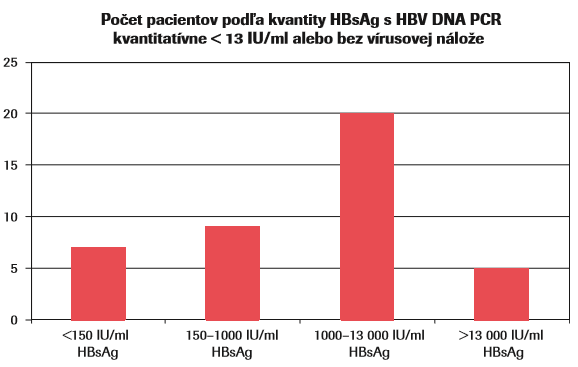
Hladinu nad 1000 IU/ml HBsAg sme zaznamenali u 25 pacientov, 16 pacientov malo hladinu HBsAg menej ako 1000 IU/ml.
Z každej skupiny nás zaujímali najmä pacienti s veľmi vysokou hladinou HBsAg (podskupina 1) a veľmi nízkou hladinou HBsAg (podskupina 2).
Do podskupiny 1 patrilo 5 pacientov s nálezom hladiny HBsAg viac ako 13 000 IU/ml. Z nich jeden bol HBeAg reaktívny, u jedného pacienta bola rozvinutá cirhóza heparu a dvaja mali zvýšenú hladinu ALT. Jeden pacient mal hladinu ALT v norme, bol HBeAg negatívny a bez známok fibrózy.
Do podskupiny 2 sa zaradilo 7 pacientov s nálezom hladiny HBsAg menej ako 150 IU/ml. Šesť pacientov z tejto skupiny malo histomorfologický nález na hepare v štádiu fi brózy F4 až cirhózy pečene. Jeden pacient mal fyziologické hladiny ALT, bol HBeAg negatívny a histomorfologicky mal hepar bez patologického nálezu (tab. 2).
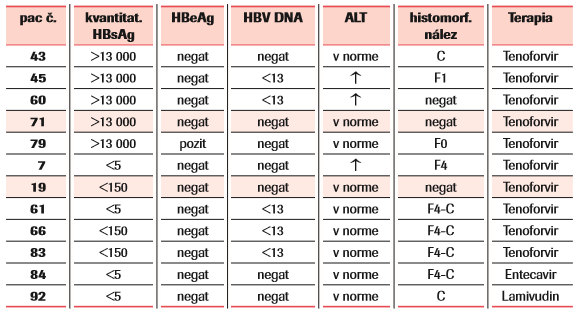
V skupine pacientov na dlhodobej terapii NAs sme identifi kovali dvoch pacientov s rovnako negatívnym nálezom ALT a HBeAg, bez fibrotického poškodenia heparu a s negatívnou virémiou. Rozdielnym nálezom bola hladina HBsAg, u prvého bola viac ako 13 000 IU/ml, u druhého menej ako 150 IU/ml.
Diskusia
Hepatitída B je ochorenie prebiehajúce akútne alebo chronicky. Chronická hepatitída B prebieha v niekoľkých štádiách. Problematickým sa javí odlíšenie fázy HBeAg negatívnej chronickej hepatitídy B, ktorá je aktívnym a progredujúcim ochorením od fázy inaktívneho nosičstva HBsAg. Brunetto a kol. v roku 2010 publikovali závery práce, v ktorej potvrdili súvislosť hladiny HBsAg a aktivity CHB u HBeAg negatívnych pacientov s hepatitídou B genotypu D. U nosičov HBs antigénu boli namerané hodnoty HBsAg menej ako 1000 IU/ml. U aktívnej HBeAg negatívnej CHB sa hodnoty kvantitatívneho HBsAg udržiavali bez významnejšej fl uktuácie nad 1000 IU/ml. Hladina vírusovej nálože HBV DNA fluktuovala 7 . V našom súbore sme u pacientov bez terapie identifi kovali 34 pacientov s nízkou vírusovou náložou pod 2 000 IU/ml. Z nich u 17-tich boli súčasne namerané hodnoty HBsAg menej ako 1000 IU/ml. To by týchto pacientov radilo do skupiny inaktívnych nosičov.
U druhých 17-tich sme namerali hodnoty HBsAg viac ako 1000 IU/ml, u piatich dokonca hladinu HBsAg vyššiu ako 13 000 IU/ml. U 5 pacientov (12 %) sme zaznamenali pri nízkej miere replikácie vírusu vysokú mieru infi kovanosti buniek, t.j. HBV DNA menej ako 2 000 IU/ml a zároveň HBsAg viac ako 13 000 IU/ml. Je pravdepodobnejšie, že sa u nich jedná o aktívne prebiehajúce ochorenie.
Aplikácia záverov vyššie uvedenej publikovanej práce na náš súbor pacientov môže pomôcť klinickým kolegom oddiferencovať neaktívnych nosičov HBsAg od pacientov s aktívnou HBeAg negatívnou CHB v kratšom čase a ekonomicky atraktívnejšou vyšetrovacou metódou. Je samozrejme potrebné potvrdiť platnosť uvedených záverov v našich zemepisných šírkach na širšom súbore pacientov.
Liečba chronickej hepatitídy B je zvyčajne indikovaná v imunoreaktívnom štádiu. Hladina HBV DNA v sére, hladina ALT a závažnosť poškodenia heparu sú rozhodujúce pri začatí terapie. Cieľom terapie je virologická supresia s biochemickou remisiou a histologickým zlepšením. Za cieľ sa považuje vymiznutie HBsAg, ideálne s prechodom do sérokonverzie na anti HBs. Jeden z indikátorov efektu terapie je vírusová nálož a v prípade terapie PEGIFN α aj sledovanie hladiny HBsAg. Počas terapie NAs, ktorá je v mnohých prípadoch dlhoročná a nezriedka doživotná, sa sleduje vírusová nálož. Boli prezentované publikácie, poväčšine ázijských autorov, v ktorých sa sledovala aj hladina HBsAg. Chan a kol. v roku 2011 publikovali prácu, v ktorej poukazujú na fakt, že rýchly pokles hladiny HBsAg po začatí terapie NAs identifi kuje pacientov, u ktorých v dlhodobom horizonte dôjde k vymiznutiu HBsAg. Zároveň zistili, že u pacientov s dobrou vírusovou odpoveďou a hladinou HBsAg nižšou ako 100 IU/ml pred ukončením terapie bolo signifi kantne nižšie riziko relapsu po ukončení terapie NAs(8). Chen a kol. v roku 2015 publikovali prácu, v ktorej sledovali vzťah medzi kvantitou HBsAg a relapsom po entecavírusovej terapii. Záverom práce bolo zistenie, že u pacientov s hladinou HBsAg menej ako 150 IU/ml pred ukončením NAs terapie sa virologický relaps vyskytol v nižšej miere. Tento fakt platil pre pacientov vo veku menej ako 55 rokov 9 .
V našom súbore pacientov na NAs terapii sme zo súboru 48 pacientov identifi kovali dvoch, u ktorých by parametre virologickej a biochemickej aktivity ochorenia a histologického nálezu teoreticky umožnili prerušenie NAs terapie. U jedného sme zaznamenali kvantitu HBsAg >13 000 IU/ml, teda predpokladáme vysokú mieru infi kovanosti buniek a vysoký predpoklad virologického relapsu. Na druhej strane je pacient, u ktorého hladina HBsAg <150 IU/ml predikuje nízku mieru relapsu po prípadnom ukončení terapie.
Relatívne nízky výskyt hepatitídy B v našich zemepisných šírkach nám bráni vytvoriť dostatočne veľký súbor, na ktorom by sme mali možnosť overenia záverov pozorovania ázijských autorov. Je potvrdený vplyv genotypu na priebeh hepatitídy B ako aj na odpoveď na terapiu. Rozdielnosť výskytu genotypov nám preto znemožňuje prebrať závery sledovania a aplikovať ich v našich podmienkach bez následných štúdií, v ktorých by sme tieto fakty potvrdili resp. vyvrátili.
Záver
Možnosti využitia kvantitatívneho HBsAg sa ukazujú v dvoch oblastiach, aj keď táto práca nemá ambíciu ich defi nitívneho vymedzenia.
Prvou je sledovanie natívneho priebehu CHB a najmä odlíšenie chronickej H BeAg negatívnej CHB od fázy inaktívneho nosičstva v čo najkratšom čase, ideálne jedným odberom a vyšetrením vzorky séra pacienta. U HBeAg negatívnej CHB sa jedná o progredujúci proces s následnými zmenami na morfologickej úrovni. Tento proces trvá viac rokov a teda aj sledovanie pacienta a vyhodnotenie záverov, resp. potvrdenie progresie je dlhodobý proces.
Druhou, podstatne zložitejšou oblasťou je sledovanie pacienta s terapiou. V našom súbore sme zatiaľ mali možnosť vyšetriť vzorky len od pacientov s terapiou analógmi báz. Mechanizmus účinku NAs je známy (obr. 1). Dochádza k blokovaniu dokončenia syntézy kompletného viriónu a jeho uvoľneniu z bunky. Pri dobrom terapeutickom účinku preto nedetegujeme HBV DNA v sére. V jadre hepatocytu perzistuje cccDNA a je prepisovaná do sgRNA aj pgRNA a je dôležité získať prehľad o jej kvantite a aktivite. Tvorba viriónu je kódovaná pgRNA. Jej zostrihom vzniká RNA kódujúca C proteín s core a pre-core oblasťou. Core oblasť kóduje syntézu HBcAg a pre-core oblasť HBeAg. HBcAg nie je uvoľňovaný do séra. HBeAg je v sére možné detegovať aj kvantifi kovať. Vzhľadom k častej mutácii v pre-core oblasti, následkom ktorej dochádza k vzniku HBeAg negatívnej CHB, ani táto možnosť nie je vyhovujúca. Obraz o kvantite cccDNA dávajú aj produkty translácie sgRNA, teda HBsAg. Nakoľko transkripcia sgRNA a pgRNA sú procesy riadené odlišnými, od seba nezávislými promotormi, sú na sebe nezávislé. Sledovaním kvantity HBsAg získame predstavu o kvantite a aktivite transkripcie cccDNA neinvazívnym a ekonomicky prijateľným testom.
Zavedenie stanovovania kvantity HBsAg je prínosom v sledovaní natívneho priebehu chronickej hepatitídy B ako aj v monitoringu liečeného pacienta.