Článek popisuje poslední poznatky etiopatogeneze formování placenty a zásadní úlohu vzájemného vztahu angiopoetinů a angiostatinů. Průkazné nízké koncentrace angiopoetinu PlGF spolu s patologickými průtoky v uterinních arteriích na konci I. trimestru selektují skupinu těhotných žen s vyšším rizikem pozdějšího vzniku preeklampsie. Pro časnou diagnózu subklinických stadií preeklampsie se osvědčilo využít stanovení poměru sFlt‑1/PlGF. Rychle rostoucí hodnota se ukazuje být dostatečně validní pro včasné ukončení těhotenství a zabránění fatálních mateřských a fetálních komplikací.

Úvod
Preeklampsie je pro těhotenství specifické onemocnění. Je definována jako těhotenstvím podmíněná hypertenze s proteinurií. Jedná se o vaskulopatii vznikající na podkladě abnormálního vývoje placenty. Klinicky se zpravidla projevuje až po 20. týdnu gravidity. V důsledku abnormální cévní reakce vede k různě významnému multiorgánovému postižení. Podle závažnosti rozlišujeme lehkou a těžkou formu preeklampsie a podle doby vzniku rozlišujeme časnou formu preeklampsie, která se manifestuje před 34. gestačním týdnem, a pozdní formu preeklampsie, která se manifestuje po 34. gestačním týdnu. Pozdní forma má z hlediska perinatologických výsledků lepší prognózu. Incidence u těhotných se pohybuje mezi 4 a 8 %. Rizikové skupiny jsou uvedeny v tabulce č. 1. 7
Etiopatogeneze preeklampsie
Etiopatogeneze preeklampsie není doposud uspokojivě objasněna. Shoda panuje v tom, že primární příčina je uložena v placentě a že porucha je založena mnohem dříve, než dojde k manifestaci prvních příznaků. Preeklampsie vzniká na základě nepřiměřené nebo patologické mateřské odpovědi na placentaci. Svou roli zde hrají fetální antigeny a imunitní mateřská odpověď. Tyto „zánětlivé signály“ vedou k lokální ischemii, kdy následná reperfuze vede k oxidačnímu stresu a vaskulárnímu poškození. Nelze tak od sebe oddělovat dvě nejuznávanější teorie vzniku preeklampsie – vaskulární a imunologickou, protože se úzce propojují. Pro omezený prostor nelze zabíhat zcela do podrobností. Uvádíme jen zásadní procesy důležité pro vývoj placenty.
Pro plynulý růst plodu a jeho dobrý stav je nezbytný koordinovaný vývoj stromu fetálního klku. Již před viabilitou plodu dochází k rozvětvené angiogenezi, v placentě se vytvoří 10–16 generací kmenových klků. Jakmile se objeví vitální známky, vývoj placenty pokročí k vytvoření velkého počtu terminálních klků schopných výměny plynů. Pro tento proces je nezbytná dostatečná trofoblastická invaze, která je dokončena mezi 12. a 14. gestačním týdnem. Hlavním obdobím pro posouzení kvality placentární implantace je 20.–24. gestační týden, protože je trofoblastem dokončena transformace myometrálních spirálních arterií v nízkorezistentní cévy s vysokým průtokem. Tím je zajištěn adekvátní průtok krve v intervilózních prostorách, kde se odehrává fetomaternální výměna. Tento proces je vícestupňovitě regulován a svoji roli v něm hrají NK buňky (natural killer cells), které ovlivňují nejen trofoblastickou invazi, ale i vaskulární změny v placentě svou schopností produkovat cytokiny, které se uplatňují v angiogenezi a ovlivňují vaskulární stabilitu. Patří k nim vaskulární endoteliální růstový faktor (vascular endothelial growth factor, VEGF), placentární růstový faktor (placenta growth factor, PlGF) a angiopoetin 2.
Tyto angiopoetiny hrají zásadní roli v procesu angiogeneze. Proti tomu působí angiostatiny – solubilní fmslike tyrosinkináza 1 (solubile fmslike tyrosine kinase 1, sFlt1), jejíž gen kóduje receptor pro vaskulární endoteliální růstový faktor 1 (vascular endothelial growth factor receptor 1, VEGFR1), protein, který reguluje proliferaci a diferenciaci buněk. V průběhu fyziologické gravidity dochází k přiměřené interakci mezi endovaskulárním trofoblastem a deciduálními leukocyty a zejména přirozenými zabíječi (NK buňkami), která následně vyvolá uvolnění VEGF a PlGF. Za přítomnosti zvýšeného zánětlivého stresu, a to i v průběhu fyziologické gravidity, jsou zvýšené koncentrace volného VEGF důležité pro zachování klidového stavu endotelu. Placentou vytvářený sFlt1 je antagonistou proangiogenních molekul VEGF a PlGF a jeho hodnoty jsou zvýšeny u preeklampsie. Placentární růstový faktor je esenciální faktor placentárního vaskulárního vývoje, proliferace a vaskulární permeability a přežívání endoteliálních buněk. Zvýšená koncentrace cirkulujícího sFlt1, proteinu z vaskulárního endotelu placenty, je spojena se sníženými cirkulujícími koncentracemi volného VEGF a PlGF, což vede k endoteliálnímu poškození. Míra zvýšení sFlt1 koreluje se závažností preeklampsie. To je v souladu s hypotézou, že narušení rovnováhy VEGF (PlGF) a sFlt1 je jednou z definitivních patofyziologických cest vzniku tohoto onemocnění. U gravidit, u kterých následně došlo k rozvoji preeklampsie a růstové restrikci plodu (fetal growth restriction, FGR), byly v prvním trimestru prokázány snížené koncentrace PlGF a naměřeny snížené hodnoty dopplerovského měření průtoku v uterinních arteriích (průkaz noche). Hodnoty sFltl se v této fázi těhotenství neliší od normy. Tyto nálezy potvrzují zásadní roli deciduálních angiogenních růstových faktorů, zejména placentárního růstového faktoru, pro fyziologický vývoj placenty.

V průběhu fyziologické gravidity jsou hodnoty sFltl do 29.–33. gestačního týdne stabilní a pak stále rostou až do porodu. Koncentrace PlGF rostou převážně do konce prvního trimestru, vrcholu dosahují kolem 29. gestačního týdne a pak postupně klesají. Zvyšující se poměr sFlt1/PlGF po 20. týdnu gestace je známkou narušené rovnováhy a slouží k časné diagnostice preklinických stadií časné formy preeklampsie. K diagnostice pozdní formy preeklampsie vzniklé po 34. gestačním týdnu není stanovení poměru sFlt1/PlGF pro diagnózu již tak průkazné. Ačkoliv příčiny placentární dysfunkce nejsou plně odhaleny, všeobecně je akceptováno, že stavy spojené s placentární dysfunkcí jsou charakterizovány mělkou trofoblastickou invazí a nedostatečnou remodelací mateřských spirálních arterií v I. a II. trimestru těhotenství. To způsobuje nedostatečnou placentární perfuzi v druhé polovině těhotenství. Endoteliální dysfunkce je výrazem excesivní mateřské zánětlivé odpovědi na těhotenství. 7
Predikce preeklampsie
Screening preeklampsie v pravém smyslu jeho významu neexistuje, ale pokud bychom na konci I. trimestru u všech těhotných stanovovali střední arteriální tlak (mean arterial pressure, MAP), hodnotu PlGF, případně doplněnou o hodnotu plazmatického specifického těhotenského proteinu A (pregnancy associated plasma protein A, PAPPA) v krvi matky, a vyšetření doplnili o flowmetrii uterinních arterií, selektovali bychom skupinu žen se zvýšeným rizikem vzniku preeklampsie v pozdějších stadiích těhotenství a cíleně bychom na ně směrovali prenatální péči. Každý abnormální výsledek z uvedených vyšetření ukazuje na zvýšená těhotenská rizika, ale riziko pro preeklampsii není specifické. Integrací všech vyšetření se specificita výrazně zvyšuje, ale i tak to neznamená, že žena s pozitivním výsledkem „I. trimestrálního screeningu“ preeklampsií onemocní. Od ideálu testování všech těhotných máme daleko, ale měli bychom se zaměřit alespoň na těhotné ženy uvedené v tabulce l v úvodu článku. Studie ASPRE z roku 2017 prokázala validitu tohoto vyšetření. Pozitivním pacientkám byla v této studii od 11. do 36. gestačního týdne preventivně podávána kyselina acetylsalicylová v dávce 150 mg/den a došlo ke snížení rizika vzniku preeklampsie před 37. gestačním týdnem o 62 %. 1,2,5
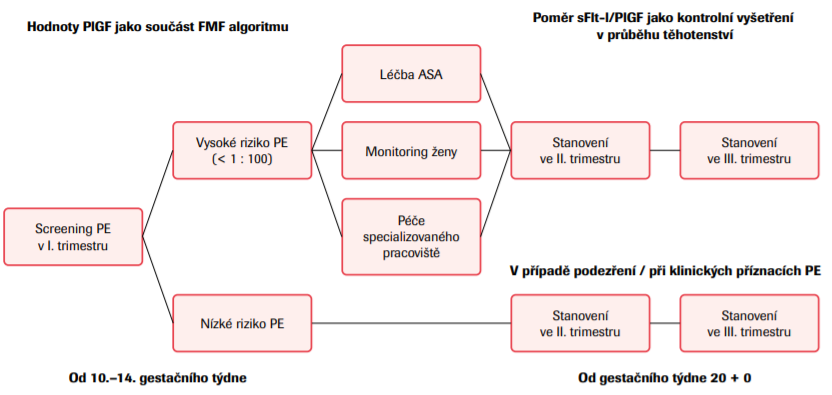
Časná diagnostika preeklampsie
V současné době je v České republice doporučena depistáž preeklampsie pouze měřením krevního tlaku a orientačním vyšetřením moči na přítomnost bílkoviny při každé návštěvě v prenatální poradně. Studie PROGNOSIS z roku 2016 ukázala na význam stanovení poměru sFltl/PlGF v časné diagnostice preklinických stadií preeklampsie ve II. a III. trimestru těhotenství. Test je doporučeno provádět u všech žen se zvýšeným rizikem preeklampsie, tedy i nezávisle na výsledku testu v I. trimestru. Rychle se zvyšující hodnota poměru sFltl/PlGF signalizuje rozvíjející se preeklampsii. Komplexní management ukazuje obr. č. 2.

Vyhodnocení a doporučený postup
Vyhodnocení a další doporučený postup jsou vždy dány výrobcem testovacích kitů. Výsledky testu je vždy nutné posuzovat komplexně s výsledky ostatních vyšetření, jako ultrazvukového a dopplerovského vyšetření, s výsledky klasických laboratorních vyšetření při preeklampsii a klinickým stavem těhotné v kontextu s gestačním stářím plodu. Je to významné z hlediska optimální doby ukončení těhotenství. 3,4,6
Závěr
Stanovení MAP, dopplerovské vyšetření uterinních arterií a stanovení hodnoty PlGF (PAPPA) v I. trimestru se zdá být užitečnou metodou selekce žen s potencionálním rizikem vzniku preeklampsie. Stanovení poměru sFlt/ PlGF ve II. a III. trimestru je nový užitečný test sloužící k časnému odhalení subklinických stadií preeklampsie. Přínosem metod je možnost predikce preeklampsie, stratifikace a optimalizace poskytované péče, což může přispět ke zlepšení prenatálních výsledků a odvrácení fatálních komplikací jak u matky, tak u plodu.
Nezávislý odborný článek publikovaný v časopise Gynekologie a porodnictví 2020; 4(2): 1-3 díky finanční podpo‑ ře společnosti Roche s.r.o., Diagnostics Division.