Onkologická a kardiovaskulární onemocnění jsou hlavními příčinami mortality i morbidity ve vyspělém světě. Podle dosavadních šetření American Cancer Society se odhaduje, že u mužů je pravděpodobnost onemocnění onkologickým maligním onemocněním 43 % a u žen 38 %1. Podle těchto šetření se alespoň nějaký nežádoucí kardiovaskulární efekt vyskytne u 30 % nemocných léčených protinádorovou terapií. Tento stav je důsledkem významných pokroků v terapii onkologických onemocnění, které představují zlepšení kvality a prodloužení života těchto pacientů, tedy i prodloužení doby, během níž se mohou manifestovat pozdní nežádoucí účinky.
Současně dochází k dalšímu významnému procesu, který je úzce spojen s touto problematikou: pokroky v terapii srdečně-cévních onemocnění a všeobecné stárnutí populace přinášejí zvyšující se počet pacientů, kteří mají anamnézu onemocnění kardiovaskulárního systému nebo vyšší polymorbiditu a v důsledku propuknutí onkologického onemocnění se musí podrobit protinádorové léčbě. Z těchto důvodů nabývají tyto otázky na významu a naším hlavním úsilím je včasná detekce a léčba projevů kardiotoxicity s cílem minimalizovat jejich vliv a uchovat velmi příznivý vliv protinádorové terapie na kvalitu života i přežití této skupiny pacientů. Významnost těchto skutečností dokladuje iniciativa pracovní skupiny pro kardioonkologii při Heart Failure Association Evropské kardiologické společnosti, která vydala doporučení pro klinickou praxi (2016 ESC Position Paper on cancer treatments and cardiovascular toxicity developed under the auspices of the ESC Committee for Practice Guidelines) 1. Tento materiál přijala mezi svá doporučení také Česká kardiologická společnost ČLS JEP 2.
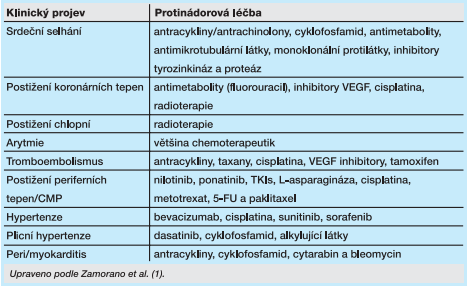
Obsah pojmu kardiotoxicita
Rozšíření spektra prostředků protinádorové terapie s sebou přineslo také rozšíření spektra potenciálně negativních účinků na kardiovaskulární systém. V současnosti pojem kardiotoxicita zahrnuje široké spektrum nežádoucích účinků (klinických projevů) protinádorové terapie na kardiovaskulární systém 1,2,3. Mezi hlavní klinické projevy kardiotoxicity jsou řazeny: srdeční selhání, postižení koronárních tepen, postižení srdečních chlopní, vznik arytmií, tromboembolismus, postižení periferních tepen včetně CMP, arteriální hypertenze, plicní hypertenze a postižení peri- a myokardu.
Základní klinické projevy kardiotoxicity protinádorové terapie

Srdeční selhání (cancer therapeutics-related cardiac dysfunction, CTRCD)
Historicky první detekovaný projev kardiotoxicity protinádorové terapie, který byl důsledkem negativního působení antracyklinů na myokard a vedl k rozvoji srdečního selhání. Incidence se pohybuje v rozmezí 2–40 % 4. K poruše funkce levé komory srdeční může vést terapie antracykliny, alkylujícími látkami, inhibitory tyrozinkázy, antimetabolity a dalšími. Patogeneze postižení není doposud uspokojivě objasněna. V minulosti se používala patogenetická klasifikace, která vycházela především z představ o reverzibilitě onemocnění:
• typ I (antracyklinový) – zpravidla ireverzibilní, který vznikl v důsledku těžkých strukturálních změn myocytů nekrózou a apoptózou, kde hlavní roli v patogenezi měly reaktivní kyslíkové radikály ovlivňující řadu procesů (karbonylaci proteinů, peroxidaci lipidů a poškození DNA), později se ukázalo jako hlavní mechanismus ovlivnění topoizomerázy 2, které vedlo k vlastnímu poškození DNA, tíže postižení byla závislá na dávce, modelovými léčivy byly antracykliny;
• typ II (herceptinový) – velmi často reverzibilní, mechanismus není zcela jasný, podle současných představ je příčinou blokáda HER 2 receptoru, který má za normálních okolností protektivní roli – příznivě ovlivňuje adaptaci myocytu na stres, jeho blokáda pak vede k poruše funkce a následnému zániku, projevem kardiotoxicity je klinicky asymptomatický nebo symptomatický pokles ejekční frakce levé komory, navíc dochází k významnému přímému poškození endotelu.
S postupem doby ztratila tato klasifikace na významu: bylo zjištěno, že i blokáda HER 2 receptorů může vést k ireverzibilnímu poškození myokardu, navíc se významně rozšířilo spektrum používaných protinádorových léků, které mají jiné mechanismy účinků.
Klinická manifestace projevů kardiotoxicity může být:
• akutní – objevuje se přibližně u 1 % pacientů, a to ihned během/po podání preparátu, je spojena s poklesem kontraktility myokardu, často je provázena arytmiemi, může být komplikována vznikem akutního koronárního syndromu;
• subakutní/chronická – manifestuje se měsíce až rok, poškození peri/myokardu asi u 2,5 % léčených;
• pozdní – manifestuje se déle než 1 rok od ukončení terapie (často za 20–30 let), postihuje do 5 % léčených.
Aby mohla být potvrzena diagnóza, je třeba prokázat alespoň 10% pokles hodnoty ejekční frakce levé komory pod normální hodnotu. Zpravidla se k tomu využívá echokardiografické vyšetření, které je nutné kvůli konfirmaci opakovat s odstupem několika týdnů. V diagnostice se uplatňuje také EKG a velmi slibným se jeví využití kardiomarkerů. V terapii symptomatického i asymptomatického poklesu ejekční frakce levé komory je namístě zvážit podání léků pro terapii srdečního selhání (inhibitory angiotenzin konvertujícího enzymu / blokátory pro angiotenzin v kombinaci s malou dávkou beta-blokátorů).
Postižení koronárních tepen
Postižení koronárních tepen může provázet terapii fluoropyrimidiny, platinou, inhibitory VEGF (vaskulárního endoteliálního růstového faktoru – bevacizumab, sorafenib, sunitinib) a iradiací. Předpokládanými mechanismy jsou poškození endotelu, vasospasmy, navození prokoagulačních stavů a vznik nástěnných trombóz. Klinická manifestace je podobná ischemické chorobě srdeční, od anginózních obtíží typu angina pectoris až po akutní koronární syndromy.
Postižení chlopní
Chlopenní aparát může být poškozen v důsledku radioterapie, a to až u 10 % případů. Ke klinické manifestaci dochází často až s delším odstupem. V klinické praxi může být problémem případná chirurgická terapie těchto pacientů, která se často potýká se změnami mediastina po ozáření. Proto se v případě změn aortální chlopně doporučuje zvážit transkatétrovou implantaci.
Arytmie
Protinádorovou terapii provází široké spektrum arytmií, a to i klinicky velmi závažných, které mohou ohrozit pacienta na životě. Někdy jde o bradyarytmie (oxid arzenitý, bortezomib, kapecitabin, cisplatina, cyklofosfamid, doxorubicin, epirubicin, 5-FU, ifosfamid, IL-2, metotrexát, mitoxantron, paklitaxel, rituximab, thalidomid), atrioventrikulární blokády (antracykliny, oxid arzenitý, bortezomib, cyklofosfamid, 5-FU, mitoxantron, taxany, rituximab, thalidomid), častá je sinusová tachykardie (antracykliny, karmustin), fibrilace síní (alkylační látky, cisplatina, cyklofosfamid, ifosfamid, melfalan, antracykliny, antimetabolity kapecitabin, 5-FU, gemcitabin, IL-2, interferony, rituximab, romidepsin, tyrozinkinázové inhibitory aj.). Velmi nebezpečné jsou komorové arytmie, ke kterým mohou vést alkylační látky (cisplatina, cyklofosfamid, ifosfamid), amsakrin, antimetabolity (kapecitabin, 5-FU, gemcitabin), oxid arzenitý, doxorubicin, IL-2, interferony, metotrexát, paklitaxel, ponatinib, inhibitory poteazomu (bortezomib, karfilzomib), rituximab a další.
Náhlá smrt se výjimečně může vyskytnout u nemocných léčených antracykliny (velmi vzácně), oxidem arzenitým, fluorouracylem (pravděpodobně při ischemii a koronárním vasospasmu), terapii interferony, nilotinibem.
V této souvislosti má zásadní význam monitorace EKG v průběhu podání u rizikových skupin nemocných, monitorace délky QTc intervalu, který může odhalit blížící se riziko, a dále odstranění všech faktorů, které by mohly usnadnit vznik takových arytmií (hydrominerálové dysbalance).
Arteriální hypertenze
Terapie některými protinádorovými léky může být spojena se signifikantním vzestupem krevního tlaku (inhibitory VEGF), proto je namístě pravidelná monitorace arteriálního tlaku a včasné zahájení antihypertenzní terapie (inhibitory ACE, sartany, beta-blokátory). Kalciové blokátory non-dihydropyridinového typu nejsou vhodné z důvodu rizika lékových interakcí.
Tromboembolismus
Některé typy protinádorové terapie jsou spojeny se zvýšením rizika tromboembolismu (antracykliny, taxany, cisplatina, VEGF inhibitory, tamoxifen), přičemž tvorba trombů a riziko následné embolizace jsou u onkologických pacientů velmi často zvýšené a vyplývají z povahy onkologického onemocnění.
CMP a onemocnění periferních tepen
Podání některých protinádorových léčiv je spojeno s postižením periferních tepen a vznikem mozkových příhod. Patří mezi ně např. nilotinib, ponatinib a inhibitory BCR-ABL kinázy. Příznaky se mohou projevit časně nebo až po letech od zahájení terapie.
Plicní hypertenze
Plicní hypertenze je spíše vzácnějším projevem kardiotoxicity, je dobré na ni myslet u nemocných léčených dasatinibem, cyklofosfamidem či alkylačními látkami. V diagnostice je metodou volby echokardiografie, která umožňuje provést odhad systolického tlaku v plicnici.
Postižení perikardu
Podání některých typů protinádorové terapie může být provázeno rozvojem akutní perikarditidy (např. antracykliny, cyklofosfamid, cytarabin, bleomycin) se všemi klinickými příznaky. Po iradiaci dochází častěji k rozvoji chronického postižení perikardu, které se objevuje zpravidla s odstupem řady měsíců až let a může vést k rozvoji konstrukce myokardu.
Diagnostika kardiotoxicity

Diagnostika projevů kardiotoxicity se opírá o vyhodnocení klinického stavu, zhodnocení 12svodového elektrokardiogramu a především o echokardiografické vyšetření. Ostatní zobrazovací metody mají spíše komplementární pozici. Naopak do centra pozornosti se dostává využití kardiomarkerů.
Elektrokardiogram (12svodové EKG) je součástí základního vyšetření nemocných léčených protinádorovou terapií. Abnormity elektrokardiogramu pomáhají identifikovat nemocné ve zvýšeném riziku, v průběhu terapie mají význam EKG kontroly pro diagnostiku komplikací (např. projevy ischemie) a identifikaci nemocných ve zvýšeném riziku arytmií (zhodnocení délky QTc intervalu jako prognostického faktoru pro vznik komorových arytmií).
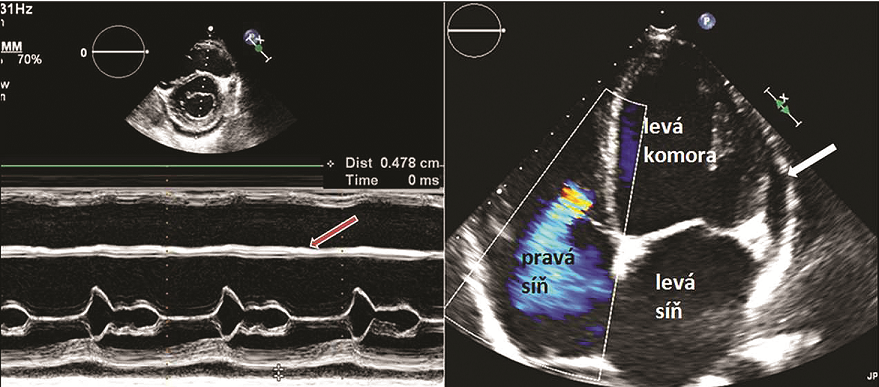
Echokardiografie je základní metodou pro iniciální stratifikaci rizika nemocných podstupujících protinádorovou terapii, v průběhu terapie je schopna odhalit změny ve funkci levé komory a prokázat tak dysfunkci myokardu, dokáže také diagnostikovat ostatní projevy kardiotoxicity (perikardiální výpotek, vznik srdeční vady a další, viz obr. 1).

Role kardiomarkerů v diagnostice kardiotoxicity
Velký potenciál přináší stanovení kardiálních markerů, kdy vzestup troponinu či hladin natriuretických peptidů (BNP a NT-proBNP) může identifikovat rizikové nemocné a nemocné s iniciálními subklinickými formami kardiotoxicity.
Markery strukturálního poškození či funkčního přetížení myokardu poskytují některé unikátní výhody v porovnání s ostatními metodami detekce kardiotoxicity: je to jejich široká dostupnost a především vysoká citlivost odhalující velmi časné až subklinické změny, a to zpravidla dříve, než se objeví první symptomy či změny detekovatelné při využití ostatních metod (elektrokardiogram nebo echokardiografie). Prozatímní nevýhodou je absence dat umožňujících standardizaci postupu.
První studie v této oblasti byly zaměřeny na potenciál využití troponinů. Již v roce 2004 prokázala D. Cardinale a kol. 5 v souboru 703 pacientů léčených vysokými dávkami antracyklinů význam stanovení troponinů před zahájením a v průběhu terapie. Studie prokázala, že u pacientů, u kterých je hladina troponinu před zahájením terapie a po jejím ukončení normální, nedojde ke vzniku dysfunkce levé komory. Naopak iniciální zvýšená hladina troponinu byla asociována s vysokým výskytem poruchy funkce levé komory (až 87 % pacientů, u kterých byly hodnoty troponinu zvýšené před terapií i po jejím ukončení). Bylo prokázáno, že vzestup troponinu je spojen s rozvojem počátečních forem diastolické dysfunkce levé komory u nemocných léčených antracykliny 6. Výsledky těchto studií byly následně potvrzeny i ve skupinách pacientů léčených trastuzumabem 7. Do studie bylo zahrnuto 251 žen léčených tímto lékem pro karcinom prsu. Analýza dat ukázala, že zvýšená hladina troponinu dokázala predikovat riziko vzniku trastuzumabem indukované kardiomyopatie. Podobně byla prokázána výpovědní hodnota u troponinů i u nemocných léčených novějšími typy terapie 8.
S nástupem užívání vysoce senzitivních metod (hs TnT) přibylo významně prací poukazujících na potenciál tohoto markeru v detekci časných forem kardiotoxicity po různých typech protinádorové terapie. Řada studií prokázala, že troponin T stanovený vysoce senzitivní metodou představuje jeden ze základních parametrů, jichž lze využít nejen k detekci časných forem kardiotoxicity, ale také ke stratifikaci rizika těchto nemocných. Například studie Katsurady a kol. 9 analyzovala možnost využití hs TnT k predikci rozvoje kardiotoxicity po terapii trastuzumabem, studie Kitayamy a kol. potvrdila tyto výsledky i pro antracykliny 10.
Dále bylo prokázáno, že hodnoty hs TnT velmi těsně korelují s detailními funkčními echokardiografickými testy, mezi něž patří tkáňově dopplerovské metody, např. speckle tracking či global longitudinal strain 11.
Podobně byla prokázána role stanovení natriuretických peptidů v diagnostice časných forem kardiotoxicity a ve stratifikaci rizika pacientů léčených protinádorovou terapií. Stanovení NT-proBNP a troponinu T se věnoval ve své studii Lipshultz a kol. Na populaci dětských pacientů prokázali schopnost NT-proBNP a troponinu T predikovat budoucí nežádoucí remodelaci levé komory srdeční 12.
Romano a kol. 13 prokázal senzitivitu NT-proBNP v predikci rozvoje kardiotoxicity u nemocných, kteří nedosahovali vysokých dávek antracyklinů. V porovnání s echokardiografií bylo stanovení NT-proBNP schopné odhalit v předstihu nemocné, u kterých se rozvíjely iniciální formy dysfunkce levé komory.
Schopnost NT-proBNP detekovat velmi časné projevy kardiotoxicity byla prokázána i u nových typů terapie (inhibitory tyrozinkináz) 14.
Závěr
Protinádorová terapie zaznamenala v posledních desetiletích významný pokrok, vedla k prodloužení života a zlepšení jeho kvality u onkologicky léčených nemocných. Proto má velký význam včasná diagnostika a zahájení léčby nežádoucích kardiovaskulárních účinků této terapie.
Z tohoto pohledu se jeví základní doporučované metody (vyhodnocení symptomů pacientů, analýza elektrokardiogramu a pravidelná echokardiografická vyšetření) jako nedostatečné a možná i nerealizovatelné s ohledem na takto velký počet potenciálně rizikových pacientů. Stanovení kardiomarkerů tedy v této indikaci představuje slibný potenciál pro iniciální stratifikaci rizika, detekci velmi časných forem kardiotoxicity a případnou monitoraci terapeutické odpovědi.