Úvod
Podíl pacientů s příznaky typickými pro akutní infarkt myokardu (AIM) na urgentních příjmech je mezi 5–10 % a tvoří až 25 % přijímaných pacientů v Evropě a USA (Druey, 2015). Nicméně kolem 80 až 90 % pacientů s podezřením na AIM má jinou konečnou diagnózu (Druey, 2015, Jaeger, 2016). Stanovení troponinů je
v současné době nezpochybnitelnou součástí diagnostického procesu u akutního koronárního syndromu, především s cílem vyloučit pacienty bez onemocnění myokardu a identifikovat pacienty s NSTEMI infarktem nebo dalšími srdečními problémy (Friedecký, 2015).
Univerzální definice infarktu myokardu
Univerzální definice infarktu myokardu vyžaduje „detekci vzestupu a/nebo poklesu srdečního biomarkeru, preferenčně troponinu měřeného vysoce senzitivními metodami, s minimálně jednou hodnotou nad 99. percentilem horního referenčního limitu a minimálně s jednou z následujících podmínek:
- příznaky ischemie;
- nové nebo předpokládaně nové signifikantní změny ST-T vlny, nebo blok levého raménka na 12svodovém EKG;
- vývoj patologických Q vln na EKG;
- důkazy nových nebo předpokládaně nových známek ztráty viabilního myokardu, nebo abnormality pohyblivosti stěn myokardu pomocí zobrazovacích metod a
- intrakoronární trombus zjištěný angiograficky nebo při pitvě.“
Typy infarktu myokardu
Podle univerzální definice infarktu myokardu z roku 2012 se rozlišuje pět (resp. šest) typů:
Typ 1: spontánní infarkt myokardu jako důsledek ruptury plátu nebo dalších procesů v luminu cévy, které vedou ke vzniku intraluminárního trombu a nekróze myokardu;
Typ 2: infarkt myokardu jako sekundární důsledek ischemické nerovnováhy mezi požadavky na přísun kyslíku a dodávkou kyslíku do myokardu, typicky při anémiích, koronárním spasmu, endoteliální dysfunkci, při dysrytmiích, respiračním selhání, hypo- a hypertenzi s hypertrofií levé komory nebo bez ní;
Typ 3: infarkt myokardu vedoucí ke smrti pacienta, bez možnosti změřit koncentrace biomarkerů;
Typ 4a: infarkt myokardu se vztahem k perkutánním koronárním intervencím, arbitrárně definovaný jako stav s překročením pětinásobku 99. percentilu koncentrace troponinů (výchozí hodnota pod 99. percentilem) nebo jako stav se vzestupem koncentrace troponinů o více než 20 % (výchozí hodnota koncentrace troponinů je zvýšená, je stabilní nebo klesá), s definovanými klinickými příznaky;
Typ 4b: infarkt myokardu se vztahem k trombóze stentu;
Typ 5: infarkt myokardu se vztahem k operačnímu zákroku na cévách (bypass), se vzestupem koncentrace troponinů nad desetinásobek 99. percentilu (výchozí hodnota pod 99. percentilem).
Původní text univerzální definice (Thygesen, 2012) uváděl: „Detection of a rise and/or fall of cardiac biomarker values [preferably cardiac troponin (cTn)].“ Výše je již uvedena aktualizovaná verze podle ESC Guidelines (Roffi, 2016), kde je drobná, leč významná změna: „Detection of an increase and/or decrease of a cardiac biomarker, preferably high-sensitivity cardiac troponin, with at least one value above the 99th percentile of the upper reference limit.“ Poměrně nešťastná formulace týkající se „increase and/or decrease“ a „99th percentile of the upper reference limit“ je dána historickým vývojem univerzální definice a není nutné ji podrobně rozebírat. Je jen potřebné si uvědomit, že připustíme-li „vzestup a/nebo pokles“, je možné u části pacientů najít stejné hodnoty, pokud jsou dvě po sobě jdoucí vyšetření provedena v delším (tj. vícehodinovém) časovém odstupu a po počátečním vzestupu byl zjištěn pokles a naopak. Také z tohoto důvodu je kratší interval mezi odběry výhodnější, samozřejmě za předpokladu používání vysoce senzitivních metod stanovení troponinů.
Diskuse o jednotlivých typech infarktu myokardu je mimo rámec tohoto sdělení. Je ale skutečností, že použitím různých metod s různou citlivostí se stalo například univerzální kritérium periprocedurálního infarktu myokardu při 5násobném zvýšení biomarkeru po výkonu na cévě (PCI, typ 4a) nebo 10násobném zvýšení po CABG (typ 5) velmi nepřesným. Pochybuje se také o typu infarktu 2, jakožto o vágním, patofyziologicky nepřesně definovaném pojmu (Collinson, 2015).
Rychlá diagnostika infarktu myokardu na urgentním příjmu je nutná, přičemž klíčovou roli hraje:
- analytická senzitivita laboratorních testů pro měření troponinů (v současné době pouze tzv. vysoce senzitivní metody, schopné vydávat číselné výsledky u více než 60 % zdravé populace);
- rychlost odezvy laboratoře (do 30 minut od dodání biologického materiálu);
- správná indikace vyšetření a správná interpretace podle vhodně zvoleného algoritmu.
Prodloužení časového intervalu v rámci rule-out diagnostiky může vést k prodlužování příjmové procedury, indikuje další zbytečná vyšetření a zvyšuje neklid pacienta i personálu na urgentním příjmu, zatímco prodloužení intervalu pro rule-in diagnostiku ohrožuje pacienta.
Jednohodinový algoritmus vyšetření u pacientů s podezřením na NSTEMI infarkt myokardu
Evropské ESC Guidelines 2015 (Roffi, 2016) uvádějí jako novinku tzv. jednohodinový algoritmus. Je založen na odběru dvou vzorků krve, při přijetí a za jednu hodinu. V algoritmu jsou uvedeny specifické postupy pro tři druhy testů (hs-cTnT Elecsys, hs-cTnI Architect a hs-cTnI Dimension Vista) s přesnými hodnotami cut-off pro rule-in a rule-out diagnostiku. Jednohodinový algoritmus je popsán v ESC Guidelines 2015 jako alternativa ke „klasickému“ tříhodinovému algoritmu, který byl poprvé uveden pro hs-cTn v ESC Guidelines v roce 2011. Vychází se přitom z faktu, že je k dispozici kvantitativní test kontinuálního charakteru, kdy se pravděpodobnost infarktu zvyšuje s rostoucí koncentrací troponinu, a dále z předpokladu, že časné absolutní změny koncentrace za jednu hodinu od prvního odběru krve jsou prediktorem změn za 3 nebo 6 hodin a přidávají tak diagnosticky cennou informaci.
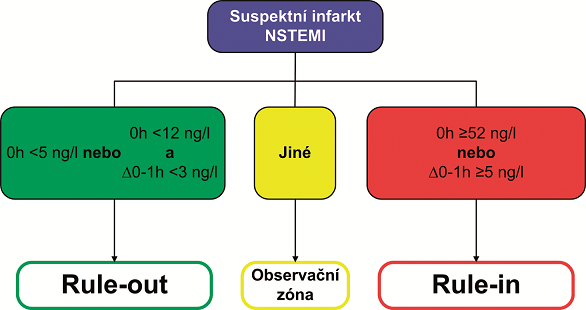
Princip algoritmu je založen na třech zónách:
- zóna rule-out, pro vyloučení infarktu myokardu, s velmi vysokou hodnotou negativní prediktivní hodnoty;
- observační zóna, kde není přítomnost infarktu myokardu možné potvrdit nebo vyloučit;
- zóna rule-in, pro identifikaci pacientů s vysokou pravděpodobností přítomnosti infarktu myokardu.
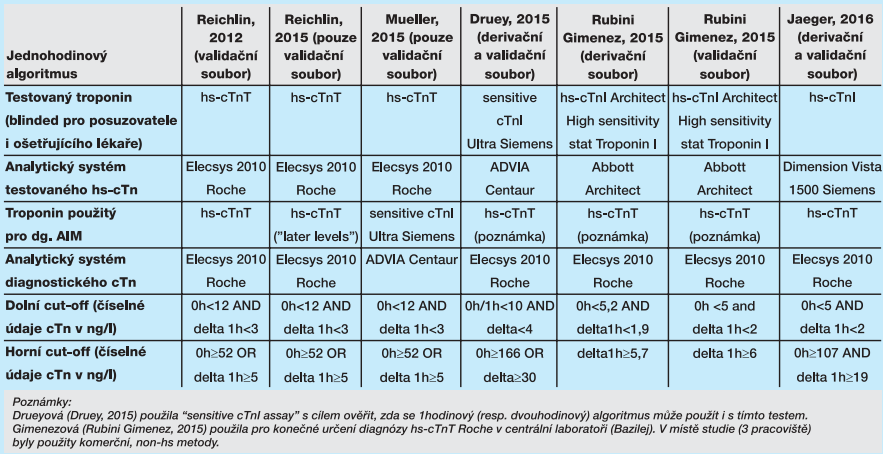
Obrázek 1 ukazuje princip jednohodinového algoritmu podle ESC Guidelines 2015 pro hs-cTnT Elecsys Roche (Roffi, 2016). Zajímavé je použití dvou cut-off hodnot, resp. definic kritérií pro zařazení do zóny rule-in nebo rule-out. Kritéria se kombinují s využitím logických operátorů „AND“ a „OR“. V případě zóny rule-out je zvolena velmi nízká koncentrace troponinů v odběru při přijetí nebo (OR) hodnota při přijetí pod 99. percentilem a současně (AND) velmi nízká hodnota delta koncentrace za jednu hodinu. V případě rule-in zóny je zvolena vyšší koncentrace při přijetí nebo (OR) vyšší hodnota delta za hodinu od přijetí. Obrázek 1 ukazuje použití cut-off hodnot v jednohodinovém algoritmu pro hs-cTnT (Elecsys). Porovnání s ostatními cut-off hodnotami viz tabulka 1. Jak vyplývá z tabulky 1, hodnoty pro rule-in a rule-out diagnostiku jsou závislé na použité diagnostické soupravě. Použití dvou diagnostických hranic vyžaduje speciální výpočty pozitivní a negativní prediktivní hodnoty, senzitivity a specifičnosti.
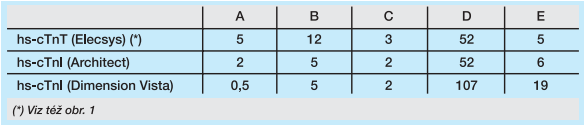
Rule-out: koncentrace v čase 0 < A OR [koncentrace v čase +1 hodina < B AND delta koncentrace mezi časem 0 a 1 hodina < C]
Rule-in: koncentrace v čase 0 >= D OR delta koncentrace mezi časem 0 a 1 hodina >= E
Nesplní-li pacient kritéria pro rule-out nebo rule-in zónu, je zařazen do tzv. observační zóny.
Základní pojmy v rozhodovacích situacích se dvěma limity pro rule-out a rule-in diagnostiku
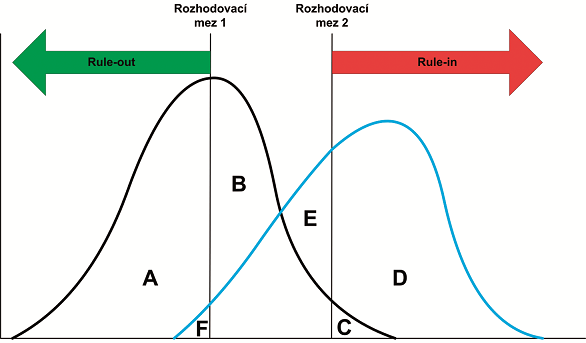
Obrázek 2 popisuje klinickou situaci použití jednohodinového algoritmu. Dvě populace (vlevo populace bez infarktu myokardu, vpravo populace s infarktem myokardu) se v hodnotách hs-cTn překrývají. Situace na obrázku je poněkud zjednodušená, protože cut-off hodnota pro rule-out a cut-off hodnota pro rule-in diagnostiku nejsou tvořeny jednou číselnou hodnotou koncentrace troponinu, ale obě cut-off hodnoty mohou být reprezentovány složenou funkcí (například hodnota při přijetí pod určitou koncentraci cTn OR hodnota při přijetí pod jinou koncentraci cTn AND delta koncentrace mezi hodnotou při přijetí a za hodinu pod jinou hodnotou rozdílu cTn).
Populace pacientů bez infarktu má část pacientů (A) pod dolní rozhodovací mezí, část pacientů (B) v observační zóně a malou část pacientů (C) nad horní rozhodovací mezí. Analogicky má populace pacientů s infarktem část pacientů (D) nad horní rozhodovací mezí, část v observační zóně (E) a část pacientů (F) pod dolní rozhodovací mezí. Poznamenejme, že jak dolní, tak horní rozhodovací mez nejsou tvořeny jednou číselnou hodnotou, ale mohou být složeny z kombinace hodnot při přijetí a/nebo ze změny koncentrace hs-cTn za jednu hodinu, jak bylo uvedeno výše. Použití dvou rozhodovacích metod vyžaduje jiné výpočty parametrů diagnostické efektivity, než je tomu u jednoduchých postupů s jednou diskriminační mezí: negativní prediktivní hodnota charakterizuje jistotu vyloučení infarktu při hodnotě hs-cTn pod dolní rozhodovací mezí, pozitivní prediktivní hodnota jistotu infarktu při výsledku nad horní rozhodovací mezí, senzitivita popisuje frekvenci výsledků nad dolní rozhodovací mezí u pacientů s AIM a specifičnost popisuje frekvenci výsledků pod horní rozhodovací mezí u pacientů bez infarktu. Podrobněji popisujeme parametry diagnostické efektivity v následujících odstavcích.
Negativní prediktivní hodnota
Klinický význam: vysoká negativní prediktivní hodnota (NPV) je potřebná v situacích, kdy je nutné bezpečně identifikovat pacienty bez vyhledávané nemoci. V případě rule-in diagnostiky akutního infarktu myokardu při použití dvou cut-off hodnot se pro tyto účely využívá dolní cut-off a jeho nastavení musí být natolik nízké, aby se pod hodnotou dolní cut-off meze prakticky nevyskytovaly osoby s infarktem. V jednohodinovém algoritmu jsou tyto hodnoty například 5 ng/l při přijetí nebo 12 ng/l při přijetí, ale za podmínky nízké hodnoty delta koncentrace (za 1 hodinu od přijetí delta méně než 3 ng/l). Z tabulky 4 vyplývá, že hodnoty NPV jsou v jednohodinovém algoritmu nastaveny na hodnoty blízké 100 %.
Statistický význam: jde o pravděpodobnost vyloučení nemoci v případě negativního testu, tj. v rámci rule-out diagnostiky při nedosažení dolní hodnoty cut-off.
Výpočet: vychází pouze z negativních hodnot testu, tedy při rule-out diagnostice s observační zónou jde o poměr mezi osobami s negativním výsledkem bez choroby (non-AIM) a všech osob s negativním výsledkem. Na obrázku 1 je tedy hodnota NPV = A/(A+F).
Pozitivní prediktivní hodnota
Klinický význam: vysoká prediktivní hodnota (PPV) není v algoritmu urgentních situací příliš podstatná, využívá se vyšší cut-off hodnota. Její nastavení se může řídit například pravděpodobností infarktu myokardu odvozenou ze studií, kapacitou lůžkového zařízení, kam je možné pacienty s překročením cut-off hodnoty v rámci rule-in diagnostiky okamžitě odeslat. V jednohodinovém algoritmu je horní cut-off hs-cTnT nastaven na 52 ng/l pro koncentraci při přijetí nebo hodnotu delta koncentrace 5 a více ng/l za 1 hodinu. Hodnoty PPV jsou v jednohodinovém algoritmu nejnižší ze sledovaných ukazatelů diagnostické efektivity (tabulka 4).
Statistický význam: jde o pravděpodobnost infarktu myokardu v případě pozitivního testu, tj. v rámci rule-in diagnostiky při překročení horní hodnoty cut-off.
Výpočet: vychází pouze z pozitivních hodnot testu, tedy při rule-in diagnostice s observační zónou jde o poměr mezi osobami s infarktem, u nichž došlo k překročení horní hodnoty cut-off (AIM), a všech osob s výsledkem nad horní hodnotou cut-off. Na obrázku 1 je tedy hodnota PPV = D/(C+D).
Senzitivita
Klinický význam: senzitivita u algoritmu s observační zónou charakterizuje pacienty s infarktem, kteří nemají výsledek pod dolní hodnotou cut-off. V jednohodinovém algoritmu je snaha nastavit senzitivitu na co nejvyšší hodnotu (společně s co nejvyšší hodnotou NPV).
Statistický význam: pravděpodobnost výsledku nad dolní hodnotou cut-off u pacientů s AIM.
Výpočet: počítá se pouze u osob s infarktem jako poměr pacientů s AIM nad dolní hodnotou cut-off a všech pacientů s AIM. Podle obrázku 1 je senzitivita = (D+E)/(D+E+F).
Specifičnost
Klinický význam: specifičnost v případě algoritmu s observační zónou charakterizuje počet pacientů bez infarktu myokardu, kteří nemají pozitivní výsledek, v tomto případě nemají pozitivní výsledek nad vyšší cut-off. Specifičnost se tedy počítá pro pacienty bez infarktu jak v observační zóně, tak v zóně rule-out.
Statistický význam: jde o pravděpodobnost výsledku pod horní hodnotou cut-off u pacientů bez AIM.
Výpočet: počítá se pouze u osob bez AIM jako poměr pacientů bez AIM pod horní hodnotou cut-off a všech pacientů bez AIM. Podle obrázku 1 je specifičnost = (A+B)/(A+B+C).
Prevalence AIM v observační zóně
Klinický význam: Observační zóna by měla zahrnovat méně pacientů s AIM, aby se péče o tyto pacienty zbytečně neodkládala. Na druhé straně vyšší počet pacientů bez AIM může zpomalovat diagnostický proces na urgentním příjmu. V jednotlivých studiích (tabulka 4) byla prevalence AIM v observační zóně mezi 8 až 23 %.
Výpočet: určí se jako podíl pacientů s infarktem a všech pacientů v observační zóně, tedy E/(B+E).
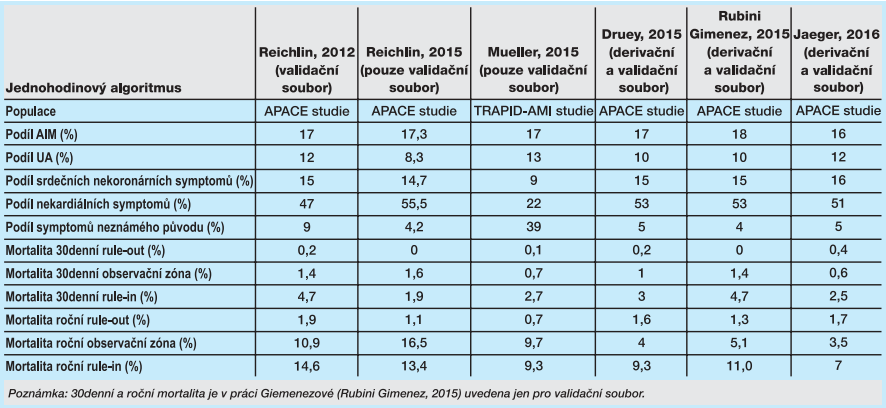
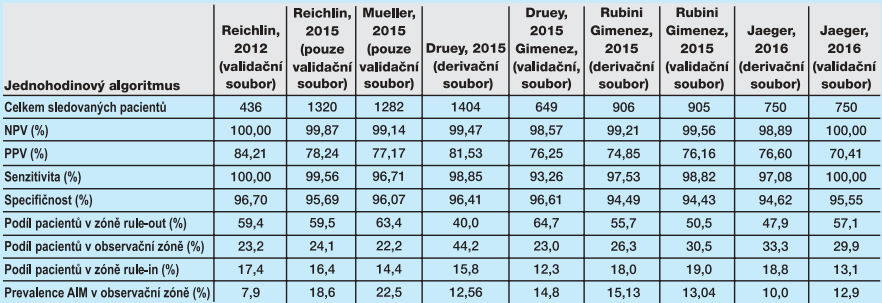
Jednohodinový algoritmus vychází ze studií, které jsou charakterizovány v tabulkách 2 až 4. Tabulka 2 ukazuje studované populace jednohodinového algoritmu, tabulka 3 testované troponiny a testovaná rozhodovací kritéria jednohodinového algoritmu. Tabulka 4 zachycuje diagnostickou efektivitu v uvedených studiích jednohodinového algoritmu.
Dvouhodinový algoritmus
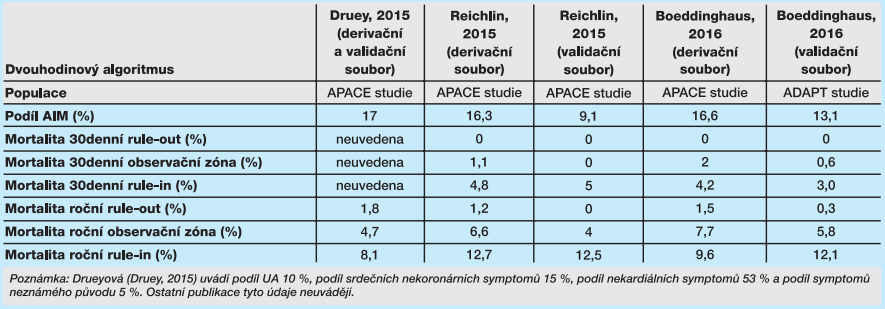
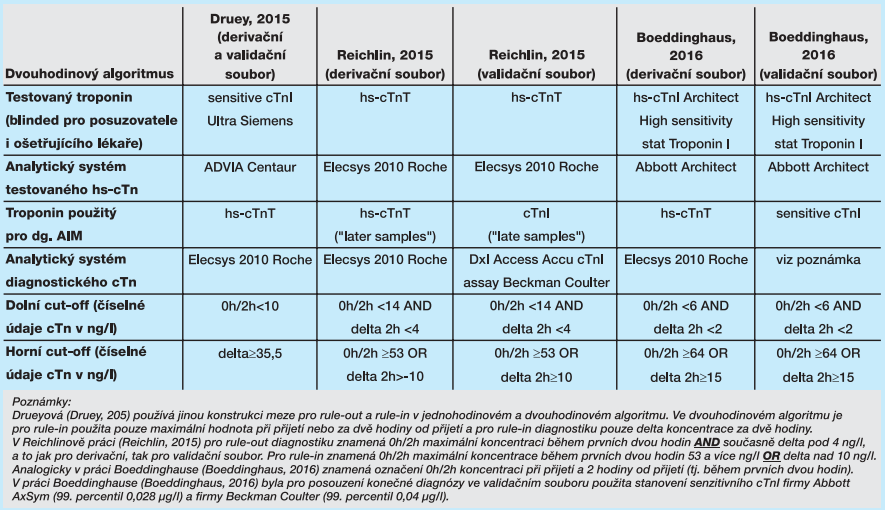
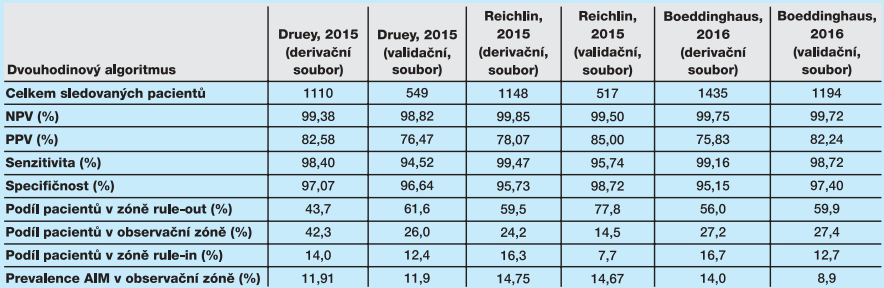
Reichlin (Reichlin, 2015) ve své práci o dvouhodinovém algoritmu upozornil na výhrady vůči bezpečnosti použití jednohodinového algoritmu v různých situacích urgentních příjmů a rovněž na praktičnost použití jednohodinového algoritmu. Navrhl proto dvouhodinový algoritmus s využitím hs-cTnT Roche na datech studie APACE. Podobně byla prověřena efektivita dvouhodinového algoritmu opět na datech studie APACE, ale s využitím nikoli hs-stanovení, ale pomocí senzitivní metody pro stanovení cTnI (Druey, 2015). Cílem této práce bylo ověřit, zda se může dvouhodinový (ale i jednohodinový) algoritmus použít i s tímto testem („sensitive cTnI assay“). Údaje z literatury o dvouhodinovém algoritmu jsou uvedeny v tabulkách 5 až 7.
Diskuse
Část studií byla provedena na pacientech studie APACE (Advantageous Predictors of Acute Coronary Syndrome Evaluation). Šlo o po sobě jdoucí pacienty z urgentního příjmu s příznaky akutního infarktu myokardu. Z této databáze pacientů čerpaly téměř všechny uvedené studie z více center, s centrálním zhodnocením konečné diagnózy na pracovišti prof. Muellera v Bazileji. Do studií byly zařazeny osoby starší 18 let, vyloučeni byli pacienti s terminálním stadiem chronického onemocnění ledvin nebo dialyzovaní pacienti. Rovněž nebyli hodnoceni pacienti se STEMI infarktem myokardu. U pacientů byly k dispozici opakovaně měřené koncentrace troponinů (obvykle do 6 hodin nebo i později od přijetí), hodnocené koncentrace v nulté, první nebo druhé hodině byly zaslepeny. V některých publikacích je samostatně vyhodnocen derivační soubor pro odvození diagnostického algoritmu a samostatně je vyhodnocen validační soubor.
Výsledky pro jednohodinový i dvouhodinový algoritmus jsou podobné. Nastavení mezí pro rule-out diagnostiku je vedeno snahou vyloučit z dalšího sledování pacienty s negativním výsledkem testu, kdy je negativní prediktivní hodnota (NPV) blízká 100 procentům. Současně s vysokou hodnotou NPV by měla být i velmi nízká falešná negativita testu (tedy vysoká senzitivita), kdy by se neměli vyskytovat pacienti s infarktem pod dolní mezí pro rule-out diagnostiku. Ve sledovaných publikacích se NPV pro jednohodinový algoritmus pohybovala mezi 98,6 až 100 % a senzitivita mezi 93,3 až 100 %, ve dvouhodinovém algoritmu byla NPV 98,8 až 99,9 % a senzitivita 94,5 až 99,5 %. Analogicky by měla být vysoká hodnota specifičnosti, kdy by pacienti bez infarktu měli mít hodnoty pod horní rozhodovací mezí (pod mezí pro rule-in diagnostiku). Pozitivní prediktivní hodnota (PPV) není až tak důležitá, protože pacient v observační zóně je dále sledován a pacient splňující podmínky pro rule-in diagnostiku je hospitalizován. Ve sledovaných publikacích se specifičnost pro jednohodinový algoritmus pohybovala mezi 94,4 až 96,7 % a PPV mezi 70,4 až 84,2 %, ve dvouhodinovém algoritmu byla specifičnost 95,7 až 98,7 % a PPV 76,5 až 85,0 %.
Použití uvedených algoritmů je možné přenést na podobné klinické situace, ve kterých byly rozhodovací meze a algoritmy odvozeny a validovány. Sami autoři upozorňují, že v jiných diagnostických situacích, kde je prevalence infarktu myokardu odlišná (ordinace praktického lékaře na straně jedné nebo naopak urgentní příjem pro specializované koronární pracoviště), nemusí být diagnostická efektivita algoritmu srovnatelná. Poměrně málo se diskutuje fakt, že variační koeficient použitých metod je v porovnání s velmi nízkými koncentracemi nebo s velmi nízkými hodnotami delta koncentrace na hranici přesného stanovení. Vznikají tak velké nároky na spolehlivost analytické metody. Je rovněž nutné vzít v úvahu, že ve většině citovaných prací se jedná stále o jeden základní soubor pacientů, práce mají většinou totožnou metodologii a autorské kolektivy mají velký průnik se zastřešením publikací prof. Muellerem. Každopádně je ale informace z jednotlivých uvedených studií vložena do rozhodovacího algoritmu, který doporučují ESC Guidelines 2015 (Roffi, 2016).
Závěry
Závěrem lze konstatovat, že použití senzitivních stanovení troponinů v klinické praxi je prověřeno (odvozeno a validováno) na populaci pacientů ze studií APACE a TRAPID AMI a je současně plně podpořeno doporučením ESC. Hodnoty PPV a NPV při použití dvou cut-off hodnot (složených z koncentrací a rozdílů koncentrací) jak v jednohodinovém, tak i dvouhodinovém algoritmu jsou vyhovující. Jisté opatrnosti je třeba v populaci pacientů se selektovaným příjmem (specifické populace) nebo při ordinaci praktickým lékařem, kde se senzitivita i specifičnost použití jednohodinového a dvouhodinového algoritmu může lišit v porovnání s populací ve studii APACE nebo TRAPID AMI. Meze algoritmu pro rule-out diagnostiku zrychlují práci na urgentním příjmu, meze pro rule-in diagnostiku nezdržují další péči o pacienty s vysokou pravděpodobností léze myokardu. U pacientů v observační zóně lze pokračovat s dalším vyšetřením koncentrace troponinů vysoce senzitivními metodami po jedné nebo dvou hodinách a podle vývoje koncentrací troponinů v klinickém kontextu stavu pacienta diagnostiku upřesnit. Vždy ale platí, že podrobná diferenciální diagnostika koncentrací troponinů vyžaduje dobrou znalost všech klinických situací, které mohou jejich koncentrace ovlivnit.