Evropská kardiologická společnost (ESC) představila na svém letošním sjezdu aktualizovaná mezinárodní doporučení pro diagnostiku a léčbu akutního a chronického srdečního selhání.1 Předchozí guidelines byla zveřejněna v roce 2016. Od té doby došlo na poli srdečního selhání k publikaci celé řady významných klinických studií a pokračuje trend jeho členění na více nozologických jednotek, především podle míry zachování ejekční frakce levé komory (LVEF). Samotná doporučení jsou zaměřená spíše na diagnostiku a léčbu, nikoliv na prevenci, která je akcentovaná v jiných ESC dokumentech. Níže přinášíme shrnutí závěrů nových doporučení pro diagnostiku srdečního selhání a přidružených komorbidit s důrazem na aktualizované poznatky.
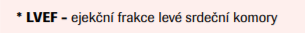
Doporučení ESC z roku 2021 připomínají, že srdeční selhání nepředstavuje jedno homogenní onemocnění, ale jedná se o pojem, který zastřešuje celou řadu klinických stavů různé etiologie. Právě identifikace konkrétní příčiny způsobující srdeční selhání je přitom klíčová pro úspěšnost léčby. Základní dělení počítá se srdečním selháním se zachovalou ejekční frakcí (HFpEF, LVEF ≥50 %), s mírně sníženou ejekční frakcí (HFmrEF, LVEF 41–49 %) a s redukovanou ejekční frakcí (HFrEF, LVEF ≤40 %). Nová doporučení ale připomínají, že se ve skutečnosti nejedná o tři izolované skupiny, ale o klinické kontinuum a že echokardiografické měření LVEF* je do jisté míry subjektivní a závisí na konkrétním vyšetřujícím.


Mezinárodní klinická doporučení klasifikují dostupnou klinickou evidenci a postupy u daného onemocnění do různých tříd doporučení a úrovně důkazů. Třídy označují prospěšnost, užitečnost a účinnost dané léčby nebo postupu (viz Tabulka 1). Úroveň důkazů potom označuje, jak rozsáhlá a konzistentní jsou data z klinických studií pro konkrétní doporučení (viz Tabulka 2). Z hlediska diagnostiky je nutno podotknout, že diagnostické postupy jsou v rámci velkých randomizovaných klinických studií testovány jen zřídka a ve většině doporučení jsou proto označeny stupněm evidence C. Autoři upozorňují, že to neznamená, že by tyto postupy nebyly před zařazením do doporučení pečlivě zkoumány a dostupná data nebyla dostatečně analyzována. Zároveň připomínají, že pro potřeby guidelines rozdělili diagnostické postupy na ty, které by měly být provedeny u každého pacienta se srdečním selháním, a na postupy určené pro specifické klinické situace. Oproti verzi z roku 2016 nabízí doporučení z roku 2021 několik zcela nových konceptů. Pojem srdeční selhání se střední ejekční frakcí se mění na srdeční selhání s mírně redukovanou ejekční frakcí (HFmrEF). Dále potom modifikuje klasifikaci pro redukovanou ejekční frakci (HFrEF) a zavádí zjednodušený algoritmus její léčby. Nová doporučení se více věnují kardiomyopatiím včetně jejich genetického testování a nových metod léčby. Součástí je také aktualizace doporučené léčby nekardiovaskulárních komorbidit, jako je diabetes, hyperkalémie, nedostatek železa nebo nádorová onemocnění, a přidání čtyř nových indikátorů kvality.
U pacientů se zachovalou ejekční frakcí (HFpEF) je doporučeno aktivně pátrat po kardiovaskulárních i nekardiovaskulárních komorbiditách a tyto by měly být léčeny (třída doporučení I). Všichni pacienti hospitalizovaní se srdečním selháním by měli být před propuštěním aktivně vyšetřeni pro přetrvávání městnání. Nově je doporučeno provádět invazivní koronarografii u pacientů se srdečním selháním se středním až vysokým podezřením na ischemickou chorobu srdeční a přítomností ischemie při zátěžových testech s vyšší třídou doporučení IIa. Naopak u pacientů s nízkým až středním podezřením nebo neprůkaznými výsledky zátěžových testů by nově s třídou IIb (dříve IIa) mohlo být zváženo srdeční CT k vyloučení koronární stenózy.
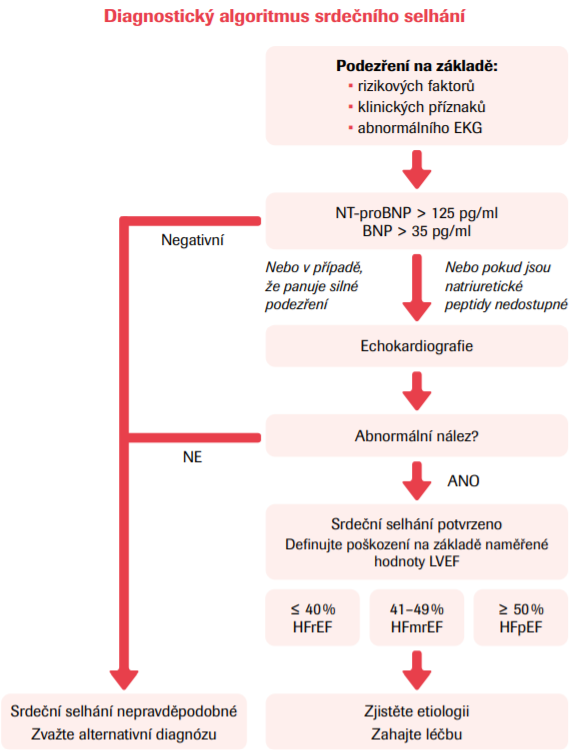
Významná změna oproti roku 2016 nastává v postavení natriuretických peptidů v diagnostickém algoritmu u chronického srdečního selhání. Natriuretické peptidy se stávají diagnostickým krokem první volby, který by měl předcházet echokardiografii (třída doporučení Ib). U pacienta s klinickým podezřením na chronické srdeční selhání je doporučen odběr NT-proBNP (pozitivní při koncentraci ≥125 pg/ml) nebo BNP (pozitivní ≥35 pg/ml). Při pozitivitě biomarkerů nebo samotném silném klinickém podezření na přítomnost srdečního selhání je doporučeno provést echokardiografii. Konkrétní určení typu srdečního selhání je provedeno na základě naměřené hodnoty LVEF. Negativní výsledek koncentrace natriuretických peptidů chronické srdeční selhání vylučuje, pozitivní hovoří pro tuto diagnózu a je užitečný pro prognostikaci nemocných. Zároveň může být použit k naplánování dalších diagnostických postupů. Klinik by ale měl mít na zřeteli, že zvýšená koncentrace natriuretických peptidů může mít i další kardiální a nekardiální příčiny, jako je fibrilace síní, vyšší věk nebo onemocnění ledvin. Na druhou stranu koncentrace natriuretických peptidů mohou být disproporcionálně snížené u obézních osob.
Diagnostický přínos natriuretických peptidů pro potvrzení nebo vyloučení srdečního selhání v kombinaci s dalšími klinickými údaji a základními testy byl ověřován v několika studiích v primární neakutní péči. Autoři doporučení shledali tyto studie jako dostatečné pro zavedení výše zmíněných cut-off hodnot do diagnostického algoritmu, a to zejména pro vyloučení chronické formy onemocnění (rule-out). Negativní prediktivní hodnota při použití 35 pg/ml proBNP, respektive 125 pg/ml pro NT-proBNP se pohybovala mezi 0,94 a 0,98. Klasifikace chronického srdečního selhání se opírá především o echokardiograficky naměřenou hodnotu LVEF. V případě selhání s mírně sníženou ejekční frakcí (HFmrEF) (LVEF 41–49 %) zmiňují nová doporučení poněkud konfliktně, že přítomnost dalších znaků včetně zvýšené koncentrace natriuretických peptidů a dalších známek strukturálního poškození srdce diagnózu podporuje, není pro ni ale zcela nutná. Ohledně problematiky diagnostiky srdečního selhání se zachovalou ejekční frakcí (HFpEF) guidelines konstatují, že zůstává svízelná. Současná diagnostická kritéria stanovená různými odbornými společnostmi vykazují různé úrovně senzitivity a specificity. Nová ESC doporučení tak zdůrazňují spíše simplifikovaný pragmatický přístup, který počítá s přítomností klinických známek srdečního selhání, hodnotami LVEF nad 50 % a objektivními známkami strukturálních a/nebo funkčních změn nebo zvýšenými plnicími tlaky levé komory, včetně zvýšené koncentrace natriuretických peptidů. Kromě toho říkají, že pokud jsou klidové echokardiografické a laboratorní parametry neprůkazné, je indikován zátěžový test. Nová ESC doporučení se věnují také dlouhodobému sledování pacientů s chronickým srdečním selháním. Pravidelné kontroly by se podle nich měly odehrát alespoň jednou za půl roku, po recentní hospitalizaci nebo změně medikace častěji. Jednou ročně by mělo být provedeno EKG. Sériový echokardiogram není nutný, indikovaný je v případě zhoršení klinického stavu, respektive 3–6 měsíců po optimalizaci standardní terapie. Samostatnou kapitolou je monitorace a optimalizace farmakoterapie pomocí biomarkerů. Klinické studie v tomto smyslu přinesly nejednoznačné závěry. Natriuretické peptidy jsou podle nich sice nesporně kvalitní prognostické markery, není ale zatím jasné, jestli poskytují přidanou hodnotu v rámci výběru a titrace konkrétní léčby.
Srdeční selhání představuje u většiny pacientů závažné onemocnění s vysokou mortalitou obecně srovnatelnou s maligními chorobami. Doporučení ESC se proto věnují i nemocným s jeho pokročilou formou, definovanou jako přetrvávající obtíže a projevy (klasifikace NYHA III nebo IV) navzdory maximální dostupné terapii, provázené silně omezenou fyzickou výkonností, doplněnou epizodami srdečního městnání vyžadujícími vysoké dávky diuretik, inotropik nebo vasopresorů, a/nebo maligními arytmiemi. Kromě toho by měl být přítomen alespoň jeden další diagnostický znak zahrnující hodnoty LVEF pod 30 %, izolované selhání pravé komory, pokročilé změny na chlopních nebo přetrvávající vysoké nebo rostoucí koncentrace natriuretických peptidů za současné diastolické dysfunkce levé komory nebo strukturální srdeční abnormality. Roční mortalita takového stavu dosahuje 25–75 %.

Akutní srdeční selhání může být buď první manifestací nově vzniklého onemocnění, nebo se častěji jedná o akutní dekompenzaci chronického srdečního selhání. V případě akutního srdečního selhání je namístě rychlá a pečlivá diagnostika, zahrnující kromě EKG echokardiografii a skiagram hrudníku, respektive sono plic. I zde se uplatňují stanovení koncentrace natriuretických peptidů, dle doporučení by měla být využita zejména v případě nejasné diagnózy a pokud jsou dostupná rychle. I zde platí, že normální koncentrace natriuretických peptidů znamená, že diagnóza akutního srdečního selhání je vysoce nepravděpodobná. Používají se ale jiné cut-off hodnoty: 100 pg/ml pro BNP a 300 pg/ml pro NT-proBNP. Vysoké koncentrace samy o sobě diagnózu akutního selhání nepotvrzují, následovat by měla vždy echokardiografie. Autoři zároveň upozorňují, že nízké koncentrace natriuretických peptidů se objevují u některých pacientů s pokročilým dekompenzovaným srdečním selháním v terminálním stavu, obezitou, plicním edémem nebo pravostranným akutním srdečním selháním. Naopak vyšší koncentrace natriuretických peptidů provází pacienty s fibrilací síní a sníženou renální funkcí. Měření koncentrace natriuretických peptidů je doporučeno sériově při příjmu a před propuštěním. Kromě toho je z laboratorních parametrů vedle rutinních vyšetření (elektrolyty, kreatinin, jaterní enzymy) doporučeno stanovit vysoce senzitivní srdeční troponin (pro vyloučení AKS), D-dimery, prokalcitonin (pro odhalení případné pneumonie nebo jiné infekce), hodnoty TSH, laktátu, arteriálních krevních plynů a parametry metabolismu železa. Po propuštění by měl mít nemocný kontrolu za 1–2 týdny. Ta by kromě klinických parametrů měla zahrnovat i laboratorní kontrolu se stanovením funkce ledvin, elektrolytů a pokud možno také natriuretického peptidu. Na základě retrospektivních klinických studií bylo pozorováno, že při adherenci k tomuto postupu a případné včasné titraci medikace dochází ke snížení třicetidenní mortality.
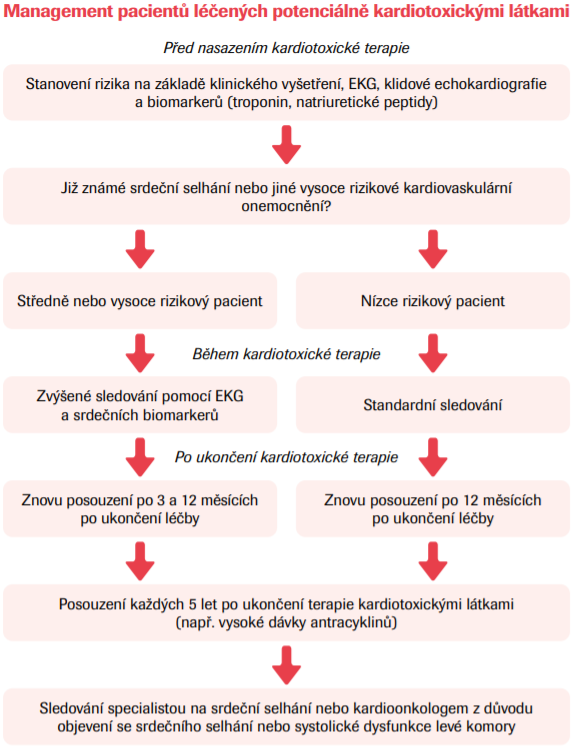
Nová ESC doporučení 2021 rovněž akcentují problematiku srdečního selhání při nádorovém onemocnění. To je v této skupině častější než v běžné populaci, ať už jako preexistující onemocnění, jako důsledek malignity, nebo důsledek onkologické terapie. Na druhou stranu přítomnost srdečního selhání může omezovat výběr vhodné protinádorové terapie. Mezi látky s kardiotoxickým účinkem patří antracykliny (doxorubicin, epirubicin), monoklonální protilátky proti HER-2 (trastuzumab), VEGF inhibitory (sunitinib, pazopanib), některé multikinázové inhibitory (ponatinib, nilotinib), proteázové inhibitory (karfilzomib, bortezomib) a imunomodulační látky (lenalidomid, pomalidomid), inhibitory RAF a MRK (dabrafenib + trametinib, vemurafenib + cobimetinib), antiandrogeny (goserelin, abiteron), check-point inhibitory (nivolumab, pembrolizumab, ipilimumab) a další látky. Pacienti vhodní pro léčbu těmito přípravky by měli být pečlivě vyšetřeni před jejich podáním, během léčby a po jejím ukončení ideálně kardiologem, který se specializuje na kardioonkologii. To platí zejména pro rizikové nemocné, nebo pacienty, kteří byli kardiotoxickým látkám vystaveni v minulosti. Vstupní kardiovaskulární riziko by mělo být stanoveno pomocí skóre HFA-ICOS. Přítomnost srdečního selhání nebo kardiomyopatie klasifikuje onkologické pacienty jako vysoce rizikové pro podání všech onkologických přípravků, kromě antiandrogenní léčby u karcinomu prostaty. Skórovací systémy individuálního rizika existují již také pro jednotlivé látky, většina z nich využívá kromě klinických a echokardiografických parametrů i koncentraci natriuretických peptidů a srdečních troponinů. Tyto parametry je doporučeno využít rovněž k monitoringu vzniku případné kardiotoxicity během léčby. Jako faktor pro zařazení do vysokého rizika používají většinou hodnoty LVEF <50 %do středního rizika potom u většiny terapeutik zvýšené koncentrace natriuretických peptidů a troponinu. Pacienti na check-point inhibitorech jsou ve zvýšeném riziku rozvoje myokarditidy a měli by být sledováni pomocí srdečních troponinů odebíraných 1x týdně po dobu alespoň prvních 6 týdnů. Monitoring by měl pokračovat i po ukončení léčby, srdeční selhání se totiž může vyvinout i s odstupem několika let.
S problematikou srdečního selhání úzce souvisí onemocnění síní, především fibrilace síní (FiS). FiS často provází chronické srdeční selhání se zachovalou ejekční frakcí (HFpEF), vyskytuje se ale mnohdy i v souvislosti s jinými srdečními dysfunkcemi. Velikost a funkce srdečních síní může být zhodnocena nejrůznějšími zobrazovacími metodami počínaje echokardiografií, podstatná je ale i zde role biomarkerů (natriuretické peptidy, vysoce senzitivní srdeční troponiny). Zvýšené koncentrace natriuretických peptidů při FiS mohou být také indikátorem hlubšího onemocnění síní. Přehledné postupy zhodnocení onemocnění síní zahrnující klinické, zobrazovací, biochemické a molekulární parametry zatím ale nejsou k dispozici. Další klinickou situací, kterou 2021 ESC doporučení rozebírají podrobněji, je myokarditida. Ta se etiologicky podílí na rozvoji srdečního selhání v závislosti na věku a regionu v 0,5–4 % případů. Chronická infekce EB virem je přítomná u 9–30 % dospělých pacientů s dilatační kardiomyopatií. Klinicky se myokarditida může projevovat různě, od nenápadných symptomů až po kardiogenní šok. Také v diagnostice myokarditid se uplatňují biomarkery, užitečné jsou především srdeční troponiny. Jejich koncentrace totiž vykazuje dynamické změny konzistentní s úrovní nekrózy myokardu. Stanovení troponinů pomáhá v tomto klinickém kontextu i v rámci indikace srdeční magnetické rezonance. Ta by měla být provedena u všech pacientů s anamnézou ukazující na možnost myokarditidy a relevantními změnami na EKG a s abnormálními nálezy na echokardiografii nebo elevovanou koncentrací troponinů, pakliže byla vyloučena ischemická choroba srdeční, nebo je nepravděpodobná. Nemocní s akutní myokarditidou by měli být hospitalizováni po dobu alespoň 48 hodin, a to zejména pokud došlo k elevaci koncentrací troponinů, nebo pokud je přítomná porucha srdeční funkce, a/nebo byly při příjmu detekovány arytmie. Odběr natriuretických peptidů a srdečních troponinů má dle nových ESC doporučení význam také při zvýšeném podezření na srdeční amyloidózu, respektive s ní spojenou kardiomyopatii. Tu totiž provází neúměrně zvýšená koncentrace NT-proBNP v porovnání s projevy srdečního selhání, a přetrvávající elevace troponinu. Samotná diagnostika vyžaduje pokročilé zobrazovací metody a/nebo srdeční biopsii.
V rámci hlavních sdělení autoři shrnují, že pacienti se srdečním selháním jsou stále klasifikováni především podle hodnot LVEF. V diagnostice srdečního selhání hrají zásadní roli měření koncentrace natriuretických peptidů a poté echokardiografie. Diagnostika chronického srdečního selhání se zachovalou srdeční frakcí (HFpEF) vyžaduje objektivní známky strukturálního kardiálního poškození nebo funkčních abnormalit a zároveň elevované koncentrace natriuretických peptidů a současnou přítomnost diastolické dysfunkce nebo zvýšených plnicích tlaků levé komory. Pacienti se srdečním selháním by měli být pravidelně monitorováni pro anémii a nedostatek železa a případně náležitě suplementováni. V sekci identifikující mezery v současné evidenci autoři zmiňují, že v tuto chvíli nejsou k dispozici definitivní výsledky studií o roli biomarkerů v diagnostice srdečního selhání. Zároveň by uvítali provedení více randomizovaných klinických studií věnujících se screeningu srdečního selhání u asymptomatických osob a jakou roli by tento screening měl pro jejich prognózu. Žádané jsou rovněž práce, které demonstrují vliv stanovování biomarkerů na prognózu v kontextu identifikace osob v riziku rozvoje srdečního selhání, respektive v kontextu řízení terapie u pacientů s již rozvinutým selháním. V problematice akutního srdečního selhání chybí práce, které popisují vliv provedení zobrazovacích metod a stanovení biomarkerů na prognózu nemocných, v problematice kardiomyopatií potom práce, které umožní jejich kvalitnější fenotypizaci (třídění) na základě biomarkerů, genetického testování a zobrazovacích metod a které umožní nasazení terapie na míru konkrétnímu pacientovi. A v neposlední řadě dosud nejsou k dispozici ani dostatečně validované protokoly pro diagnostiku chronického srdečního selhání s mírně sníženou a zachovalou ejekční frakcí. Biomarkery se objevují také mezi indikátory kvality péče o nemocné se srdečním selháním.
